Clear Sky Science · pt
O impacto dos mutantes K-Ras Gly12 na homeostase e na tumorigênese do epitélio colônico
Por que pequenas mudanças em um gene do câncer importam
O câncer de cólon está entre os mais frequentes, e muitos casos são impulsionados por danos em um gene chamado KRAS. Médicos já sabiam há muito tempo que pacientes cujos tumores carregam mutações em KRAS frequentemente respondem mal ao tratamento, mas nem todas as alterações em KRAS são iguais. Este estudo faz uma pergunta aparentemente simples, com grandes implicações para a medicina de precisão: três versões muito comuns do KRAS mutante se comportam de forma diferente no cólon, e essas diferenças podem ser aproveitadas para tratamentos mais eficazes e personalizados?
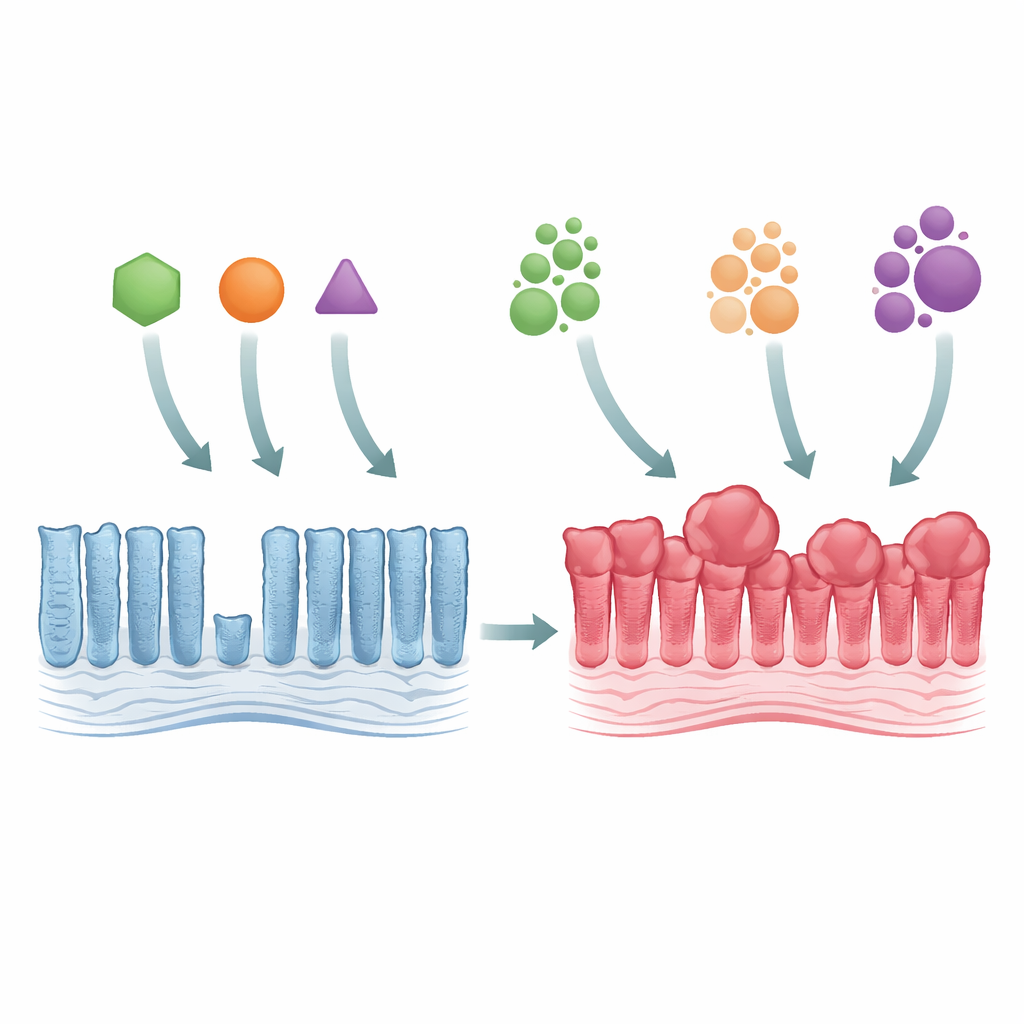
Do revestimento intestinal normal ao crescimento tumoral inicial
Os pesquisadores usaram camundongos geneticamente modificados para imitar três mutações principais em KRAS, todas afetando o mesmo bloco de construção da proteína (chamado Gly12) mas alterando-o de modos diferentes (G12C, G12D e G12V). Quando qualquer um desses mutantes foi ativado no revestimento do cólon, o tecido tornou-se mais espesso e compactado, com glândulas alongadas e um excesso de células maduras. Apesar desse crescimento excessivo, a zona efetiva de proliferação celular não se expandiu muito, sugerindo que o problema não era um aumento na taxa de nascimento das células, e sim uma redução no turnover celular. Todos os três mutantes ativaram fortemente uma via de controle de crescimento conhecida como MAPK e eliminaram certos tipos especializados de células intestinais, mostrando que até mudanças genéticas sutis podem perturbar amplamente o equilíbrio interno do intestino.
Tumores com aparência semelhante, resultados muito distintos
Para estudar a formação de câncer, a equipe combinou cada mutante KRAS com a perda do gene supressor de tumor APC, um evento inicial comum no câncer de cólon humano. Os tumores resultantes apresentaram aparência semelhante ao microscópio e exibiram ativação comparável da via central de crescimento conduzida por KRAS. Ainda assim, os camundongos não tiveram o mesmo desfecho. Animais com a mutação G12D desenvolveram mais tumores e tiveram menor sobrevida; os com G12V ficaram em posição intermediária; e os com G12C tiveram menos tumores e viveram mais. Mini-tumores cultivados em laboratório a partir desses animais (organoides) também mostraram respostas distintas a novos fármacos bloqueadores de KRAS: tumores G12D foram os mais difíceis de eliminar, G12V os mais sensíveis, e G12C ficou entre eles e respondeu de forma diferente dependendo do modo de ação do medicamento.
Programas de crescimento compartilhados entre camundongos e humanos
Para entender o que essas mutações faziam dentro das células, os pesquisadores mediram a atividade gênica global e os níveis de proteínas tanto em tumores de camundongo quanto em conjuntos de dados de câncer de cólon humano. Eles encontraram uma “assinatura” comum de KRAS mutante entre as espécies: genes que impulsionam a divisão celular e suportam a via de crescimento MAPK estavam ligados, enquanto muitos genes de metabolismo energético foram reduzidos, consistente com o redesenho do uso de combustível pelas células cancerosas. Vários genes e proteínas que atuam em loops de retroalimentação — seja amplificando ou tentando conter a sinalização KRAS — apareceram consistentemente elevados. A equipe também observou maior atividade em vias ligadas à inflamação e sinais imunes, sugerindo que essas mutações podem ajudar a moldar um microambiente favorável ao tumor já nas fases iniciais da doença.
Uma vulnerabilidade especial em um dos mutantes
Apesar desse programa central compartilhado, um mutante, G12C, se destacou. Tumores com G12C exibiram ativação extra de vias de desenvolvimento como Wnt/β-catenina e Notch, que influenciam como as células decidem seu destino. Isoladamente, drogas que bloqueiam essas vias tiveram efeitos semelhantes em todos os mutantes. Mas quando os pesquisadores combinaram um inibidor específico de KRAS G12C com bloqueadores de Wnt ou Notch, os organoides com a mutação G12C encolheram dramaticamente, muito mais do que os com G12D ou G12V. Isso sugere que tumores dirigidos por G12C dependem especialmente dessas vias adicionais e podem ser levados ao colapso quando tanto KRAS quanto suas rotas auxiliares são alvo simultaneamente.
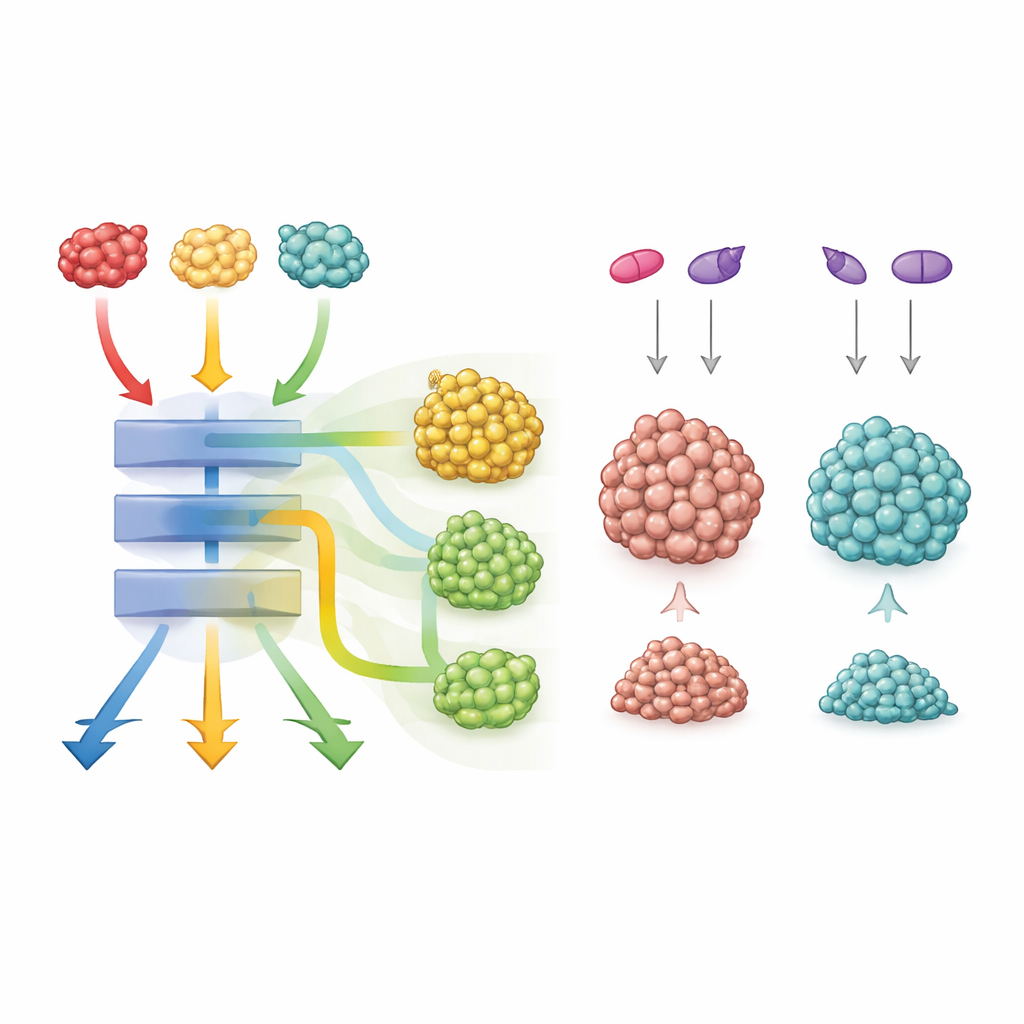
O que isso significa para o cuidado com o câncer no futuro
No geral, o estudo mostra que três mutações em KRAS no mesmo exato resíduo podem produzir tumores de cólon que se parecem, mas se comportam de maneiras bem distintas em termos de crescimento, sobrevida e resposta a drogas. Todas compartilham um motor central poderoso que impulsiona a divisão celular e o redesenho metabólico, ainda que cada mutante ajuste redes de sinalização adicionais à sua maneira. Para os pacientes, isso significa que saber apenas que um tumor é “KRAS-mutante” não é suficiente. Entender exatamente qual alteração de KRAS está presente, e quais vias parceiras ela recruta, pode orientar combinações mais inteligentes de drogas direcionadas — especialmente para o mutante G12C, em que associar inibidores de KRAS a bloqueadores de Wnt ou Notch pode oferecer um novo caminho para tratamentos melhores.
Citação: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Palavras-chave: mutações KRAS, câncer de cólon, terapia alelo-específica, sinalização tumoral, direcionamento combinado