Clear Sky Science · es
El impacto de los mutantes K-Ras Gly12 en la homeostasis y la tumorigénesis del epitelio colónico
Por qué importan los pequeños cambios en un gen cancerígeno
El cáncer de colon es uno de los tumores más comunes, y muchos casos están impulsados por alteraciones en un gen llamado KRAS. Los médicos saben desde hace tiempo que los pacientes cuyos tumores presentan mutaciones en KRAS suelen responder peor al tratamiento, pero no todas las variantes de KRAS son iguales. Este estudio plantea una pregunta aparentemente sencilla con grandes implicaciones para la medicina de precisión: ¿se comportan de forma distinta en el colon tres versiones muy frecuentes de KRAS mutante, y pueden esas diferencias convertirse en tratamientos más eficaces y personalizados?
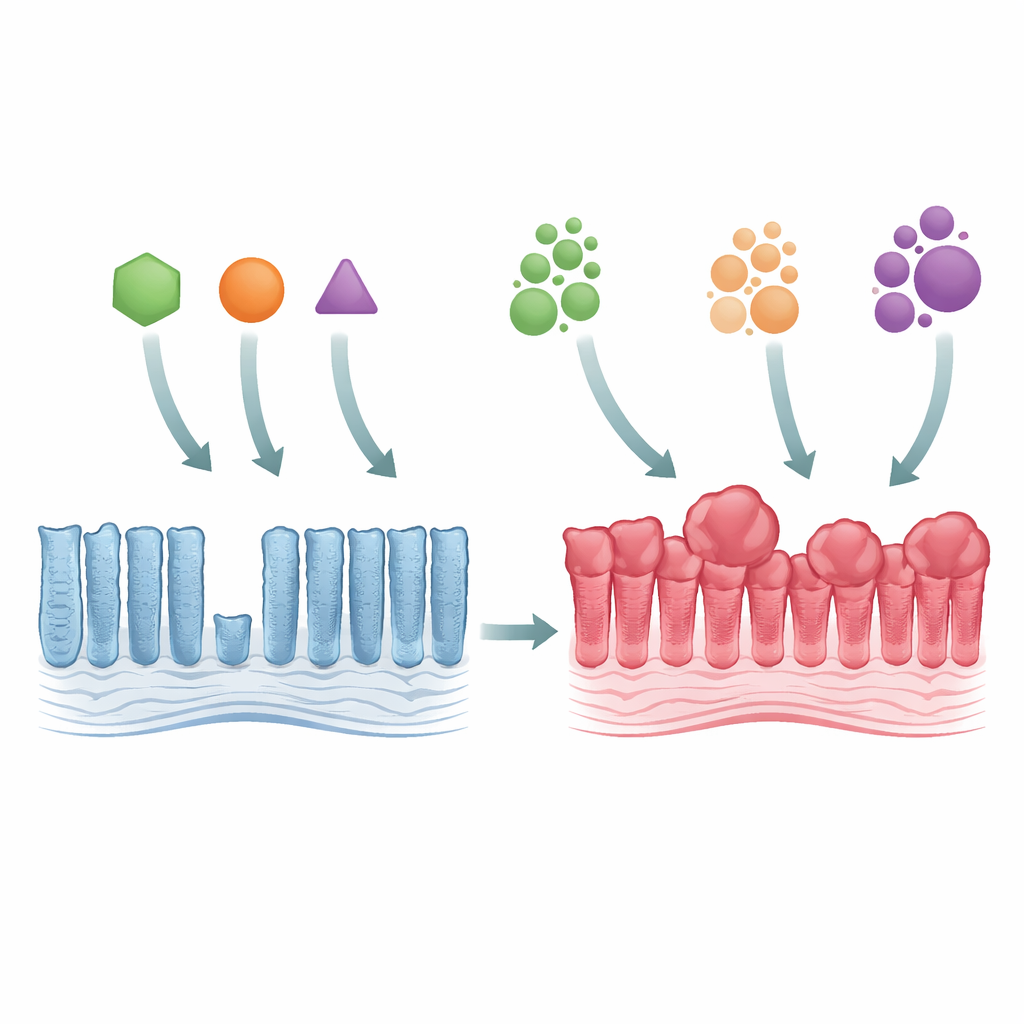
Del revestimiento intestinal normal al crecimiento tumoral temprano
Los investigadores utilizaron ratones genéticamente modificados para imitar tres mutaciones principales de KRAS, todas afectan al mismo aminoácido de la proteína (denominado Gly12) pero lo cambian de distintas maneras (G12C, G12D y G12V). Cuando cualquiera de estos mutantes se activó en el epitelio colónico, el tejido se engrosó y se volvió más denso, con glándulas alargadas y una sobreabundancia de células maduras. A pesar de este crecimiento excesivo, la zona real donde las células se dividían no se expandió mucho, lo que sugiere que el problema no era un nacimiento celular más rápido sino una renovación celular más lenta. Los tres mutantes activaron con fuerza una vía de control del crecimiento conocida como MAPK, y eliminaron ciertos tipos celulares especializados del intestino, demostrando que incluso cambios genéticos sutiles pueden alterar de forma amplia el equilibrio interno del intestino.
Tumores de aspecto similar, resultados muy distintos
Para estudiar la formación de cáncer, el equipo combinó cada mutante de KRAS con la pérdida del gen supresor tumoral APC, un evento temprano frecuente en el cáncer de colon humano. Los tumores resultantes presentaban un aspecto microscópico similar y mostraban una activación comparable de la vía central de crecimiento impulsada por KRAS. Sin embargo, los ratones no evolucionaron igual. Los animales con la mutación G12D desarrollaron más tumores y tuvieron la supervivencia más corta; los con G12V quedaron en un punto intermedio; y los con G12C tuvieron menos tumores y vivieron más tiempo. Mini-tumores cultivados en el laboratorio a partir de estos ratones (organoides) también mostraron respuestas distintas a nuevos fármacos bloqueadores de KRAS: los tumores con G12D fueron los más difíciles de eliminar, los G12V los más sensibles, y los G12C quedaron en un término medio y respondieron de manera diferente según el modo de acción del fármaco.
Programas de crecimiento compartidos entre ratones y humanos
Para entender qué estaban haciendo estas mutaciones dentro de las células, los investigadores midieron la actividad génica global y los niveles de proteínas tanto en tumores de ratón como en conjuntos de datos de cáncer de colon humano. Encontraron una “firma” común de KRAS mutante entre especies: genes que impulsan la división celular y sostienen la vía de crecimiento MAPK estaban activados, mientras que muchos genes del metabolismo energético se replegaban, coherente con la reconfiguración del uso de combustible por parte de las células cancerosas. Varios genes y proteínas que actúan en bucles de retroalimentación —ya sea amplificando o intentando frenar la señalización de KRAS— estaban continuamente elevados. El equipo también observó mayor actividad en vías relacionadas con la inflamación y señales inmunitarias, lo que sugiere que estas mutaciones pueden ayudar a moldear desde temprano un microambiente favorable al tumor.
Una vulnerabilidad especial en un mutante
A pesar de este programa central compartido, un mutante, G12C, destacó. Los tumores con G12C mostraron activación adicional de vías del desarrollo como Wnt/β-catenina y Notch, que influyen en cómo las células deciden su destino. Por sí solos, los fármacos que bloquean estas vías tuvieron efectos similares en todos los mutantes. Pero cuando los investigadores combinaron un inhibidor específico de KRAS para G12C con bloqueadores de Wnt o Notch, los organoides con la mutación G12C se redujeron dramáticamente, mucho más que los G12D o G12V. Esto sugiere que los tumores impulsados por G12C dependen de forma particularmente intensa de estas vías adicionales y pueden colapsar cuando se atacan a la vez KRAS y sus rutas complementarias.
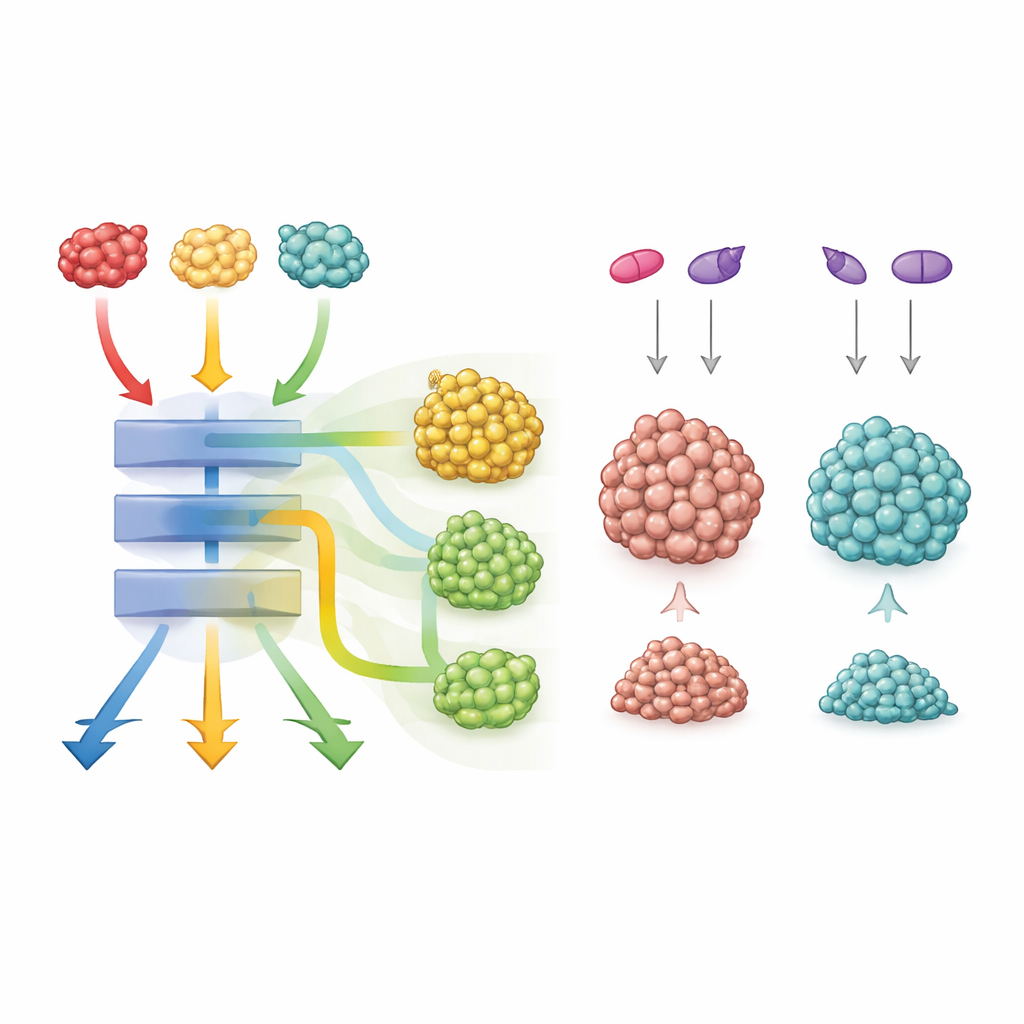
Qué significa esto para el cuidado del cáncer en el futuro
En conjunto, el estudio muestra que tres mutaciones de KRAS en exactamente la misma posición pueden producir tumores de colon que se parecen entre sí pero se comportan de manera bastante distinta en cuanto a crecimiento, supervivencia y respuesta a fármacos. Todas comparten un motor central potente que impulsa la división celular y la reprogramación metabólica, pero cada mutante ajusta redes de señalización adicionales a su manera. Para los pacientes, esto implica que saber simplemente que un tumor es “mutante en KRAS” no basta. Conocer exactamente qué alteración de KRAS está presente, y qué vías socias activa, podría guiar combinaciones más inteligentes de fármacos dirigidos—especialmente para el mutante G12C, donde asociar inhibidores de KRAS con bloqueadores de Wnt o Notch podría ofrecer una nueva vía hacia tratamientos más eficaces.
Cita: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Palabras clave: mutaciones KRAS, cáncer de colon, terapia específica de alelo, señalización tumoral, ataque combinado