Clear Sky Science · ru
Влияние мутантов K-Ras в положении Gly12 на гомеостаз и опухолеобразование в эпителии ободочной кишки
Почему крошечные изменения в гене рака имеют значение
Рак толстой кишки — одно из самых распространённых онкологических заболеваний, и во многих случаях его развитие запускается повреждением гена KRAS. Врачи давно заметили, что пациенты с опухолями, несущими мутации KRAS, часто хуже реагируют на лечение, однако не все изменения в KRAS одинаковы. В этом исследовании задают кажущимся простым, но важным для точной медицины вопрос: ведут ли себя три очень распространённые версии мутантного KRAS по‑разному в толстой кишке, и можно ли эти различия использовать для более эффективных индивидуальных терапий?
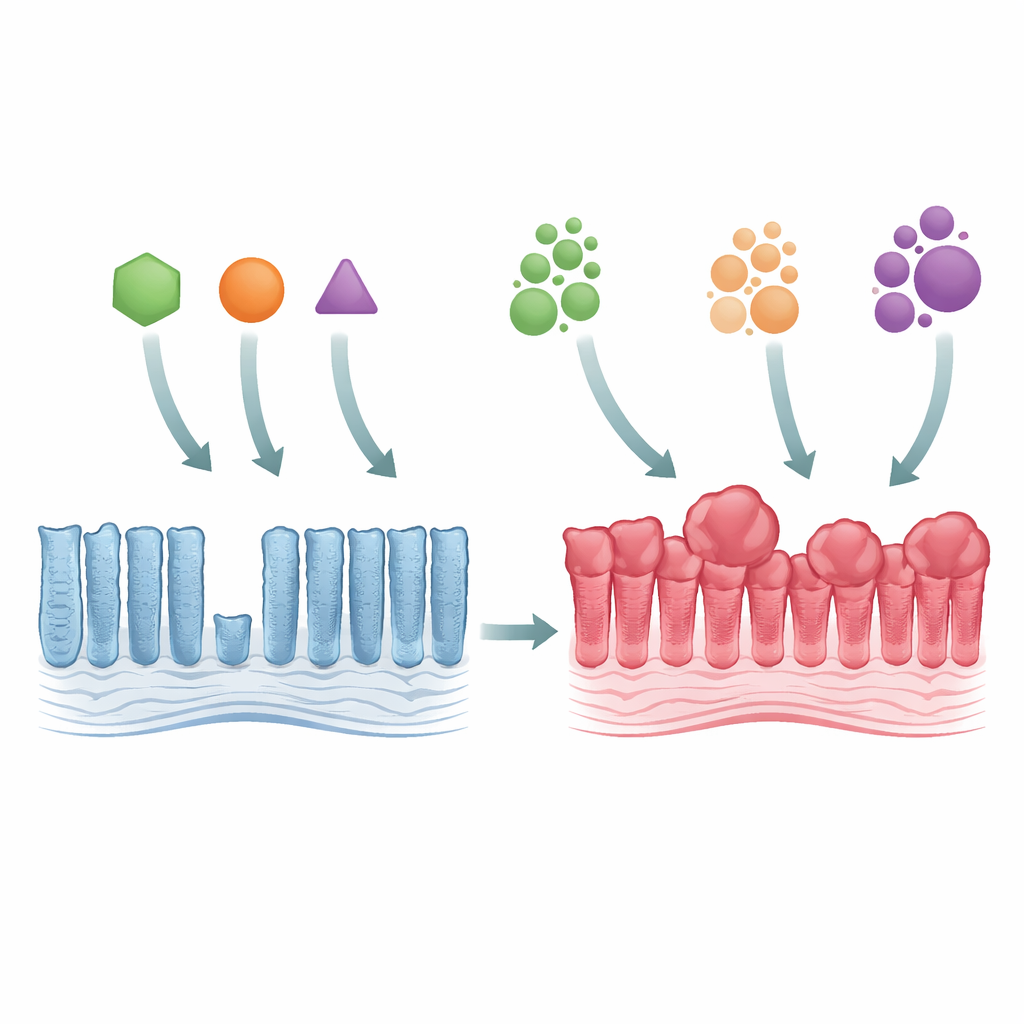
От нормального слизистого слоя к раннему росту опухоли
Исследователи использовали генетически модифицированных мышей, чтобы смоделировать три основных мутации KRAS, каждая из которых затрагивает один и тот же строительный блок белка (называемый Gly12), но заменяет его по‑разному (G12C, G12D и G12V). При включении любой из этих мутаций в слизистой оболочке толстой кишки ткань утолщалась и становилась более плотной, с удлинёнными железами и избытком зрелых клеток. Несмотря на это разрастание, зона активного деления клеток практически не расширялась, что указывает на то, что проблема заключалась не в увеличении скорости рождения клеток, а в замедленном их обновлении. Все три мутации сильно активировали сигнальный путь контроля роста MAPK и уничтожали определённые специализированные клетки кишечника, показывая, что даже тонкие генетические изменения способны широко нарушать внутреннее равновесие кишечника.
Опухоли похожи внешне, но имеют разные исходы
Чтобы изучить формирование рака, команда совместила каждую мутацию KRAS с потерей опухолевого супрессора APC, что является распространённым ранним событием при раке толстой кишки у человека. Получившиеся опухоли под микроскопом выглядели похоже и демонстрировали сопоставимую активацию основного сигнального пути, запускаемого KRAS. Однако результаты для животных различались. У мышей с мутацией G12D развивалось наибольшее число опухолей и была самая короткая выживаемость, у G12V показатели были промежуточными, а у G12C — меньше опухолей и более длительная жизнь. Мини‑опухоли, выращенные в лаборатории из этих мышей (органоиды), также показали разные ответы на новые блокаторы KRAS: опухоли G12D были наименее чувствительны к уничтожению, G12V — наиболее чувствительны, а G12C заняли промежуточное положение и реагировали по‑разному в зависимости от механизма действия препарата.
Общие программы роста у мышей и людей
Чтобы понять, что именно эти мутации делают внутри клеток, исследователи измеряли глобальную активность генов и уровни белков как в мышиных опухолях, так и в наборах данных по раку толстой кишки человека. Они выявили общую «подпись» мутантного KRAS между видами: включались гены, стимулирующие деление клеток и поддерживающие путь роста MAPK, тогда как многие гены энергетического обмена были понижены, что согласуется с перенастройкой путей использования топлива в раковых клетках. Несколько генов и белков, участвующих в петлях обратной связи — либо усиливающих, либо пытающихся ограничить сигнал KRAS — постоянно повышались. Также команда отметила усиление активности путей, связанных с воспалением и иммунными сигналами, что даёт основание полагать, что эти мутации могут способствовать формированию микроокружения, благоприятного для опухоли, на ранних стадиях болезни.
Особая уязвимость одного из мутантов
Несмотря на общий базовый набор эффектов, один мутант — G12C — выделялся. Опухоли с G12C демонстрировали дополнительную активацию путей развития, таких как Wnt/β‑catenin и Notch, которые влияют на принятие клетками решений о собственной судьбе. По отдельности препараты, блокирующие эти пути, оказывали схожие эффекты на все мутации. Но когда исследователи комбинировали специфический ингибитор KRAS для G12C с блокаторами Wnt или Notch, органоиды с мутацией G12C значительно уменьшались в размерах — гораздо сильнее, чем органоиды с G12D или G12V. Это говорит о том, что опухоли, вызванные G12C, особенно зависят от этих дополнительных путей и могут быть «дожаты», если одновременно таргетировать и KRAS, и его вспомогательные маршруты.
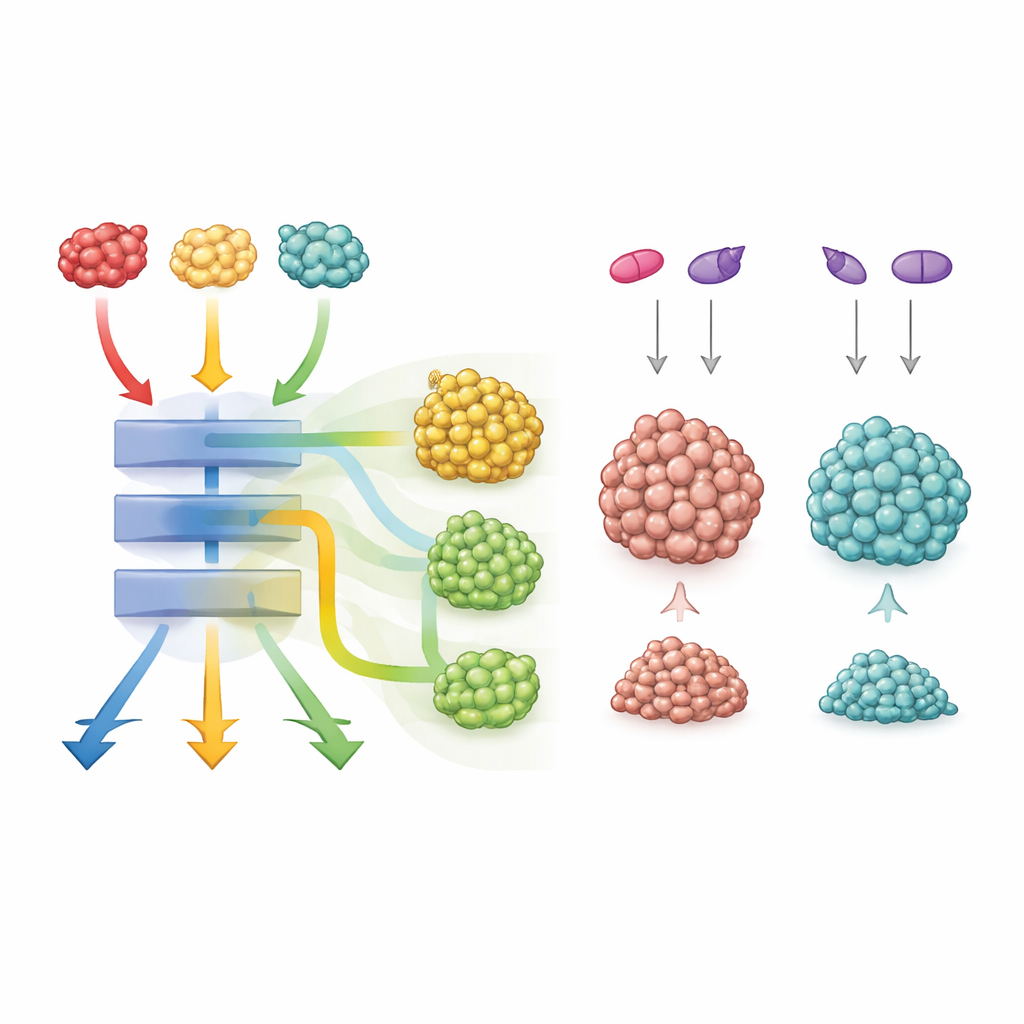
Что это значит для будущей онкологической помощи
В целом исследование показывает: три мутации KRAS в одной и той же позиции могут давать опухоли толстой кишки, которые выглядят одинаково, но существенно различаются в темпах роста, выживаемости и отклике на лекарства. У всех них есть мощный общий «двигатель», стимулирующий деление клеток и метаболическую перенастройку, но каждая мутация по‑своему тонко настраивает дополнительные сигнальные сети. Для пациентов это означает: простого знания факта «мутация KRAS» недостаточно. Понимание того, какая именно модификация KRAS присутствует и какие сопряжённые пути она привлекает, может помочь подобрать более разумные комбинированные таргетные терапии — особенно для мутанта G12C, где сочетание ингибиторов KRAS с блокаторами Wnt или Notch может открыть новый путь к более эффективному лечению.
Цитирование: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Ключевые слова: мутации KRAS, рак толстой кишки, аллельно-специфическая терапия, опухолевые сигналы, комбинированное таргетирование