Clear Sky Science · fr
L’impact des mutants K-Ras Gly12 sur l’homéostasie et la tumorigenèse de l’épithélium colique
Pourquoi de toutes petites variations dans un gène du cancer ont de l’importance
Le cancer du côlon est l’un des cancers les plus fréquents, et de nombreux cas sont entraînés par des altérations d’un gène appelé KRAS. Les cliniciens savent depuis longtemps que les patients dont les tumeurs portent des mutations de KRAS répondent souvent mal aux traitements, mais toutes les modifications de KRAS ne se valent pas. Cette étude pose une question apparemment simple mais aux grandes implications pour la médecine de précision : trois variantes très courantes de KRAS muté se comportent-elles différemment dans le côlon, et ces différences peuvent‑elles être exploitées pour des traitements plus efficaces et personnalisés ?
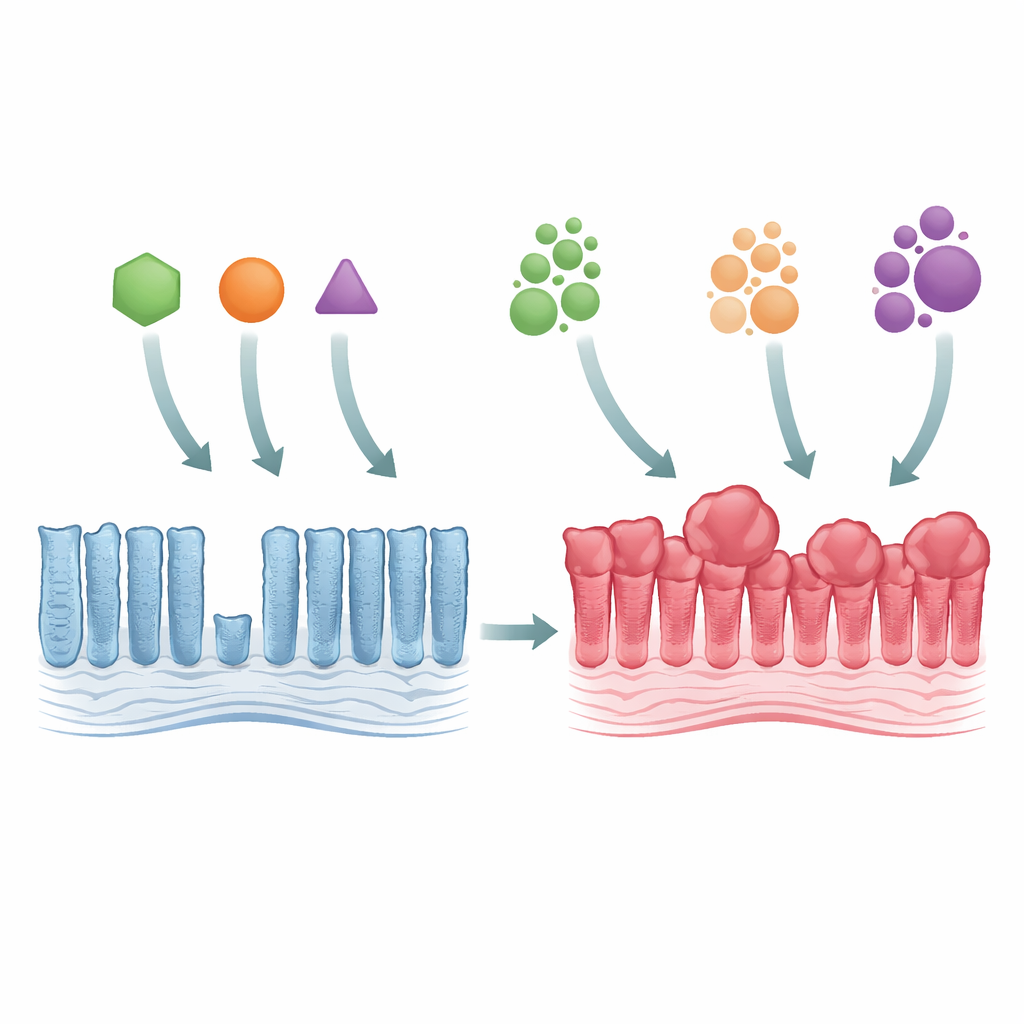
De la muqueuse intestinale normale aux premiers stades tumoraux
Les chercheurs ont utilisé des souris génétiquement modifiées pour reproduire trois mutations majeures de KRAS, qui touchent toutes le même acide aminé de la protéine (appelé Gly12) mais le modifient de façons différentes (G12C, G12D et G12V). Lorsque l’un ou l’autre de ces mutants était activé dans l’épithélium colique, le tissu s’épaississait et devenait plus encombré, avec des glandes allongées et un excès de cellules matures. Malgré cette hyperplasie, la zone de prolifération cellulaire ne s’étendait pas beaucoup, ce qui suggère que le problème n’était pas une augmentation de la naissance cellulaire mais un ralentissement du renouvellement. Les trois mutants activaient fortement une voie de contrôle de la croissance connue sous le nom de MAPK, et éliminaient certains types de cellules intestinales spécialisées, montrant que des modifications génétiques subtiles peuvent perturber largement l’équilibre interne de l’intestin.
Tumeurs d’aspect semblable, issues très différentes
Pour étudier la formation tumorale, l’équipe a combiné chaque mutant KRAS avec la perte du gène suppresseur de tumeur APC, un événement précoce fréquent dans le cancer du côlon humain. Les tumeurs obtenues se ressemblaient au microscope et présentaient une activation comparable de la voie de croissance centrale mise en marche par KRAS. Pourtant, l’issue chez les souris était différente selon le mutant. Les animaux portant la mutation G12D développaient le plus de tumeurs et avaient la survie la plus courte, ceux avec G12V avaient un phénotype intermédiaire, et les G12C formaient moins de tumeurs et vivaient plus longtemps. Des mini‑tumeurs cultivées en laboratoire à partir de ces souris (organoïdes) montraient aussi des réponses distinctes aux nouveaux médicaments bloquant KRAS : les tumeurs G12D étaient les plus difficiles à éliminer, G12V les plus sensibles, et G12C se situait entre les deux et répondait différemment selon le mode d’action du médicament.
Programmes de croissance partagés chez la souris et l’humain
Pour comprendre ce que faisaient ces mutations à l’intérieur des cellules, les chercheurs ont mesuré l’expression génétique globale et les niveaux protéiques dans les tumeurs murines et dans des jeux de données de cancer du côlon humain. Ils ont trouvé une « signature » commune des mutants KRAS entre les espèces : des gènes favorisant la division cellulaire et soutenant la voie MAPK étaient activés, tandis que de nombreux gènes du métabolisme énergétique étaient réprimés, cohérent avec une réorganisation de l’utilisation du carburant par les cellules cancéreuses. Plusieurs gènes et protéines impliqués dans des boucles de rétroaction — amplifiant ou tentant de freiner la signalisation KRAS — étaient systématiquement augmentés. L’équipe a également observé une activité accrue de voies liées à l’inflammation et aux signaux immunitaires, laissant entendre que ces mutations peuvent contribuer tôt à façonner un microenvironnement favorable à la tumeur.
Une vulnérabilité particulière pour un mutant
Malgré ce programme central partagé, un mutant, G12C, se démarquait. Les tumeurs porteuses de G12C présentaient une activation supplémentaire de voies développementales telles que Wnt/β‑caténine et Notch, qui influencent les décisions de destin cellulaire. Pris isolément, les médicaments bloquant ces voies avaient des effets similaires sur tous les mutants. Mais lorsque les chercheurs ont combiné un inhibiteur spécifique de KRAS G12C avec des bloqueurs de Wnt ou de Notch, les organoïdes G12C ont régressé de façon spectaculaire, bien plus que ceux porteurs de G12D ou G12V. Cela suggère que les tumeurs drivées par G12C dépendent particulièrement de ces voies additionnelles et peuvent être renversées lorsque KRAS et ses voies auxiliaires sont ciblés simultanément.
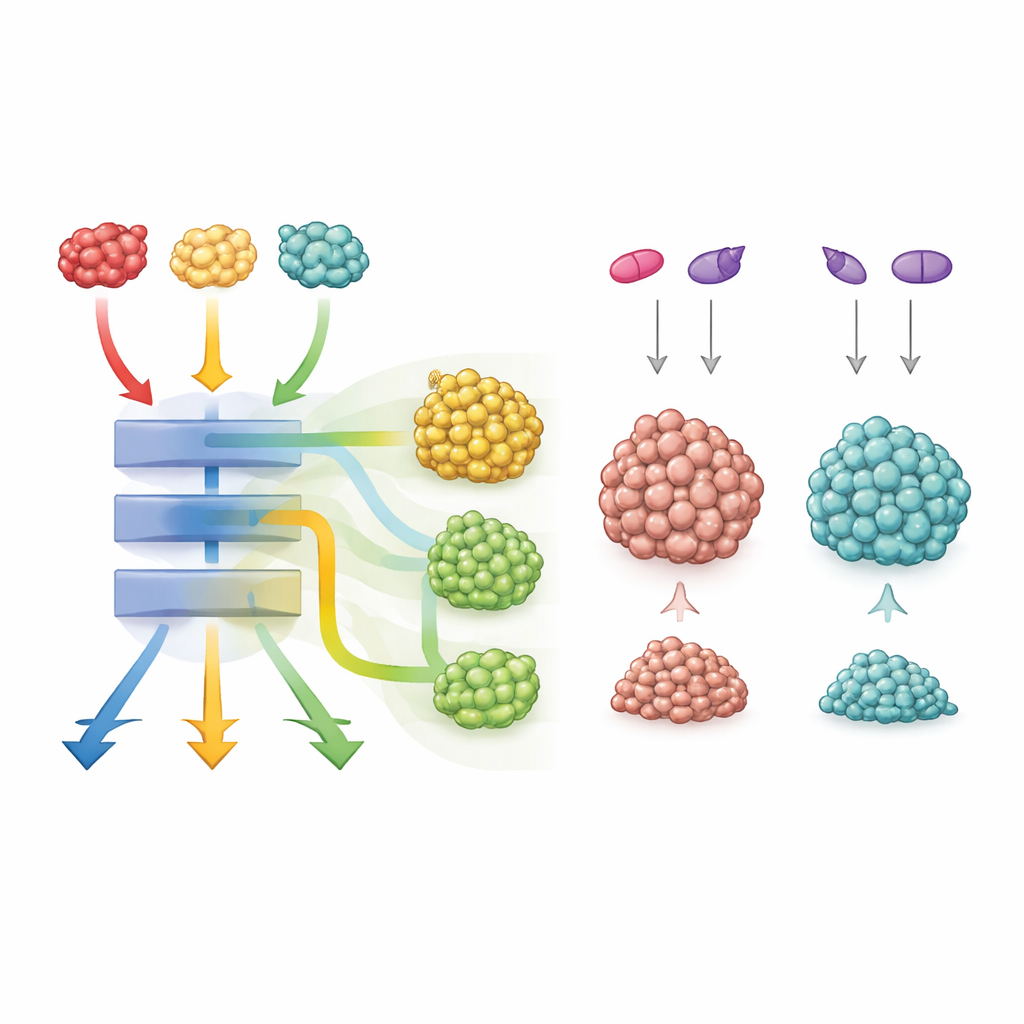
Ce que cela signifie pour les soins anticancéreux futurs
Dans l’ensemble, l’étude montre que trois mutations de KRAS au même endroit peuvent produire des tumeurs coliques d’apparence similaire mais au comportement très différent en termes de croissance, de survie et de réponse aux médicaments. Elles partagent toutes un moteur central puissant qui stimule la division cellulaire et la réorganisation métabolique, mais chaque mutant ajuste à sa manière des réseaux de signalisation supplémentaires. Pour les patients, cela signifie que savoir seulement qu’une tumeur est « KRAS‑mutée » ne suffit pas. Connaître précisément quelle altération de KRAS est présente, et quelles voies partenaires elle mobilise, pourrait orienter des combinaisons de thérapies ciblées plus intelligentes — en particulier pour le mutant G12C, où l’association d’inhibiteurs KRAS avec des bloqueurs de Wnt ou de Notch pourrait ouvrir une nouvelle voie vers des traitements améliorés.
Citation: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Mots-clés: mutations KRAS, cancer du côlon, thérapie spécifique d’allèle, signalisation tumorale, ciblage combiné