Clear Sky Science · it
L’impatto dei mutanti K-Ras Gly12 sull’omeostasi e sulla tumorigenesi nell’epitelio colico
Perché piccole variazioni in un gene del cancro contano
Il cancro del colon è uno dei tumori più comuni e molti casi sono guidati da alterazioni di un gene chiamato KRAS. I medici sanno da tempo che i pazienti i cui tumori presentano mutazioni di KRAS spesso rispondono male alle terapie, ma non tutte le variazioni di KRAS sono uguali. Questo studio pone una domanda apparentemente semplice ma con grandi implicazioni per la medicina di precisione: tre versioni molto comuni di KRAS mutato si comportano diversamente nel colon, e queste differenze possono essere sfruttate per terapie più efficaci e su misura?
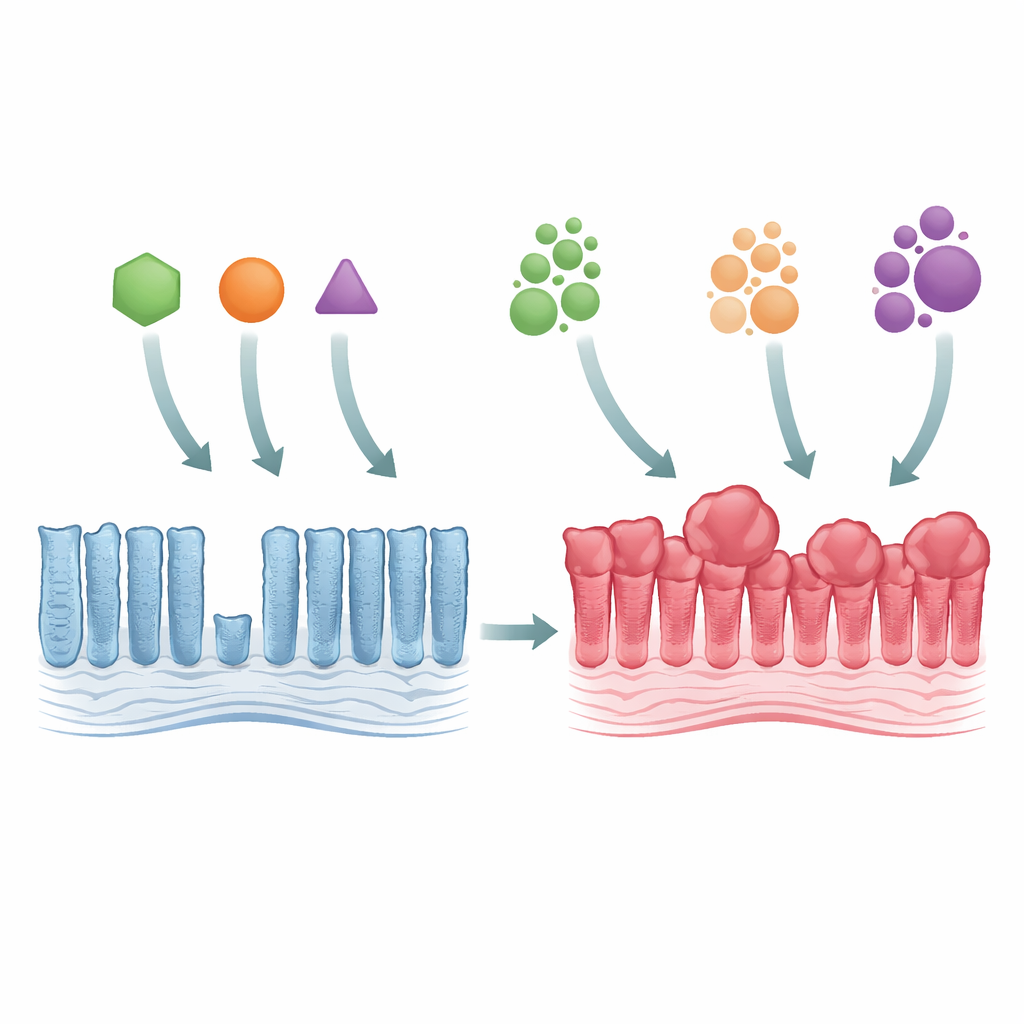
Dall’epitelio intestinale normale alla crescita tumorale iniziale
I ricercatori hanno usato topi geneticamente modificati per riprodurre tre principali mutazioni di KRAS, tutte interessanti lo stesso amminoacido della proteina (chiamato Gly12) ma alterandolo in modi diversi (G12C, G12D e G12V). Quando uno qualsiasi di questi mutanti veniva attivato nell’epitelio colico, il tessuto diventava più spesso e congestionato, con ghiandole allungate e un accumulo di cellule mature. Nonostante questa iperplasia, la zona in cui le cellule si dividevano non si espandeva molto, suggerendo che il problema non fosse una nascita cellulare più rapida ma un turnover cellulare rallentato. Tutti e tre i mutanti attivavano intensamente una via di controllo della crescita nota come MAPK e azzeravano alcuni tipi specializzati di cellule intestinali, dimostrando che anche cambiamenti genetici sottili possono perturbare ampiamente l’equilibrio interno dell’intestino.
Tumori che sembrano uguali, esiti molto diversi
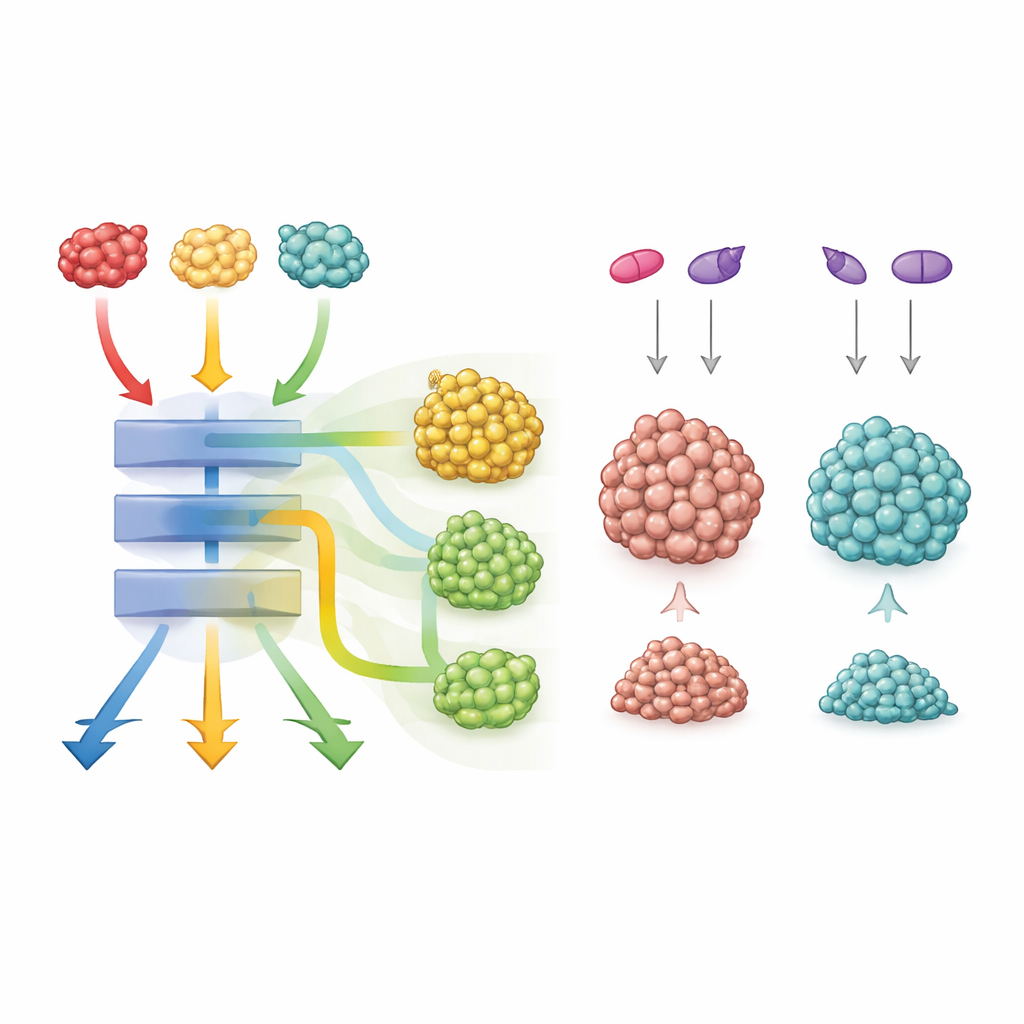
Per studiare la formazione del cancro, il gruppo ha combinato ciascun mutante KRAS con la perdita del gene oncosoppressore APC, un evento precoce comune nel cancro del colon umano. I tumori risultanti apparivano simili al microscopio e mostravano un’attivazione comparabile della via di crescita centrale indotta da KRAS. Tuttavia, i topi non andarono allo stesso modo. Gli animali con la mutazione G12D svilupparono il maggior numero di tumori e mostrarono la sopravvivenza più breve, quelli con G12V ebbero un quadro intermedio, e i soggetti con G12C presentarono meno tumori e vissero più a lungo. I mini-tumori coltivati in vitro da questi topi (organoidi) mostrarono anch’essi risposte diverse a nuovi farmaci inibitori di KRAS: i tumori G12D erano i più difficili da eliminare, i G12V i più sensibili, e i G12C si collocavano in mezzo e reagivano in modo differente a seconda del meccanismo d’azione del farmaco.
Programmi di crescita condivisi tra topi e umani
Per capire cosa facessero queste mutazioni all’interno delle cellule, i ricercatori misurarono l’espressione genica globale e i livelli proteici sia nei tumori murini sia in dataset di cancro del colon umano. Trovarono una “firma” comune dei mutanti KRAS attraverso le specie: geni che favoriscono la divisione cellulare e sostengono la via di crescita MAPK risultavano attivati, mentre molti geni del metabolismo energetico erano soppressi, coerente con il riprogrammarsi dell’uso del combustibile nelle cellule tumorali. Diverse proteine e geni che agiscono in circuiti di feedback — sia amplificando sia cercando di contenere la segnalazione KRAS — risultarono costantemente elevati. Il gruppo osservò inoltre un’aumentata attività in percorsi legati all’infiammazione e ai segnali immunitari, suggerendo che queste mutazioni possano contribuire a plasmare precocemente un microambiente favorevole al tumore.
Una vulnerabilità specifica in un mutante
Nonostante questo nucleo condiviso, un mutante, G12C, si distingueva. I tumori portatori di G12C mostravano una maggiore attivazione di vie di sviluppo come Wnt/β-catenina e Notch, che influenzano le decisioni di destino cellulare. Da soli, i farmaci che bloccano queste vie avevano effetti simili su tutti i mutanti. Ma quando i ricercatori combinarono un inibitore specifico per KRAS G12C con bloccanti di Wnt o Notch, gli organoidi con la mutazione G12C si ridussero in modo drammatico, molto più di quelli con G12D o G12V. Questo suggerisce che i tumori guidati da G12C fanno particolarmente affidamento su questi percorsi supplementari e possono essere spinti oltre il punto di non ritorno quando sia KRAS sia le sue vie di supporto vengono bersagliate insieme.
Cosa significa per la cura del cancro in futuro
Complessivamente, lo studio mostra che tre mutazioni di KRAS nella stessa posizione possono produrre tumori del colon che si assomigliano morfologicamente ma si comportano in modo molto diverso in termini di crescita, sopravvivenza e risposta ai farmaci. Tutti condividono un potente motore centrale che guida la divisione cellulare e il riprogrammarsi metabolico, tuttavia ogni mutante modula a modo suo reti di segnalazione aggiuntive. Per i pazienti, questo significa che sapere semplicemente che un tumore è “KRAS-mutato” non basta. Conoscere esattamente quale alterazione di KRAS è presente e quali vie partner coinvolge potrebbe guidare combinazioni più intelligenti di farmaci mirati — specialmente per il mutante G12C, dove associare inibitori di KRAS con bloccanti di Wnt o Notch potrebbe offrire una nuova strada verso trattamenti migliori.
Citazione: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Parole chiave: mutazioni KRAS, cancro del colon, terapia allele-specifica, segnalazione tumorale, targeting combinato