Clear Sky Science · de
Die Auswirkungen von K‑Ras‑Gly12‑Mutanten auf Homöostase und Tumorentstehung im Kolonepithel
Warum winzige Veränderungen in einem Krebsgen wichtig sind
Darmkrebs gehört zu den häufigsten Krebserkrankungen, und viele Fälle werden durch Schädigungen eines Gens namens KRAS angetrieben. Ärztinnen und Ärzte wissen seit langem, dass Patientinnen und Patienten mit KRAS‑mutierten Tumoren oft schlecht auf Therapien ansprechen, doch nicht alle KRAS‑Veränderungen sind gleich. Diese Studie stellt eine auf den ersten Blick einfache, aber für die Präzisionsmedizin folgenreiche Frage: Verhalten sich drei sehr verbreitete Varianten des mutierten KRAS im Kolon unterschiedlich, und lassen sich diese Unterschiede in wirksamere, maßgeschneiderte Behandlungen ummünzen?
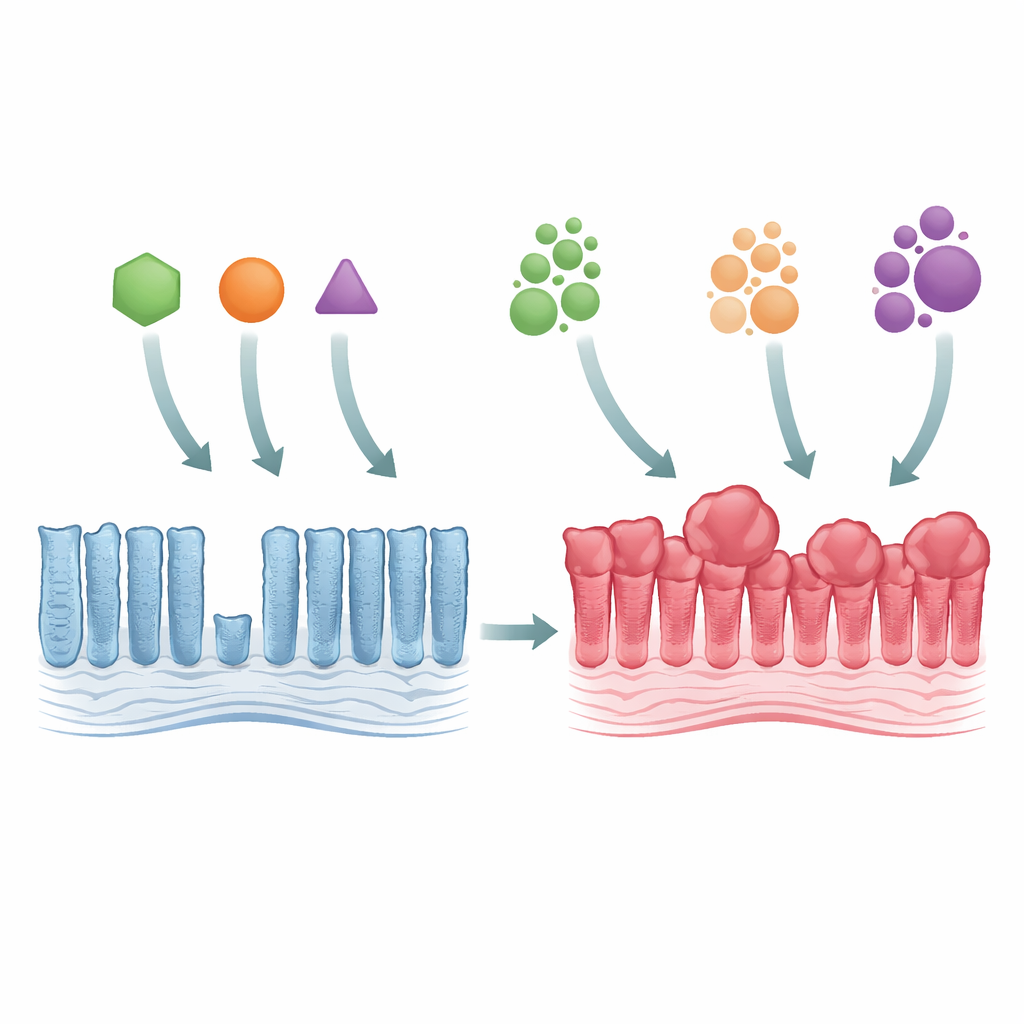
Vom normalen Darmepithel zum frühen Tumorwachstum
Die Forschenden verwendeten genetisch veränderte Mäuse, um drei wichtige KRAS‑Mutationen nachzubilden, die alle denselben Baustein des Proteins betreffen (genannt Gly12), ihn aber unterschiedlich verändern (G12C, G12D und G12V). Wenn einer dieser Mutanten in der Darmwand aktiviert wurde, wurde das Gewebe dicker und dichter, mit verlängerten Drüsen und einer Überfülle an ausgereiften Zellen. Trotz dieses Überwuchses dehnte sich die eigentliche Zone der Zellteilung nur wenig aus, was darauf hindeutet, dass das Problem nicht eine erhöhte Zellproliferation, sondern ein verlangsamter Zellersatz ist. Alle drei Mutanten aktivierten stark den wachstumssteuernden MAPK‑Signalweg und eliminierten bestimmte spezialisierte Darmzellen, was zeigt, dass selbst subtile genetische Änderungen das innere Gleichgewicht des Darms umfassend stören können.
Optisch ähnliche Tumoren, sehr unterschiedliche Verläufe
Um die Krebsentstehung zu untersuchen, kombinierten die Forschenden jede KRAS‑Mutation mit dem Verlust des Tumorsuppressorgens APC, ein häufiger früher Schritt beim menschlichen Darmkrebs. Die entstehenden Tumoren sahen unter dem Mikroskop ähnlich aus und zeigten eine vergleichbare Aktivierung des zentralen, von KRAS angetriebenen Wachstumspfads. Dennoch verlief die Erkrankung bei den Mäusen unterschiedlich. Tiere mit der G12D‑Mutation entwickelten die meisten Tumoren und hatten die kürzeste Überlebenszeit; solche mit G12V lagen im Mittelfeld; und Mäuse mit G12C hatten weniger Tumoren und lebten länger. Mini‑Tumoren, die im Labor aus diesen Mäusen gezüchtet wurden (Organoide), zeigten ebenfalls unterschiedliche Reaktionen auf neue KRAS‑blockierende Wirkstoffe: G12D‑Tumoren waren am schwersten zu eliminieren, G12V am empfindlichsten, und G12C lag dazwischen und reagierte je nach Wirkungsweise des Medikaments unterschiedlich.
Geteilte Wachstumsprogramme bei Maus und Mensch
Um zu verstehen, was diese Mutationen in den Zellen bewirken, maßen die Forschenden die globale Genaktivität und Proteinmengen sowohl in Maus‑Tumoren als auch in Datensätzen menschlicher Darmkrebserkrankungen. Sie fanden eine gemeinsame KRAS‑mutante „Signatur“ über die Arten hinweg: Gene, die die Zellteilung vorantreiben und den MAPK‑Wachstumsweg unterstützen, waren hochreguliert, während viele Gene des Energiestoffwechsels heruntergefahren waren — im Einklang damit, dass Krebszellen ihren Umgang mit Energie umstellen. Mehrere Gene und Proteine, die in Rückkopplungsschleifen wirken — entweder zur Verstärkung oder zur Eindämmung der KRAS‑Signalgebung — waren konsistent erhöht. Das Team beobachtete außerdem eine stärkere Aktivität in Signalwegen, die mit Entzündung und Immunantworten verknüpft sind, was darauf hindeutet, dass diese Mutationen früh im Krankheitsverlauf zur Ausbildung eines tumorfreundlichen Mikro‑Umfelds beitragen könnten.
Eine besondere Verwundbarkeit bei einem Mutanten
Trotz dieses gemeinsamen Kernprogramms stach ein Mutant hervor: G12C. Tumoren mit G12C zeigten eine zusätzliche Aktivierung von Entwicklungswegen wie Wnt/β‑Catenin und Notch, die beeinflussen, wie Zellen über ihr Schicksal entscheiden. Allein griffen Hemmstoffe dieser Wege bei den verschiedenen Mutanten ähnlich. Kombinierte man jedoch einen G12C‑spezifischen KRAS‑Inhibitor mit Blockern von Wnt oder Notch, schrumpften die G12C‑Organoide dramatisch — deutlich stärker als die Organoide mit G12D oder G12V. Das deutet darauf hin, dass G12C‑getriebene Tumoren besonders stark auf diese zusätzlichen Wege angewiesen sind und sich durch gleichzeitiges Anvisieren von KRAS und seinen Helferwegen besonders effektiv angreifen lassen.
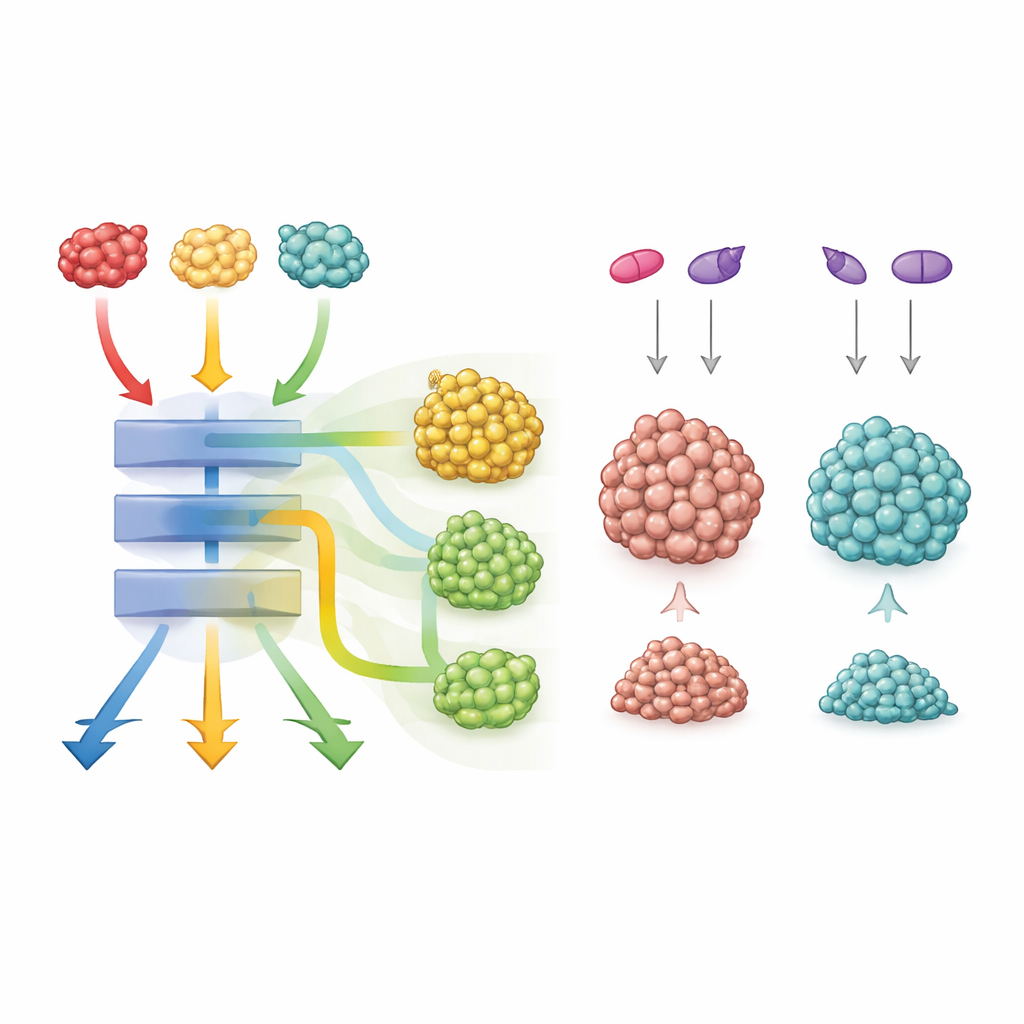
Was das für die zukünftige Krebsbehandlung bedeutet
Insgesamt zeigt die Studie, dass drei KRAS‑Mutationen an genau derselben Position Kolontumoren hervorrufen können, die gleich aussehen, sich aber deutlich in Wachstum, Prognose und Ansprechen auf Medikamente unterscheiden. Sie teilen zwar einen mächtigen Kernmotor, der Zellteilung und den Stoffwechsel umprogrammiert, doch jeder Mutant justiert zusätzliche Signalnetzwerke auf seine Weise. Für Patientinnen und Patienten bedeutet das: Die Information, dass ein Tumor „KRAS‑mutiert“ ist, reicht nicht aus. Zu wissen, welche konkrete KRAS‑Veränderung vorliegt und welche Partnerwege sie aktiviert, könnte klügere Kombinationen zielgerichteter Therapien ermöglichen — besonders beim G12C‑Mutanten, bei dem die Kombination von KRAS‑Inhibitoren mit Wnt‑ oder Notch‑Blockern einen neuen Weg zu besseren Behandlungen eröffnen könnte.
Zitation: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Schlüsselwörter: KRAS‑Mutationen, Darmkrebs, allelenspezifische Therapie, Tumorsignalgebung, Kombinationszielsetzung