Clear Sky Science · pl
Wpływ mutacji K-Ras Gly12 na homeostazę i nowotworzenie w nabłonku okrężnicy
Dlaczego drobne zmiany w genie nowotworowym mają znaczenie
Rak jelita grubego jest jednym z najczęstszych nowotworów, a wiele przypadków jest napędzanych uszkodzeniem genu o nazwie KRAS. Lekarze od dawna wiedzą, że pacjenci, których guzy niosą mutacje KRAS, często słabiej odpowiadają na leczenie, ale nie wszystkie zmiany w KRAS są jednakowe. To badanie stawia pozornie proste pytanie o dalekosiężnych konsekwencjach dla medycyny precyzyjnej: czy trzy bardzo powszechne warianty zmutowanego KRAS zachowują się inaczej w okrężnicy i czy te różnice można wykorzystać do skuteczniejszych, dopasowanych terapii?
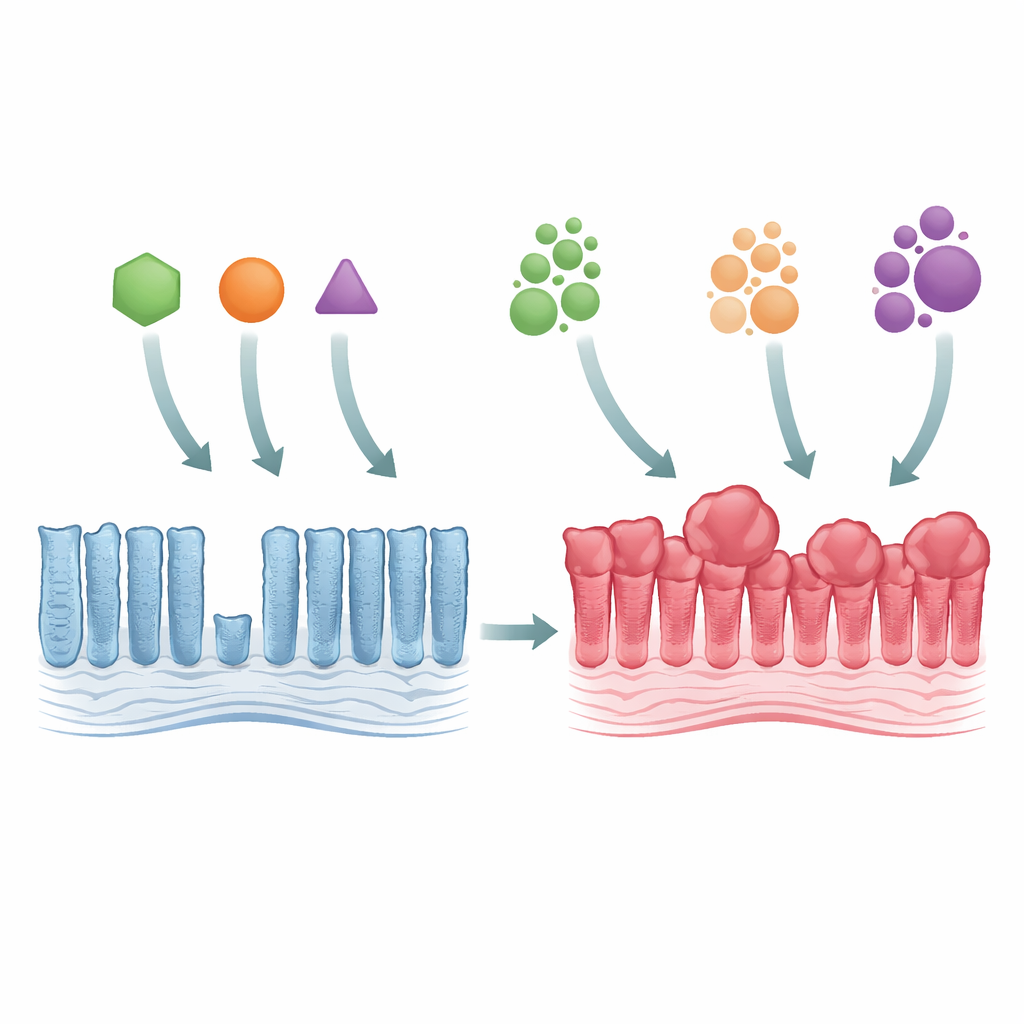
Od normalnej wyściółki jelita do wczesnego wzrostu guza
Naukowcy wykorzystali genetycznie zmodyfikowane myszy, aby odtworzyć trzy główne mutacje KRAS, wszystkie dotyczące tego samego aminokwasu w białku (zwanego Gly12), ale zmieniając go na różne sposoby (G12C, G12D i G12V). Gdy dowolny z tych mutantów został aktywowany w nabłonku okrężnicy, tkanka stała się grubsza i bardziej zagęszczona, z wydłużonymi gruczołami i nadmiarem dojrzałych komórek. Pomimo tego przerostu strefa dzielenia się komórek nie rozszerzyła się znacząco, co sugeruje, że problem nie wynikał z szybszego rodzenia się komórek, lecz z wolniejszego ich usuwania. Wszystkie trzy mutanty silnie aktywowały szlak kontroli wzrostu znany jako MAPK i eliminowały pewne wyspecjalizowane komórki jelitowe, pokazując, że nawet subtelne zmiany genetyczne mogą szeroko zaburzać wewnętrzną równowagę jelita.
Guz wyglądający podobnie, bardzo różne rezultaty
Aby zbadać formowanie się raka, zespół połączył każdy mutant KRAS z utratą genu supresorowego APC, co jest częstym wczesnym zdarzeniem w ludzkim raku jelita grubego. Powstałe guzy pod mikroskopem wyglądały podobnie i wykazywały porównywalną aktywację podstawowego szlaku wzrostowego napędzanego przez KRAS. Mimo to myszy nie miały jednakowego przebiegu choroby. Zwierzęta z mutacją G12D rozwijały najwięcej guzów i miały najkrótsze przeżycie, te z G12V zajmowały pozycję pośrednią, a z G12C miały mniej guzów i żyły dłużej. Mini-guzki hodowane w laboratorium z tych myszy (organoidy) również wykazały odrębne odpowiedzi na nowe leki blokujące KRAS: guzy G12D były najtrudniejsze do zabicia, G12V najwrażliwsze, a G12C znajdowało się pośrodku i reagowało odmiennie w zależności od mechanizmu działania leku.
Wspólne programy wzrostu u myszy i ludzi
Aby zrozumieć, co te mutacje robią wewnątrz komórek, badacze zmierzyli globalną aktywność genów i poziomy białek zarówno w guzach mysich, jak i w ludzkich zestawach danych raka jelita grubego. Odkryli wspólny „sygnaturowy” obraz mutanta KRAS między gatunkami: geny promujące podziały komórkowe i wspierające szlak MAPK były włączone, podczas gdy wiele genów związanych z metabolizmem energii było wyciszonych, co jest zgodne z przeprogramowaniem wykorzystania paliwa przez komórki nowotworowe. Kilka genów i białek działających w pętlach sprzężenia zwrotnego — wzmacniających lub próbujących hamować sygnalizację KRAS — było konsekwentnie podwyższonych. Zespół zaobserwował także silniejszą aktywność szlaków związanych z zapaleniem i sygnałami immunologicznymi, co sugeruje, że te mutacje mogą we wczesnym stadium choroby kształtować mikrośrodowisko sprzyjające nowotworowi.
Szczególna wrażliwość jednego wariantu
Mimo wspólnego rdzenia programów wzrostu, jeden mutant, G12C, wyróżniał się. Guzy z G12C wykazywały dodatkową aktywację szlaków rozwojowych, takich jak Wnt/β-katenina i Notch, które wpływają na decyzje dotyczące losów komórek. Same w sobie leki blokujące te szlaki miały podobne efekty we wszystkich mutantach. Jednak gdy badacze połączyli inhibitor KRAS specyficzny dla G12C z blokerami Wnt lub Notch, organoidy z mutacją G12C kurczyły się dramatycznie, znacznie bardziej niż te z G12D czy G12V. Sugeruje to, że guzy napędzane przez G12C szczególnie silnie polegają na tych dodatkowych szlakach i można je zmusić do krytycznego załamania, gdy celuje się jednocześnie w KRAS i jego wspomagające drogi.
Co to oznacza dla przyszłej opieki onkologicznej
Podsumowując, badanie pokazuje, że trzy mutacje KRAS w tym samym miejscu mogą dawać guzy okrężnicy, które wyglądają podobnie, ale różnią się znacząco pod względem wzrostu, przeżycia i odpowiedzi na leki. Wszystkie dzielą potężny rdzeń napędzający podziały komórkowe i przeprogramowanie metabolizmu, jednak każdy mutant dopracowuje dodatkowe sieci sygnalizacyjne na swój sposób. Dla pacjentów oznacza to, że samo stwierdzenie „mutacja KRAS” nie wystarcza. Dokładne rozpoznanie, która zmiana w KRAS występuje i które partnerujące szlaki są zaangażowane, może ukierunkować mądrzejsze kombinacje leków ukierunkowanych — szczególnie w przypadku mutanta G12C, gdzie łączenie inhibitorów KRAS z blokerami Wnt lub Notch może otworzyć nową drogę do lepszych terapii.
Cytowanie: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Słowa kluczowe: mutacje KRAS, rak jelita grubego, terapia specyficzna dla allelu, sygnalizacja nowotworowa, celowanie kombinacyjne