Clear Sky Science · nl
De invloed van K-Ras Gly12-mutaties op homeostase en tumorvorming in het colonepitheel
Waarom kleine veranderingen in een kankergen ertoe doen
Darmkanker is een van de meest voorkomende kankers, en veel gevallen worden aangedreven door schade aan een gen dat KRAS heet. Artsen weten al lange tijd dat patiënten met tumoren die KRAS-mutaties dragen vaak slecht op behandeling reageren, maar niet alle KRAS-veranderingen zijn hetzelfde. Deze studie stelt een schijnbaar eenvoudige vraag met grote gevolgen voor precisiegeneeskunde: gedragen drie veelvoorkomende varianten van gemuteerd KRAS zich verschillend in de dikke darm, en kunnen die verschillen worden omgezet in effectievere, op maat gemaakte behandelingen?
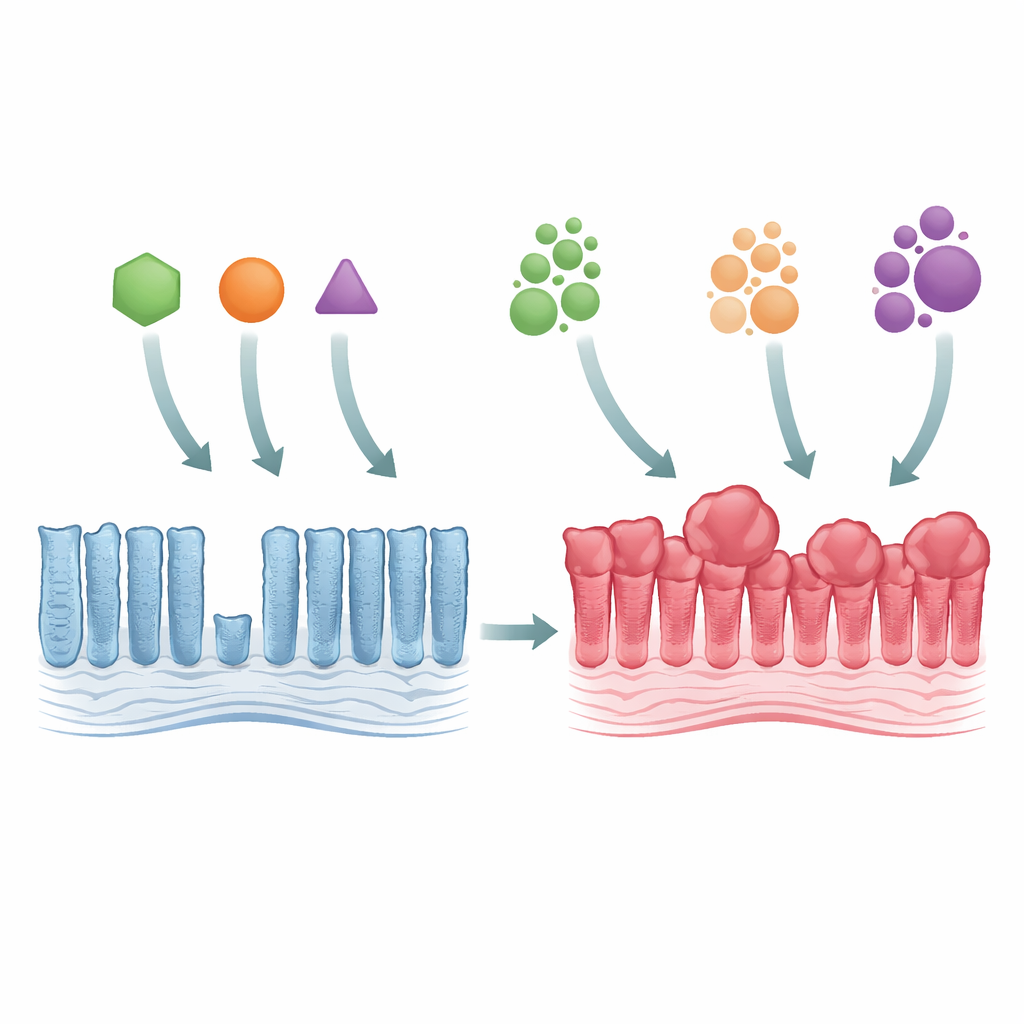
Van normaal darmslijmvlies tot vroege tumorgroei
De onderzoekers gebruikten genetisch gemodificeerde muizen om drie belangrijke KRAS-mutaties na te bootsen, die allemaal hetzelfde bouwsteen in het eiwit aantasten (genoemd Gly12) maar op verschillende wijze veranderen (G12C, G12D en G12V). Wanneer elk van deze mutanten in het colonepitheel werd aangezet, werd het weefsel dikker en dichter, met verlengde klieren en een overvloed aan rijpe cellen. Ondanks deze overgroei breidde de zone waar cellen zich delen zich niet sterk uit, wat suggereert dat het probleem niet snellere celdeling maar langzamere celverversing was. Alle drie de mutanten activeerden krachtig een groeiregulerend pad dat bekendstaat als MAPK, en ze wisten bepaalde gespecialiseerde darmcellen uit te roeien, wat laat zien dat zelfs subtiele genetische veranderingen de interne balans van de darm breed kunnen verstoren.
Gelijkende tumoren, zeer verschillende uitkomsten
Om tumorvorming te bestuderen combineerde het team elke KRAS-mutant met verlies van het tumorsuppressorgen APC, een veelvoorkomende vroege gebeurtenis bij menselijke darmkanker. De resulterende tumoren zagen er onder de microscoop vergelijkbaar uit en toonden vergelijkbare activatie van het kern-groeipad dat door KRAS wordt aangestuurd. Toch gingen de muizen niet hetzelfde aan. Dieren met de G12D-mutatie ontwikkelden de meeste tumoren en hadden de kortste overleving, die met G12V zaten ertussenin, en dieren met G12C hadden minder tumoren en leefden langer. Mini-tumoren die in het lab uit deze muizen werden gekweekt (organoïden) lieten ook onderscheidende reacties zien op nieuwe KRAS-remmende middelen: G12D-tumoren waren het moeilijkst te doden, G12V het gevoeligst, en G12C viel er tussenin en reageerde verschillend afhankelijk van het werkingsmechanisme van het geneesmiddel.
Gedeelde groeiprogramma’s bij muizen en mensen
Om te begrijpen wat deze mutaties in cellen deden, maten de onderzoekers de globale genactiviteit en eiwitniveaus in zowel muizentumoren als menselijke darmkankergegevenssets. Ze vonden een gemeenschappelijke KRAS-mutant “handtekening” over soorten heen: genen die celdeling stimuleren en het MAPK-groeipad ondersteunen waren aangezet, terwijl veel energie‑metabolismegenen waren teruggeschroefd, wat overeenkomt met het idee dat kankercellen hun brandstofgebruik herprogrammeren. Verschillende genen en eiwitten die in feedbacklussen werken — hetzij KRAS-signaal versterken of proberen het te remmen — waren consequent verhoogd. Het team zag ook sterkere activiteit in paden die verband houden met ontsteking en immuunsignalen, wat suggereert dat deze mutaties vroeg in de ziekte kunnen bijdragen aan het vormgeven van een tumorvriendelijke micro‑omgeving.
Een bijzondere kwetsbaarheid bij één mutant
Ondanks dit gedeelde kernprogramma stak één mutant, G12C, er uit. Tumoren met G12C toonden extra activatie van ontwikkelingspaden zoals Wnt/β‑catenine en Notch, die beïnvloeden hoe cellen hun lot bepalen. Op zichzelf hadden middelen die deze paden blokkeren vergelijkbare effecten over alle mutanten. Maar toen de onderzoekers een G12C‑specifieke KRAS-remmer combineerden met blokkades van Wnt of Notch, krimpten organoïden met de G12C‑mutatie dramatisch, veel meer dan die met G12D of G12V. Dit suggereert dat G12C‑gedreven tumoren bijzonder sterk leunen op deze aanvullende paden en dat ze omver te duwen zijn wanneer zowel KRAS als zijn hulproutes tegelijk worden aangepakt.
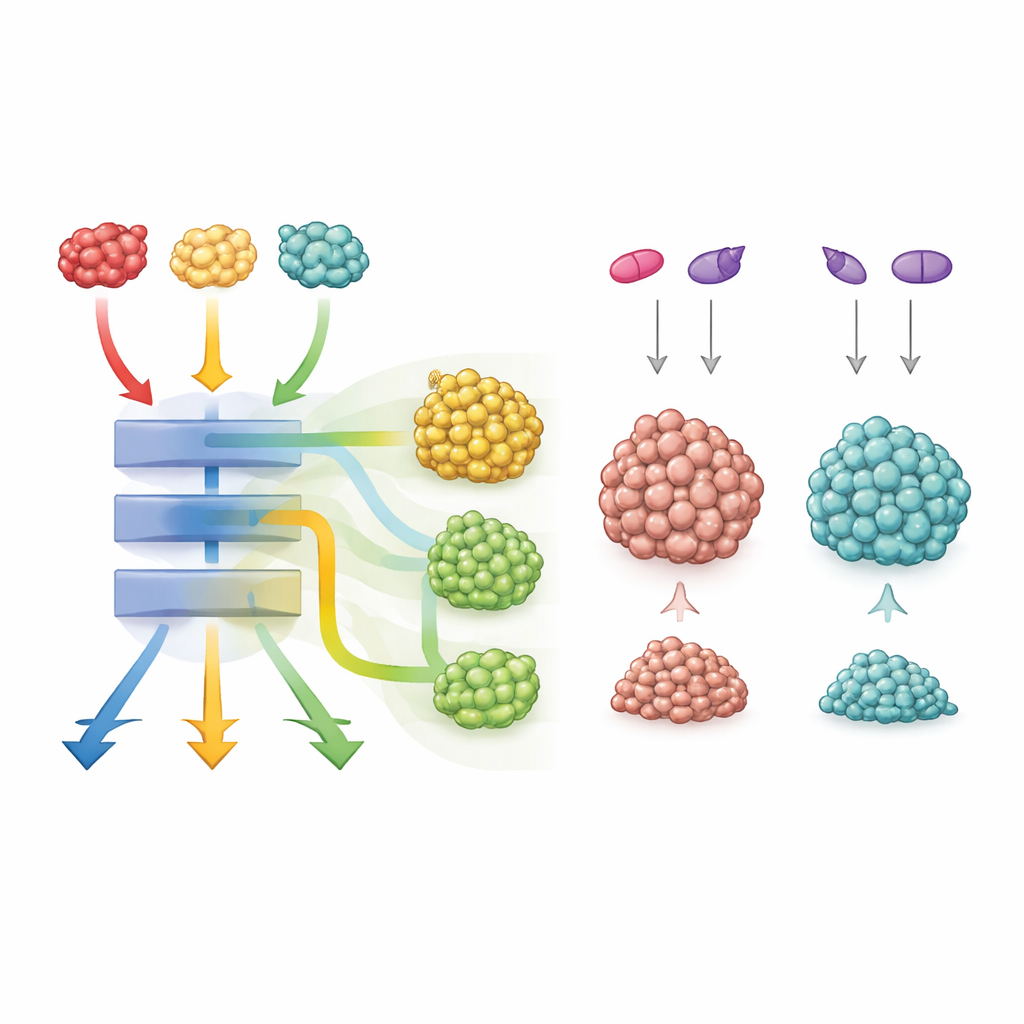
Wat dit betekent voor toekomstige kankerzorg
Samengevat toont de studie aan dat drie KRAS‑mutaties op precies dezelfde positie colon‑tumoren kunnen produceren die er hetzelfde uitzien maar heel verschillend reageren wat betreft groei, overleving en medicijngevoeligheid. Ze delen allemaal een krachtig kernmechanisme dat celdeling en metabole herprogrammering aandrijft, maar elke mutant stemt aanvullende signaalnetwerken op zijn eigen manier bij. Voor patiënten betekent dit dat alleen weten dat een tumor “KRAS‑gemuteerd” is niet genoeg is. Precies vaststellen welke KRAS‑verandering aanwezig is, en welke partnerpaden daarbij worden ingeschakeld, kan leiden tot slimmere combinaties van gerichte middelen — vooral voor de G12C‑mutant, waarbij het koppelen van KRAS‑remmers met Wnt‑ of Notch‑blokkers een nieuwe route naar betere behandelingen kan bieden.
Bronvermelding: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Trefwoorden: KRAS-mutaties, darmkanker, alleelspecifieke therapie, tumorsignalering, combinatiedoelgerichte behandeling