Clear Sky Science · zh
LINC-AC092535.5 调控 MICAL2 mRNA 水平以抑制鼻咽癌中 p53 介导的铁死亡
这项研究为何重要
鼻咽癌发生在鼻后和咽上部,一旦复发或转移仍然难以治愈。本研究揭示了一种隐蔽的分子“刹车”,帮助这些肿瘤细胞躲避一种新近被认可的细胞死亡形式——铁死亡,该过程依赖于铁和氧化损伤。通过揭示这一刹车机制,研究人员提出了使顽固性鼻咽肿瘤对治疗更易感的新策略。
癌细胞死亡的另一种路径
大多数抗癌药物通过触发如凋亡等已知的死亡程序来杀死肿瘤细胞,然而肿瘤常常学会逃避这些途径。铁死亡是一种不同的细胞死亡类型,由铁和一阵阵破坏细胞膜(尤其是线粒体)的活性氧分子驱动。许多对常规疗法耐受的癌症仍可通过诱导铁死亡被清除。鼻咽癌细胞对能够触发这一过程的药物特别敏感,表明如果科学家能弄清阻碍铁死亡的机制,就可以将其转化为治疗优势。
一种保护肿瘤免受铁驱动损伤的蛋白质
通过查询大型基因数据库和患者肿瘤样本,团队锁定了一个名为 MICAL2 的蛋白,先前与癌症生长和氧化化学有关。他们发现 MICAL2 在鼻咽肿瘤中的表达明显高于正常组织,且 MICAL2 水平高的患者往往疾病更晚期、转移更多、存活率更差。当研究者在鼻咽癌细胞系中降低 MICAL2 水平时,细胞的增殖和转移能力减弱,对诱导铁死亡的药物(如 Erastin 和索拉非尼)变得更敏感。细胞内铁水平、氧化应激及抗氧化平衡的测量结果均朝着支持增强铁死亡的方向变化,这在体外培养细胞和小鼠肿瘤模型中均得到验证。
一种新发现的 RNA 将防护提升
研究人员接着探究为何 MICAL2 在这些肿瘤中如此丰富。他们发现了一种此前未被表征的长非编码 RNA,命名为 LINC-AC092535.5,在头颈部癌症中强烈上调,并与 MICAL2 水平呈平行变化。与编码蛋白的 RNA 不同,该 RNA 起到调控者的作用。它能物理结合 MICAL2 的信使分子,并通过两种方式增强其生成:一方面增强 MICAL2 基因启动子的活性,另一方面减缓 MICAL2 mRNA 的降解。当沉默 LINC-AC092535.5 时,MICAL2 水平下降,铁死亡标志物上升,肿瘤细胞对铁驱动的氧化损伤更为易感。恢复 MICAL2 可部分逆转这些效应,表明该 RNA 与 MICAL2 协同构成一个增强回路,保护癌细胞免受铁死亡。
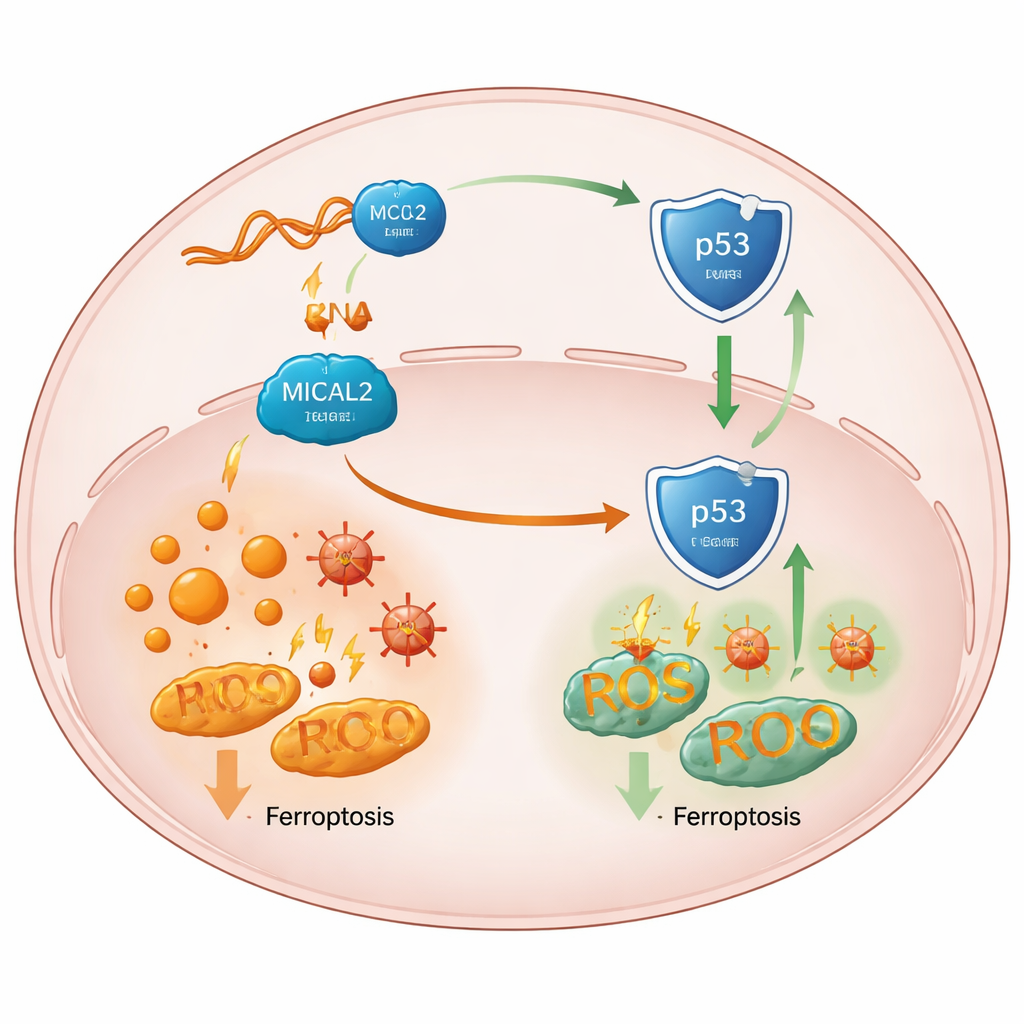
这一防护如何削弱关键的肿瘤守护者
进一步研究显示,MICAL2 的作用可追溯至 p53——这是一种关键的“守护者”蛋白,通常有助于抑制肿瘤并能在细胞受应激时促进铁死亡。高水平的 MICAL2 活性抑制了 p53 通路,而丧失 MICAL2 则在不改变其基因转录的情况下稳定并增加 p53 蛋白含量。研究者表明 MICAL2 能物理与 p53 及 MDM2 结合,MDM2 是一种标记 p53 以便降解的蛋白。MICAL2 帮助 MDM2 增加这些降解标签,使 p53 被送往细胞的降解系统,并从细胞核转运出来,而在细胞核内 p53 本可激活保护性基因。当敲低 MICAL2 或 LINC-AC092535.5 时,p53 在细胞核中累积,其下游信号向铁死亡倾斜,多种肿瘤细胞类型的铁驱动细胞死亡增加——除非 p53 本身被去除。
对未来治疗的意义
综上所述,这项工作勾画了鼻咽癌中的一条新型控制轴:长非编码 RNA LINC-AC092535.5 增强 MICAL2,而 MICAL2 又帮助剥夺 p53 的保护性作用,使肿瘤细胞得以抵抗铁死亡。干扰这一轴线——通过抑制该 RNA、阻断 MICAL2 或阻止 p53 被降解——可能恢复铁驱动的细胞死亡,并使现有的诱导铁死亡药物更有效。对于复发或治疗耐药的鼻咽癌患者,这类联合策略未来或能将癌细胞自身的铁和氧化应激反过来用作致死手段。
引用: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
关键词: 鼻咽癌, 铁死亡, p53, 长非编码 RNA, MICAL2