Clear Sky Science · fr
LINC-AC092535.5 régule le niveau d’ARNm de MICAL2 pour inhiber la ferroptose médiée par p53 dans le carcinome nasopharyngé
Pourquoi cette étude est importante
Le carcinome nasopharyngé est un cancer qui prend naissance derrière le nez et au-dessus de la gorge, et il reste difficile à guérir lorsqu’il récidive ou se dissémine. Cette étude met au jour un « frein » moléculaire caché qui aide ces cellules tumorales à échapper à une forme de mort cellulaire récemment caractérisée, la ferroptose, dépendante du fer et des dommages oxydatifs. En exposant ce frein, les chercheurs ouvrent la voie à de nouvelles stratégies pour rendre les tumeurs nasopharyngées réfractaires plus vulnérables au traitement.
Une autre façon pour les cellules cancéreuses de mourir
La plupart des médicaments anticancéreux cherchent à tuer les cellules tumorales en déclenchant des programmes de mort bien connus, tels que l’apoptose. Les tumeurs, cependant, apprennent souvent à échapper à ces voies. La ferroptose est un type distinct de mort cellulaire, entraîné par le fer et des explosions de molécules réactives de l’oxygène qui détruisent les membranes cellulaires, en particulier celles des mitochondries, les centrales énergétiques de la cellule. De nombreux cancers résistants aux thérapies standards peuvent néanmoins être poussés vers la ferroptose. Les cellules du carcinome nasopharyngé sont particulièrement sensibles aux médicaments qui déclenchent ce processus, ce qui suggère que la ferroptose pourrait devenir un avantage thérapeutique — à condition que les scientifiques comprennent ce qui la freine.
Une protéine qui protège les tumeurs des dommages liés au fer
En explorant de larges bases de données génétiques et des échantillons tumoraux de patients, l’équipe s’est intéressée à une protéine appelée MICAL2, déjà associée à la croissance tumorale et à la chimie oxydative. Ils ont constaté que les niveaux de MICAL2 sont nettement plus élevés dans les tumeurs nasopharyngées que dans les tissus normaux, et que les patients présentant davantage de MICAL2 ont tendance à avoir une maladie plus avancée, plus de métastases et une survie plus mauvaise. Lorsque les chercheurs ont réduit les niveaux de MICAL2 dans des lignées cellulaires de carcinome nasopharyngé, les cellules croissaient et se propageaient moins facilement, et elles devenaient beaucoup plus sensibles aux médicaments inducteurs de ferroptose tels que l’erastin et le sorafénib. Les mesures du fer, du stress oxydatif et de l’équilibre antioxydant ont toutes évolué dans un sens compatible avec une ferroptose accrue, à la fois dans des cellules en culture et dans des modèles tumoraux murins.
Un ARN nouvellement découvert qui renforce la protection
Les investigateurs se sont ensuite demandé pourquoi MICAL2 est si abondant dans ces tumeurs. Ils ont découvert un ARN long non codant auparavant non caractérisé, nommé LINC-AC092535.5, fortement élevé dans les cancers de la tête et du cou et corrélant avec les niveaux de MICAL2. Contrairement aux ARN qui codent des protéines, cet ARN agit comme un régulateur. Il se lie physiquement au message de MICAL2 et en stimule la production de deux manières : il augmente l’activité du promoteur du gène MICAL2 et il ralentit la dégradation de l’ARNm de MICAL2. Lorsque LINC-AC092535.5 a été éteint, les niveaux de MICAL2 ont chuté, les marqueurs de ferroptose ont augmenté et les cellules tumorales sont devenues plus vulnérables aux dommages oxydatifs dépendants du fer. La restauration de MICAL2 pouvait partiellement inverser ces effets, montrant que cet ARN et MICAL2 fonctionnent ensemble comme un circuit auto-renforçant qui protège les cellules cancéreuses de la ferroptose.
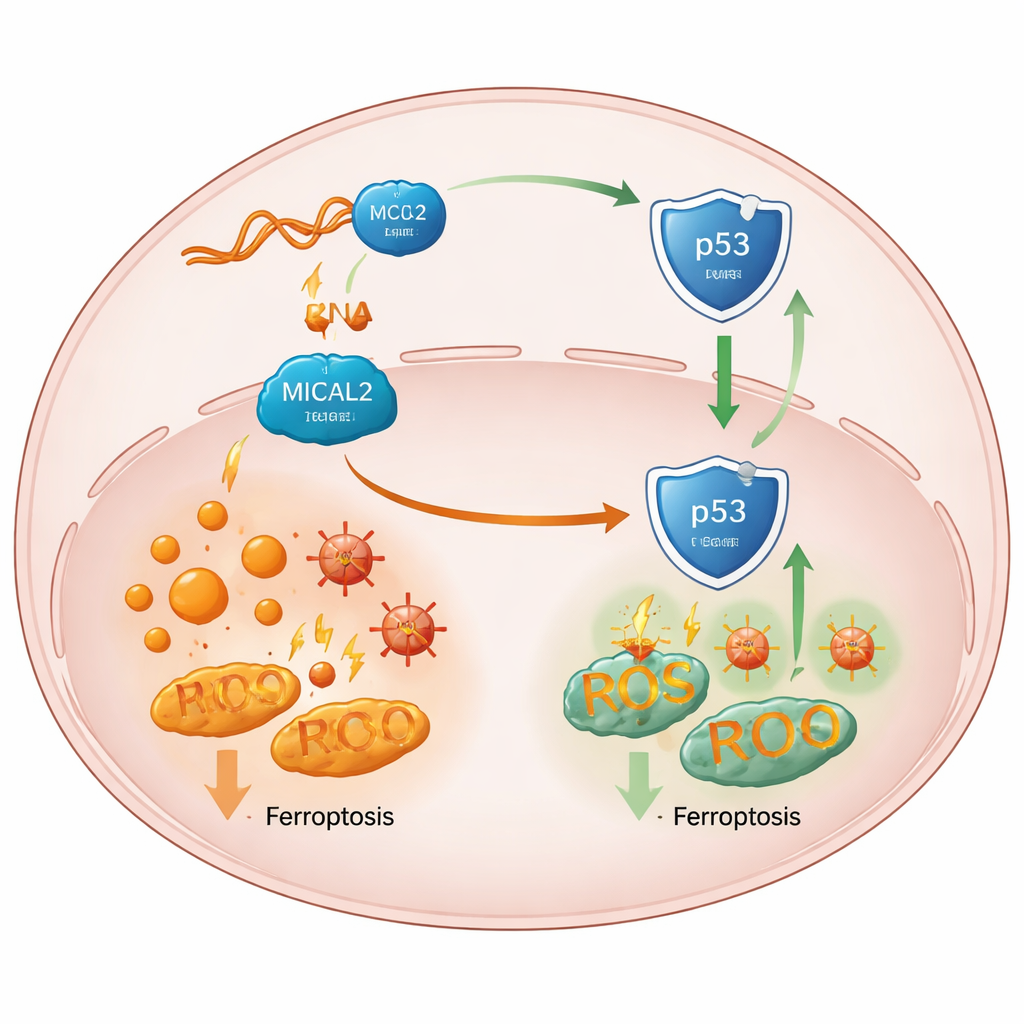
Comment la protection affaiblit un gardien clé de la tumeur
En creusant plus loin, l’équipe a rattaché l’effet de MICAL2 à p53, une protéine « gardienne » centrale qui aide normalement à prévenir les tumeurs et peut favoriser la ferroptose dans les cellules sous stress. Une activité élevée de MICAL2 atténuait la voie de p53, tandis que la perte de MICAL2 stabilisait et augmentait la protéine p53 sans modifier l’activité de son gène. Les chercheurs ont montré que MICAL2 s’associe physiquement à p53 et à MDM2, une protéine qui marque p53 pour sa destruction. MICAL2 favorise l’ajout de ces marques par MDM2, envoyant p53 vers le système d’élimination cellulaire et l’exportant hors du noyau, où il activerait sinon des gènes protecteurs. Lorsque MICAL2 ou LINC-AC092535.5 étaient inhibés, p53 s’accumulait dans le noyau, ses signaux en aval s’orientaient vers la ferroptose, et des cellules cancéreuses de plusieurs types montraient plus de mort dépendante du fer — à moins que p53 lui-même ne soit supprimé.
Ce que cela signifie pour les traitements futurs
Pris ensemble, ces travaux décrivent un nouvel axe de contrôle dans le carcinome nasopharyngé : l’ARN LINC-AC092535.5 stimule MICAL2, et MICAL2 à son tour contribue à supprimer l’influence protectrice de p53, permettant aux cellules tumorales de résister à la ferroptose. Interrompre cet axe — en inhibant l’ARN, en bloquant MICAL2 ou en empêchant la dégradation de p53 — pourrait restaurer la mort cellulaire induite par le fer et rendre les médicaments inducteurs de ferroptose existants plus efficaces. Pour les patients atteints d’un cancer nasopharyngé en rechute ou résistant au traitement, de telles combinaisons pourraient un jour offrir un moyen d’utiliser le fer et le stress oxydatif du cancer contre lui-même.
Citation: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Mots-clés: carcinome nasopharyngé, ferroptose, p53, ARN long non codant, MICAL2