Clear Sky Science · es
LINC-AC092535.5 regula el nivel de ARNm de MICAL2 para inhibir la ferroptosis mediada por p53 en el carcinoma nasofaríngeo
Por qué importa este estudio
El carcinoma nasofaríngeo es un cáncer que surge detrás de la nariz y por encima de la garganta, y sigue siendo difícil de curar cuando reaparece o se disemina. Este estudio revela un “freno” molecular oculto que ayuda a estas células tumorales a eludir una forma de muerte celular recientemente reconocida llamada ferroptosis, que depende del hierro y del daño oxidativo. Al exponer este freno, los investigadores señalan nuevas estrategias para hacer que los tumores nasofaríngeos resistentes sean más vulnerables al tratamiento.
Una vía diferente para que mueran las células cancerosas
La mayoría de los fármacos contra el cáncer intentan matar las células tumorales activando programas de muerte conocidos, como la apoptosis. Sin embargo, los tumores a menudo aprenden a eludir esas rutas. La ferroptosis es un tipo distinto de muerte celular impulsada por el hierro y por ráfagas de moléculas reactivas de oxígeno que destruyen las membranas celulares, particularmente en las mitocondrias, las centrales energéticas de la célula. Muchos cánceres que resisten las terapias estándar aún pueden ser inducidos a ferroptosis. Las células del carcinoma nasofaríngeo son especialmente sensibles a fármacos que desencadenan este proceso, lo que sugiere que la ferroptosis podría convertirse en una ventaja terapéutica—si los científicos pueden comprender qué la frena.
Una proteína que protege a los tumores del daño inducido por hierro
Al analizar grandes bases de datos genéticos y muestras tumorales de pacientes, el equipo se centró en una proteína llamada MICAL2, previamente vinculada al crecimiento canceroso y a la química oxidativa. Encontraron que los niveles de MICAL2 son notablemente más altos en tumores nasofaríngeos que en tejido normal, y los pacientes con más MICAL2 tienden a presentar enfermedad más avanzada, más metástasis y peor supervivencia. Cuando los investigadores redujeron los niveles de MICAL2 en líneas celulares de carcinoma nasofaríngeo, las células proliferaron y se diseminaron menos y se volvieron mucho más sensibles a fármacos que inducen ferroptosis, como Erastina y Sorafenib. Las medidas de hierro, estrés oxidativo y equilibrio antioxidante cambiaron en sentido compatible con una ferroptosis aumentada, tanto en células en cultivo como en modelos tumorales en ratones.
Un ARN recién descubierto que refuerza el escudo
Los investigadores preguntaron luego por qué MICAL2 es tan abundante en estos tumores. Descubrieron un ARN largo no codificante previamente no caracterizado, llamado LINC-AC092535.5, que está fuertemente elevado en cánceres de cabeza y cuello y refleja los niveles de MICAL2. A diferencia de los ARN que codifican proteínas, este ARN actúa como regulador. Se une físicamente al mensajero de MICAL2 y aumenta su producción de dos maneras: potencia la actividad del promotor del gen MICAL2 y ralentiza la degradación del ARNm de MICAL2. Cuando se silenció LINC-AC092535.5, los niveles de MICAL2 descendieron, aumentaron los marcadores de ferroptosis y las células tumorales se volvieron más vulnerables al daño oxidativo inducido por hierro. Restaurar MICAL2 pudo deshacer parcialmente estos efectos, mostrando que este ARN y MICAL2 funcionan juntos como un circuito reforzador que protege a las células cancerosas de la ferroptosis.
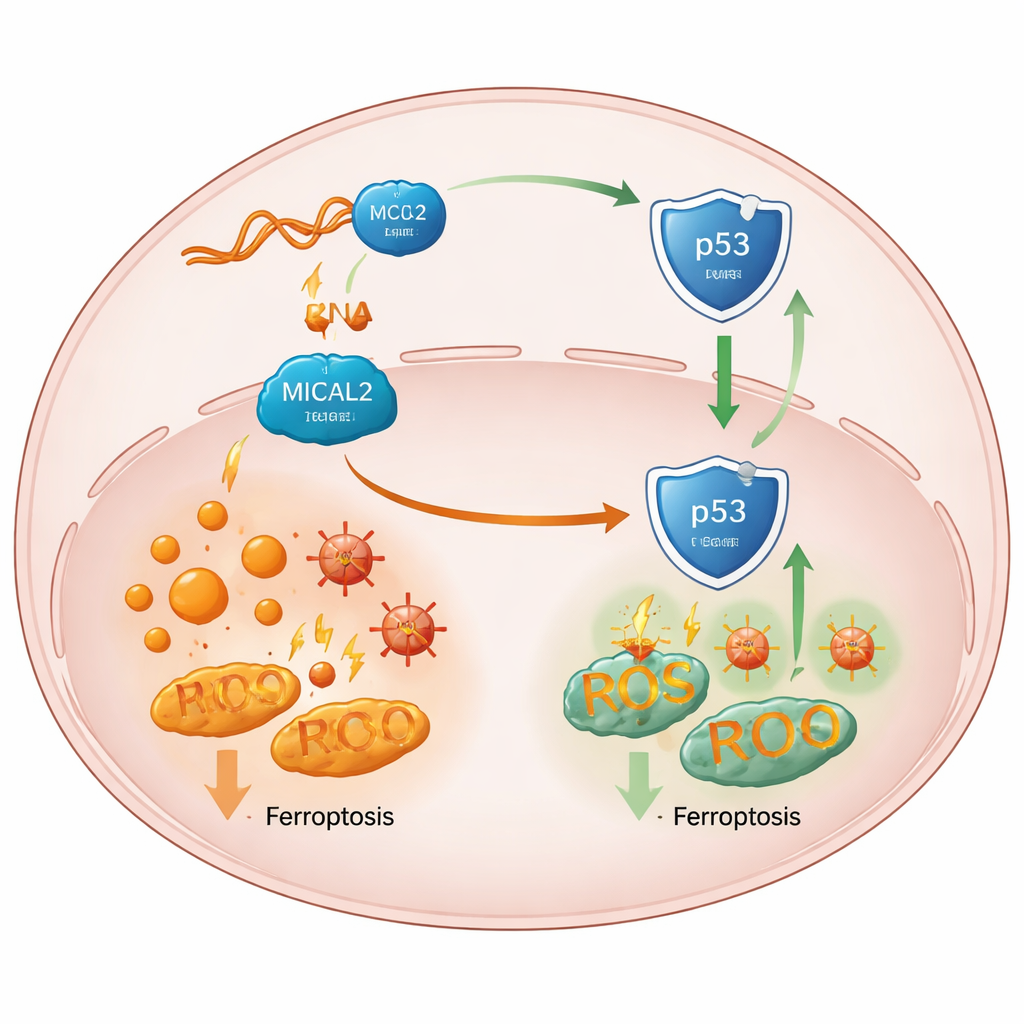
Cómo el escudo debilita a un guardián clave del tumor
Indagando más, el equipo vinculó el efecto de MICAL2 con p53, una proteína central «guardiana» que normalmente ayuda a prevenir tumores y puede favorecer la ferroptosis en células bajo estrés. La alta actividad de MICAL2 atenuó la vía de p53, mientras que la pérdida de MICAL2 estabilizó e incrementó la proteína p53 sin cambiar la actividad de su gen. Los investigadores mostraron que MICAL2 se asocia físicamente con p53 y con MDM2, una proteína que marca a p53 para su destrucción. MICAL2 ayuda a MDM2 a añadir más de estas marcas, enviando a p53 al sistema de reciclaje celular y expulsándolo del núcleo, donde de otro modo activaría genes protectores. Cuando se redujo MICAL2 o LINC-AC092535.5, p53 se acumuló en el núcleo, sus señales descendentes se inclinaron hacia la ferroptosis y las células cancerosas de varios tipos tumorales mostraron más muerte inducida por hierro—a menos que se eliminara el propio p53.
Qué significa esto para tratamientos futuros
En conjunto, el trabajo describe un nuevo eje de control en el carcinoma nasofaríngeo: el ARN LINC-AC092535.5 potencia a MICAL2, y MICAL2 a su vez ayuda a eliminar la influencia protectora de p53, permitiendo que las células tumorales resistan la ferroptosis. Interrumpir este eje—inhibiendo el ARN, bloqueando MICAL2 o impidiendo la degradación de p53—podría restaurar la muerte celular inducida por hierro y hacer que los fármacos inductores de ferroptosis existentes sean más eficaces. Para los pacientes con carcinoma nasofaríngeo en recaída o resistente al tratamiento, tales combinaciones podrían algún día ofrecer una forma de volver la propia carga de hierro y el estrés oxidativo del cáncer en su contra.
Cita: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Palabras clave: carcinoma nasofaríngeo, ferroptosis, p53, ARN largo no codificante, MICAL2