Clear Sky Science · it
LINC-AC092535.5 regola il livello di mRNA di MICAL2 per inibire la ferroptosi mediata da p53 nel carcinoma nasofaringeo
Perché questo studio è importante
Il carcinoma nasofaringeo è un tumore che insorge dietro il naso e sopra la gola e resta difficile da curare quando recidiva o si diffonde. Questo studio mette in luce un «freno» molecolare nascosto che aiuta queste cellule tumorali a sfuggire a una forma di morte cellulare recentemente riconosciuta, la ferroptosi, che dipende dal ferro e dal danno ossidativo. Smontando questo freno, i ricercatori indicano nuove strategie per rendere i tumori nasofaringei ostinati più vulnerabili al trattamento.
Un modo diverso in cui le cellule tumorali possono morire
La maggior parte dei farmaci antitumorali cerca di uccidere le cellule tumorali attivando programmi di morte noti, come l’apoptosi. I tumori, tuttavia, spesso imparano a eludere queste vie. La ferroptosi è un tipo distinto di morte cellulare guidata dal ferro e da esplosioni di molecole reattive dell’ossigeno che distruggono le membrane cellulari, in particolare nei mitocondri, le centrali energetiche della cellula. Molti tumori che resistono alle terapie standard possono comunque essere spinti verso la ferroptosi. Le cellule del carcinoma nasofaringeo sono particolarmente sensibili ai farmaci che innescano questo processo, il che suggerisce che la ferroptosi potrebbe essere sfruttata terapeuticamente—se i ricercatori capiscono cosa la ostacola.
Una proteina che protegge i tumori dai danni indotti dal ferro
Analizzando ampie banche dati genetiche e campioni tumorali di pazienti, il gruppo si è concentrato su una proteina chiamata MICAL2, in passato collegata alla crescita tumorale e alla chimica ossidativa. Hanno rilevato che i livelli di MICAL2 sono nettamente più alti nei tumori nasofaringei rispetto ai tessuti normali, e i pazienti con più MICAL2 tendono ad avere malattia più avanzata, più metastasi e una sopravvivenza peggiore. Quando i ricercatori hanno ridotto i livelli di MICAL2 in linee cellulari di carcinoma nasofaringeo, le cellule proliferavano e migravano meno e divennero molto più sensibili ai farmaci che inducono la ferroptosi, come Erastin e Sorafenib. Indicatori di ferro, stress ossidativo ed equilibrio antiossidante mutarono in modo coerente con un aumento della ferroptosi, sia in colture cellulari sia in modelli tumorali murini.
Un RNA di recente scoperta che aumenta la protezione
Gli investigatori si sono poi chiesti perché MICAL2 sia così abbondante in questi tumori. Hanno identificato un RNA non codificante lungo finora non caratterizzato, denominato LINC-AC092535.5, fortemente elevato nei tumori della testa e del collo e parallelo ai livelli di MICAL2. A differenza degli RNA che codificano proteine, questo RNA agisce come regolatore. Si lega fisicamente alla molecola messaggera di MICAL2 e ne accresce la produzione in due modi: potenzia l’attività del promotore del gene MICAL2 e rallenta la degradazione dell’mRNA di MICAL2. Quando LINC-AC092535.5 è stato silenziato, i livelli di MICAL2 sono diminuiti, i marcatori di ferroptosi sono aumentati e le cellule tumorali sono diventate più vulnerabili al danno ossidativo indotto dal ferro. Il ripristino di MICAL2 ha potuto in parte annullare questi effetti, dimostrando che questo RNA e MICAL2 funzionano insieme come un circuito di rinforzo che protegge le cellule tumorali dalla ferroptosi.
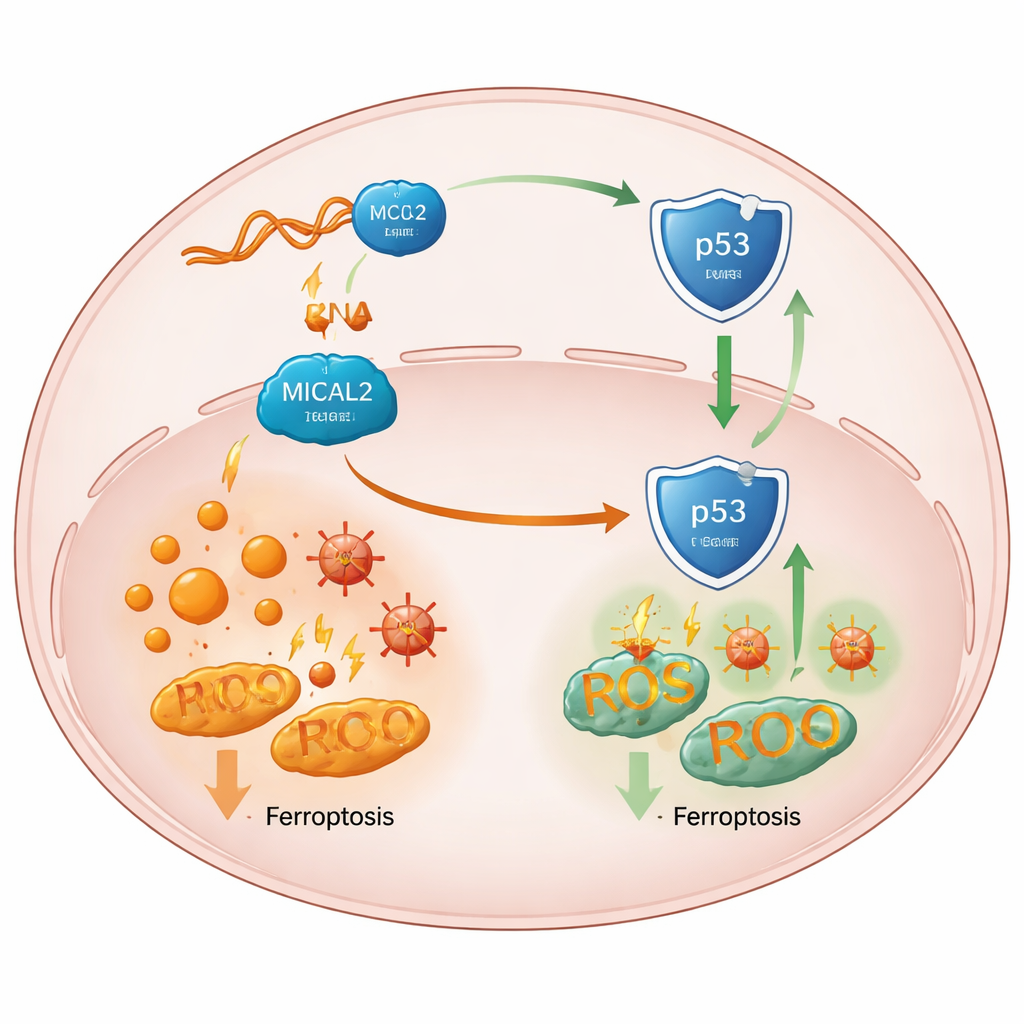
Come lo scudo indebolisce un importante guardiano tumorale
Approfondendo, il team ha ricondotto l’effetto di MICAL2 a p53, una proteina «guardiana» centrale che normalmente aiuta a prevenire i tumori e può favorire la ferroptosi nelle cellule sotto stress. Un’elevata attività di MICAL2 attenuava la via di p53, mentre la perdita di MICAL2 stabilizzava e aumentava la proteina p53 senza alterare l’attività del suo gene. I ricercatori hanno dimostrato che MICAL2 si associa fisicamente a p53 e a MDM2, una proteina che marca p53 per la distruzione. MICAL2 favorisce l’attacco di queste marcature da parte di MDM2, inviando p53 al sistema di smaltimento cellulare e allontanandolo dal nucleo, dove altrimenti attiverebbe geni protettivi. Quando MICAL2 o LINC-AC092535.5 venivano soppressi, p53 si accumulava nel nucleo, i suoi segnali a valle si spostavano verso la ferroptosi e le cellule tumorali di diversi tipi mostravano maggior morte indotta dal ferro—a meno che p53 stesso non fosse rimosso.
Cosa significa per i trattamenti futuri
Nel complesso, il lavoro delinea un nuovo asse di controllo nel carcinoma nasofaringeo: l’RNA LINC-AC092535.5 promuove MICAL2, e MICAL2 a sua volta contribuisce a eliminare l’influenza protettiva di p53, permettendo alle cellule tumorali di resistere alla ferroptosi. Interrompere questo asse—inibendo l’RNA, bloccando MICAL2 o impedendo la degradazione di p53—potrebbe ripristinare la morte cellulare indotta dal ferro e rendere più efficaci gli agenti che inducono la ferroptosi già esistenti. Per i pazienti con carcinoma nasofaringeo recidivante o resistente ai trattamenti, tali combinazioni potrebbero un giorno offrire un modo per rivolgere contro il tumore il suo stesso ferro e lo stress ossidativo.
Citazione: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Parole chiave: carcinoma nasofaringeo, ferroptosi, p53, RNA non codificante lungo, MICAL2