Clear Sky Science · pl
LINC-AC092535.5 reguluje poziom mRNA MICAL2, hamując ferroptozę zależną od p53 w raku nosogardzieli
Dlaczego to badanie ma znaczenie
Rak nosogardzieli powstaje za nosem i powyżej gardła i pozostaje trudny do wyleczenia po nawrocie lub rozsiewie. Badanie to ujawnia ukrytą molekularną „hamulec”, który pomaga komórkom nowotworowym unikać nowo rozpoznanego rodzaju śmierci komórkowej zwanego ferroptozą — zależnej od żelaza i uszkodzeń oksydacyjnych. Obnażając ten mechanizm, badacze wskazują nowe strategie, dzięki którym oporne guzy nosogardzieli mogą stać się bardziej podatne na terapię.
Inny sposób, w jaki komórki raka mogą ginąć
Większość leków przeciwnowotworowych próbuje zabić komórki guza, wywołując znane programy śmierci, takie jak apoptoza. Guzy jednak często uczą się unikać tych dróg. Ferroptoza to odrębny typ śmierci komórkowej napędzany przez żelazo i nagłe wybuchy reaktywnych cząsteczek tlenu, które niszczą błony komórkowe, szczególnie w mitochondriach — elektrowniach komórki. Wiele nowotworów opornych na standardowe terapie można jednak sprowokować do ferroptozy. Komórki raka nosogardzieli są szczególnie wrażliwe na leki wywołujące ten proces, co sugeruje, że ferroptoza może zostać wykorzystana terapeutycznie — pod warunkiem, że naukowcy zrozumieją, co ją tłumi.
Białko, które chroni guzy przed uszkodzeniami wywołanymi przez żelazo
Przeszukując duże bazy genetyczne i próbki guzów od pacjentów, zespół skoncentrował się na białku o nazwie MICAL2, wcześniej powiązanym z rozwojem nowotworów i chemią oksydacyjną. Stwierdzili, że poziomy MICAL2 są wyraźnie wyższe w guzach nosogardzieli niż w tkance normalnej, a pacjenci z większą ilością MICAL2 mają zwykle bardziej zaawansowaną chorobę, więcej przerzutów i gorsze przeżycie. Po obniżeniu poziomu MICAL2 w liniach komórkowych raka nosogardzieli komórki rzadziej się namnażały i szerzyły, a także stały się znacznie bardziej wrażliwe na leki wywołujące ferroptozę, takie jak Erastyna i Sorafenib. Wskaźniki żelaza, stresu oksydacyjnego i równowagi antyoksydacyjnej zmieniały się w sposób zgodny z nasileniem ferroptozy, zarówno w hodowlach komórkowych, jak i w modelach guzów u myszy.
Nowo odkryte RNA, które wzmacnia tę osłonę
Naukowcy zapytali następnie, dlaczego MICAL2 jest tak obfity w tych guzach. Odkryli wcześniej nieopisane długie niekodujące RNA, nazwane LINC-AC092535.5, które jest silnie podwyższone w nowotworach głowy i szyi i idzie w parze z poziomami MICAL2. W przeciwieństwie do RNA kodujących białka, ten RNA działa jako regulator. Fizycznie wiąże się z cząsteczką mRNA MICAL2 i zwiększa jego produkcję na dwa sposoby: wzmacnia aktywność promotora genu MICAL2 i spowalnia rozpadowi mRNA MICAL2. Gdy LINC-AC092535.5 została wyciszona, poziomy MICAL2 spadły, markery ferroptozy wzrosły, a komórki nowotworowe stały się bardziej podatne na oksydacyjne uszkodzenia zależne od żelaza. Przywrócenie MICAL2 częściowo odwracało te efekty, pokazując, że to RNA i MICAL2 działają razem jako obwód wzmacniający, który chroni komórki nowotworowe przed ferroptozą.
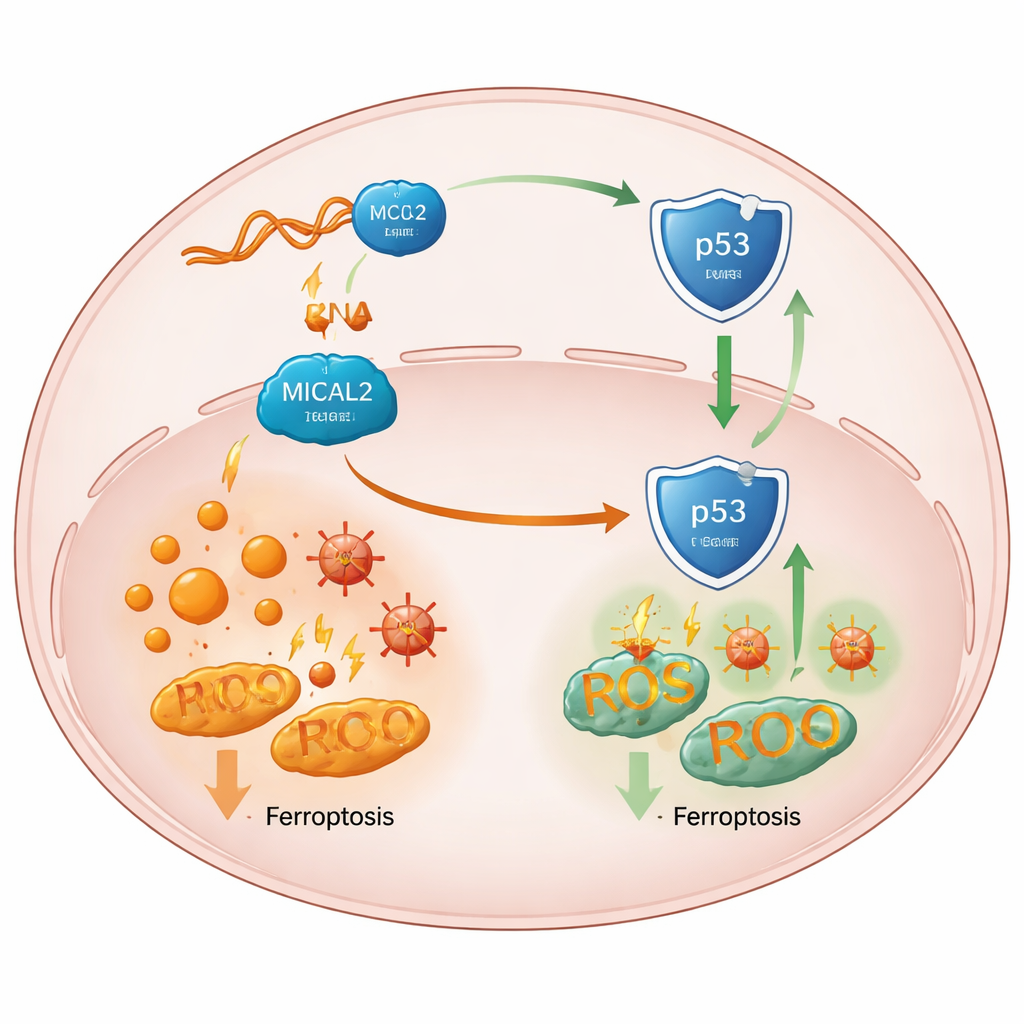
Jak osłona osłabia kluczowego strażnika guza
Wnikliwsze badania wykazały, że efekt MICAL2 odnosi się do p53, centralnego „strażnika” białkowego, który normalnie pomaga zapobiegać nowotworom i może promować ferroptozę w komórkach poddanych stresowi. Wysoka aktywność MICAL2 tłumiła szlak p53, podczas gdy utrata MICAL2 stabilizowała i zwiększała poziom białka p53 bez zmiany aktywności jego genu. Badacze pokazali, że MICAL2 fizycznie kojarzy się z p53 oraz z MDM2 — białkiem, które znakuję p53 do degradacji. MICAL2 pomaga MDM2 przyłączać więcej takich znaczników, kierując p53 do komórkowego systemu utylizacji i wypychając go z jądra komórkowego, gdzie normalnie włączałby geny ochronne. Gdy MICAL2 lub LINC-AC092535.5 były wyciszone, p53 gromadził się w jądrze, jego sygnały spustowe przesuwały się w stronę ferroptozy, a komórki nowotworowe różnych typów wykazywały więcej śmierci zależnej od żelaza — o ile tylko p53 nie został uprzednio usunięty.
Co to oznacza dla przyszłych terapii
Podsumowując, praca opisuje nową oś regulacyjną w raku nosogardzieli: RNA LINC-AC092535.5 zwiększa MICAL2, a MICAL2 z kolei pomaga pozbawić p53 jego ochronnego wpływu, pozwalając komórkom guza opierać się ferroptozie. Przerwanie tej osi — poprzez hamowanie RNA, blokowanie MICAL2 lub zapobieganie degradacji p53 — mogłoby przywrócić śmierć komórek wywoływaną przez żelazo i zwiększyć skuteczność istniejących leków indukujących ferroptozę. Dla pacjentów z nawrotowym lub opornym na leczenie rakiem nosogardzieli takie kombinacje mogą pewnego dnia pozwolić wykorzystać żelazo i stres oksydacyjny guza przeciwko niemu samemu.
Cytowanie: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Słowa kluczowe: rak nosogardzieli, ferroptoza, p53, długa niekodująca RNA, MICAL2