Clear Sky Science · nl
LINC-AC092535.5 reguleert het MICAL2-mRNA-niveau om p53-gemedieerde ferroptose bij nasofaryngeaal carcinoom te remmen
Waarom deze studie belangrijk is
Nasofaryngeaal carcinoom is een kanker die ontstaat achter de neus en boven de keel en blijft moeilijk te genezen zodra ze terugkeert of uitzaait. Deze studie onthult een verborgen moleculaire "rem" die tumorcellen helpt een recent beschreven vorm van celdood, ferroptose, te omzeilen; ferroptose is afhankelijk van ijzer en oxidatieve schade. Door deze rem bloot te leggen, wijzen de onderzoekers op nieuwe strategieën om hardnekkige nasofaryngeale tumoren gevoeliger te maken voor behandeling.
Een andere manier waarop kankercellen kunnen sterven
De meeste kankermedicijnen proberen tumorcellen te doden door gangbare doodsprogramma’s zoals apoptose te activeren. Tumoren leren echter vaak deze routes te ontwijken. Ferroptose is een aparte vorm van celdood, aangedreven door ijzer en plotselinge uitbarstingen van reactieve zuurstofmoleculen die celmembranen, met name in mitochondriën, vernietigen. Veel kanker die resistent is tegen standaardtherapieën kan nog wel gedwongen worden tot ferroptose. Nasofaryngeale kankercellen zijn bijzonder gevoelig voor middelen die dit proces opwekken, wat suggereert dat ferroptose therapeutisch benut kan worden—als onderzoekers begrijpen wat het belemmert.
Een eiwit dat tumoren beschermt tegen ijzer-gedreven schade
Door grote genetische databanken en tumormonsters van patiënten te doorzoeken, focuste het team op een eiwit genaamd MICAL2, eerder in verband gebracht met kankergroei en oxidatieve chemie. Ze vonden dat MICAL2-niveaus duidelijk hoger zijn in nasofaryngeale tumoren dan in normaal weefsel, en patiënten met meer MICAL2 neigen naar gevorderdere ziekte, meer metastasen en slechtere overleving. Wanneer de onderzoekers MICAL2-niveaus verlaagden in nasofaryngeale kankecelijnen, groeiden en verspreidden de cellen zich minder gemakkelijk en werden ze veel gevoeliger voor ferroptose-inducerende middelen zoals Erastin en Sorafenib. Metingen van ijzer, oxidatieve stress en antioxidantbalans verschooften op een manier die overeenkomt met verhoogde ferroptose, zowel in gekweekte cellen als in muismodellen met tumoren.
Een nieuw ontdekt RNA dat het schild versterkt
De onderzoekers vroegen zich vervolgens af waarom MICAL2 in deze tumoren zo veel voorkomt. Ze ontdekten een eerder ongekarakteriseerde lange niet-coderende RNA, genoemd LINC-AC092535.5, dat sterk verhoogd is in hoofd- en halskankers en parallel loopt met MICAL2-niveaus. In tegenstelling tot RNA’s die eiwitten coderen, werkt dit RNA als regulator. Het bindt fysiek aan het boodschappermolecuul van MICAL2 en verhoogt de productie op twee manieren: het versterkt de activiteit van de promoter van het MICAL2-gen en vertraagt de afbraak van MICAL2-messenger-RNA. Wanneer LINC-AC092535.5 werd stilgelegd, daalden MICAL2-niveaus, namen markers van ferroptose toe en werden tumorcellen kwetsbaarder voor ijzer-gedreven oxidatieve schade. Het herstel van MICAL2 kon deze effecten gedeeltelijk ongedaan maken, wat laat zien dat dit RNA en MICAL2 samen functioneren als een versterkend circuit dat kankercellen tegen ferroptose beschermt.
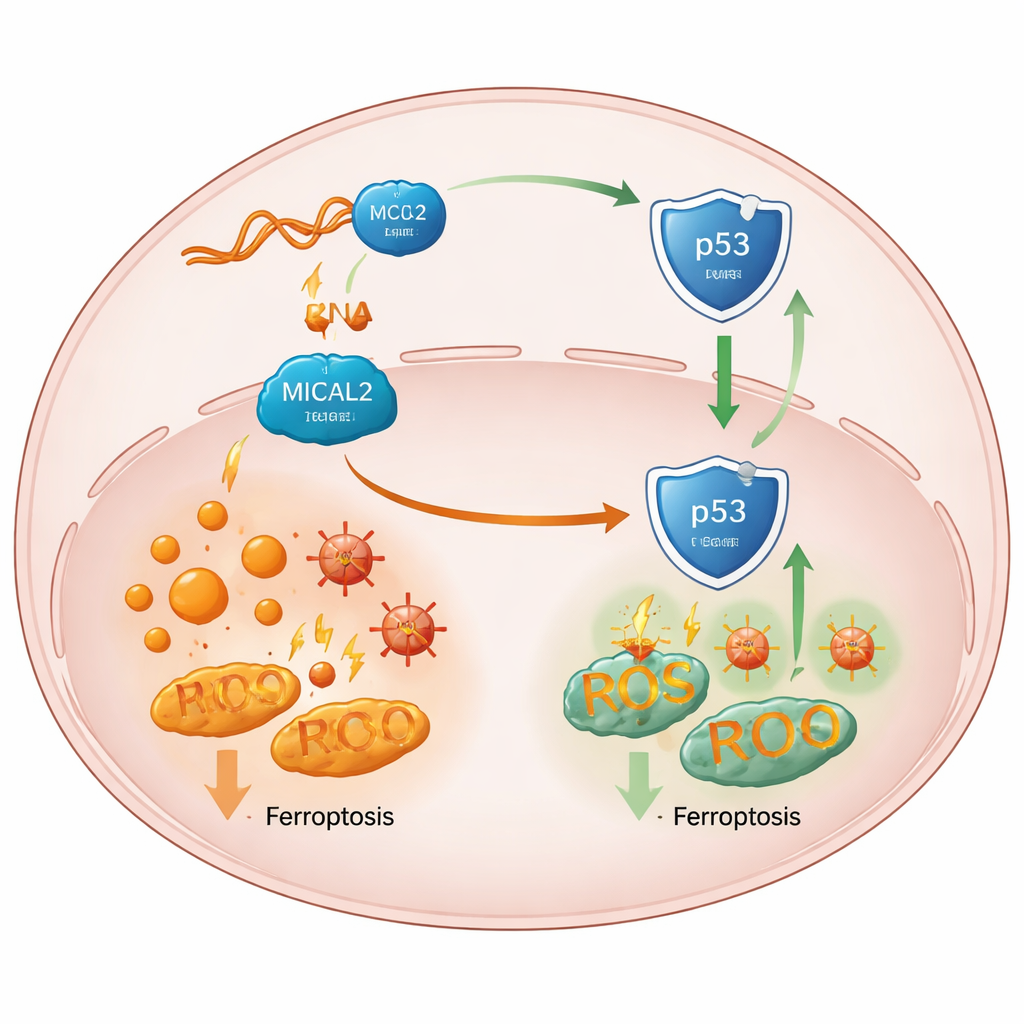
Hoe het schild een belangrijke tumorbeschermer verzwakt
Dieper gravend traceerde het team het effect van MICAL2 naar p53, een centraal "bewaker"-eiwit dat normaal tumoren helpt te voorkomen en onder stress ferroptose kan bevorderen. Hoge MICAL2-activiteit dempte het p53-pad, terwijl verlies van MICAL2 het p53-eiwit stabiliseerde en deed toenemen zonder de genactiviteit ervan te veranderen. De onderzoekers toonden aan dat MICAL2 fysiek geassocieerd is met p53 en met MDM2, een eiwit dat p53 markeert voor afbraak. MICAL2 helpt MDM2 meer van deze labels te bevestigen, waardoor p53 naar het cellulaire afvalverwerkingssysteem wordt gestuurd en uit de kern wordt verdreven, waar het anders beschermende genen zou activeren. Wanneer MICAL2 of LINC-AC092535.5 werden onderdrukt, stapelde p53 zich op in de kern, verschoof de signaalvoering richting ferroptose en toonden kankercellen uit verschillende tumortypes meer ijzer-gedreven celdood—tenzij p53 zelf werd verwijderd.
Wat dit betekent voor toekomstige behandelingen
Gezamenlijk schetst het werk een nieuwe regelas in nasofaryngeaal carcinoom: het RNA LINC-AC092535.5 verhoogt MICAL2, en MICAL2 helpt op zijn beurt de beschermende invloed van p53 weg te nemen, waardoor tumorcellen weerstand tegen ferroptose krijgen. Het onderbreken van deze as—door het RNA te remmen, MICAL2 te blokkeren of afbraak van p53 te voorkomen—zou ijzer-gedreven celdood kunnen herstellen en bestaande ferroptose-inducerende middelen effectiever kunnen maken. Voor patiënten met teruggekeerde of therapieresistente nasofaryngeale kanker kunnen dergelijke combinaties mogelijk een manier bieden om het eigen ijzer en oxidatieve stress van de tumor tegen de tumor te keren.
Bronvermelding: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Trefwoorden: nasofaryngeaal carcinoom, ferroptose, p53, lange niet-coderende RNA, MICAL2