Clear Sky Science · pt
LINC-AC092535.5 regula o nível de mRNA de MICAL2 para inibir a ferroptose mediada por p53 no carcinoma nasofaríngeo
Por que este estudo é importante
O carcinoma nasofaríngeo é um câncer que surge atrás do nariz e acima da garganta, e continua difícil de curar quando recorre ou se espalha. Este estudo revela um “freio” molecular oculto que ajuda essas células tumorais a escapar de uma forma de morte celular recentemente reconhecida chamada ferroptose, que depende de ferro e de danos oxidativos. Ao expor esse freio, os pesquisadores apontam para novas estratégias para tornar tumores nasofaríngeos resistentes mais vulneráveis ao tratamento.
Uma maneira diferente de as células cancerosas morrerem
A maioria dos medicamentos contra o câncer tenta matar células tumorais desencadeando programas de morte bem conhecidos, como apoptose. No entanto, os tumores frequentemente aprendem a evitar essas rotas. A ferroptose é um tipo distinto de morte celular impulsionado pelo ferro e por explosões de moléculas reativas de oxigênio que destroem membranas celulares, particularmente nas mitocôndrias, as usinas de energia da célula. Muitos cânceres que resistem às terapias padrão ainda podem ser levados à ferroptose. Células do carcinoma nasofaríngeo são particularmente sensíveis a drogas que desencadeiam esse processo, o que sugere que a ferroptose poderia ser aproveitada terapeuticamente — se os cientistas conseguirem entender o que a reprime.
Uma proteína que protege tumores do dano induzido por ferro
Ao vasculhar grandes bancos de dados genéticos e amostras tumorais de pacientes, a equipe concentrou-se em uma proteína chamada MICAL2, anteriormente associada ao crescimento do câncer e à química oxidativa. Eles descobriram que os níveis de MICAL2 são marcadamente mais altos em tumores nasofaríngeos do que em tecido normal, e pacientes com mais MICAL2 tendem a ter doença mais avançada, mais metástases e pior sobrevida. Quando os pesquisadores reduziram os níveis de MICAL2 em linhagens celulares de carcinoma nasofaríngeo, as células cresceram e se espalharam menos prontamente, e tornaram-se muito mais sensíveis a drogas que induzem ferroptose, como Erastina e Sorafenibe. Medidas de ferro, estresse oxidativo e equilíbrio antioxidante mudaram de forma consistente com aumento da ferroptose, tanto em células cultivadas quanto em modelos tumorais em camundongos.
Um RNA recém-descoberto que aumenta essa proteção
Os investigadores então perguntaram por que MICAL2 é tão abundante nesses tumores. Eles descobriram um RNA longo não codificante, previamente não caracterizado, chamado LINC-AC092535.5, que está fortemente elevado em cânceres de cabeça e pescoço e acompanha os níveis de MICAL2. Ao contrário de RNAs que codificam proteínas, esse RNA atua como regulador. Ele se liga fisicamente à molécula mensageira de MICAL2 e aumenta sua produção de duas maneiras: potencializa a atividade do promotor do gene MICAL2 e retarda a degradação do RNA mensageiro de MICAL2. Quando LINC-AC092535.5 foi silenciado, os níveis de MICAL2 caíram, os marcadores de ferroptose aumentaram e as células tumorais ficaram mais vulneráveis ao dano oxidativo induzido por ferro. Restaurar MICAL2 pôde desfazer parcialmente esses efeitos, mostrando que esse RNA e MICAL2 funcionam juntos como um circuito de reforço que protege as células cancerosas da ferroptose.
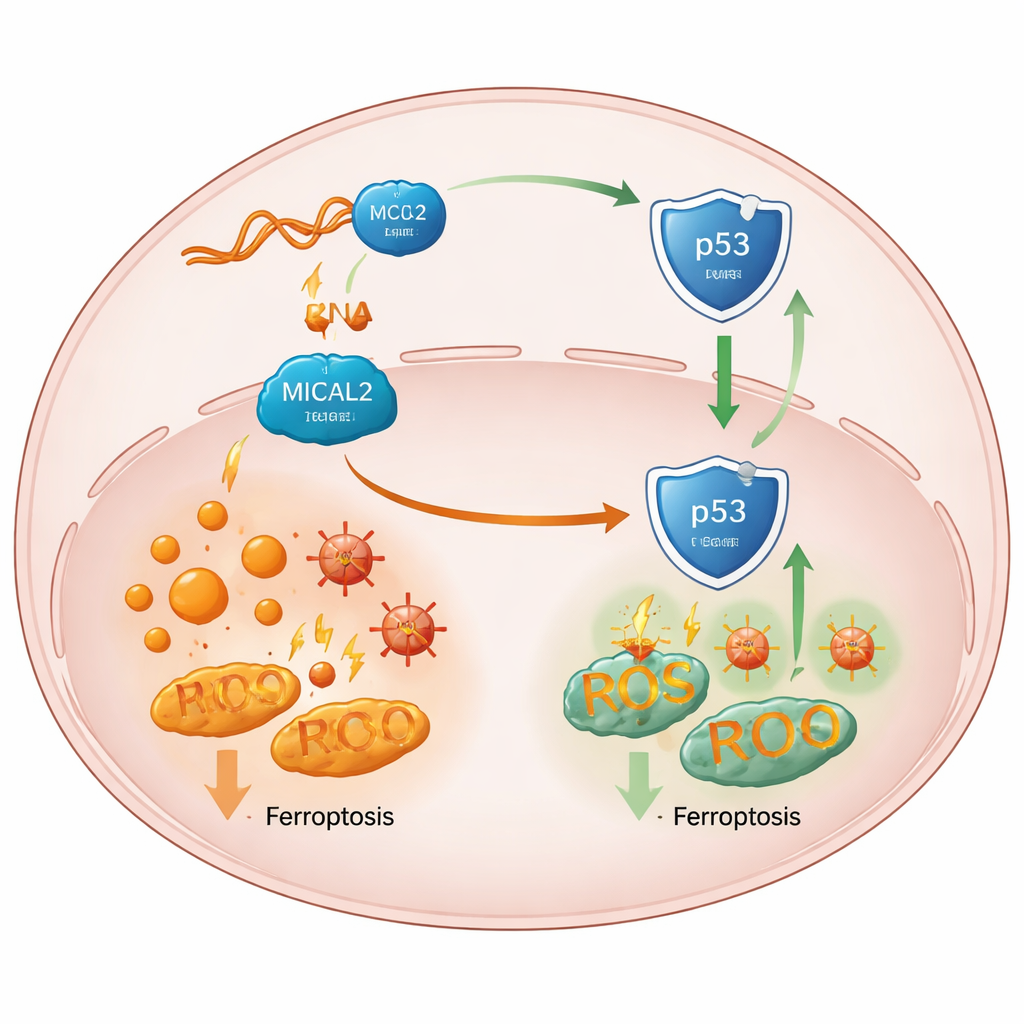
Como a proteção enfraquece um guardião tumoral chave
Aprofundando, a equipe rastreou o efeito de MICAL2 até p53, uma proteína “guardião” central que normalmente ajuda a prevenir tumores e pode promover a ferroptose em células estressadas. Alta atividade de MICAL2 atenuou a via de p53, enquanto a perda de MICAL2 estabilizou e aumentou a proteína p53 sem alterar a atividade do seu gene. Os pesquisadores mostraram que MICAL2 se associa fisicamente a p53 e a MDM2, uma proteína que marca p53 para destruição. MICAL2 ajuda a MDM2 a anexar mais dessas marcações, enviando p53 para o sistema de degradação celular e deslocando-o para fora do núcleo, onde normalmente ativaria genes protetores. Quando MICAL2 ou LINC-AC092535.5 foram reduzidos, p53 se acumulou no núcleo, seus sinais a jusante migraram em direção à ferroptose, e células tumorais de vários tipos mostraram mais morte induzida por ferro — a menos que o próprio p53 fosse removido.
O que isso significa para tratamentos futuros
Em conjunto, o trabalho descreve um novo eixo de controle no carcinoma nasofaríngeo: o RNA LINC-AC092535.5 aumenta MICAL2, e MICAL2 por sua vez ajuda a retirar a influência protetora de p53, permitindo que as células tumorais resistam à ferroptose. Interromper esse eixo — inibindo o RNA, bloqueando MICAL2 ou evitando a degradação de p53 — poderia restaurar a morte celular induzida por ferro e tornar drogas existentes que promovem a ferroptose mais eficazes. Para pacientes com câncer nasofaríngeo recidivado ou resistente ao tratamento, tais combinações podem um dia oferecer uma forma de voltar o próprio ferro e estresse oxidativo do tumor contra ele.
Citação: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Palavras-chave: carcinoma nasofaríngeo, ferroptose, p53, RNA longo não codificante, MICAL2