Clear Sky Science · de
LINC-AC092535.5 reguliert das MICAL2-mRNA-Niveau, um p53-vermittelte Ferroptose beim Nasopharynxkarzinom zu hemmen
Warum diese Studie wichtig ist
Nasopharynxkarzinom ist eine Krebserkrankung, die hinter der Nase und oberhalb des Rachens entsteht und die nach Rückfall oder Metastasierung schwer zu behandeln bleibt. Diese Studie legt eine verborgene molekulare "Bremse" offen, die den Tumorzellen hilft, einer neu erkannten Form des Zelltods namens Ferroptose zu entkommen, die auf Eisen und oxidative Schäden beruht. Indem die Forschenden diese Bremse aufdecken, weisen sie auf neue Strategien hin, um hartnäckige nasopharyngeale Tumoren wieder empfindlicher für Therapien zu machen.
Ein anderer Weg, wie Krebszellen sterben können
Die meisten Krebsmedikamente versuchen, Tumorzellen durch Aktivierung bekannter Todesprogramme wie Apoptose zu beseitigen. Tumoren lernen jedoch oft, solche Wege zu umgehen. Ferroptose ist eine eigenständige Form des Zelltods, die durch Eisen und Schübe reaktiver Sauerstoffmoleküle ausgelöst wird und Zellmembranen zerstört, insbesondere in den Mitochondrien, den Kraftwerken der Zelle. Viele Krebsarten, die gegenüber Standardtherapien resistent sind, lassen sich dennoch in die Ferroptose treiben. Nasopharynxkarzinomzellen sind besonders empfindlich gegenüber Wirkstoffen, die diesen Prozess auslösen, was nahelegt, dass Ferroptose therapeutisch genutzt werden könnte — falls Forschende verstehen, was sie hemmt.
Ein Protein, das Tumoren vor eisengetriebenen Schäden schützt
Bei der Durchsuchung großer genetischer Datenbanken und von Tumorproben aus Patientinnen und Patienten konzentrierte sich das Team auf ein Protein namens MICAL2, das zuvor mit Tumorwachstum und oxidativer Chemie in Verbindung gebracht worden war. Sie stellten fest, dass die MICAL2-Spiegel in nasopharyngealen Tumoren deutlich höher sind als im Normalgewebe, und Patientinnen und Patienten mit mehr MICAL2 tendenziell weiter fortgeschrittene Erkrankungen, mehr Metastasen und eine schlechtere Überlebensrate haben. Wenn die Forschenden MICAL2 in nasopharyngealen Krebszelllinien reduzierten, wuchsen und breiteten sich die Zellen weniger leicht aus, und sie wurden deutlich empfindlicher gegenüber Ferroptose-induzierenden Wirkstoffen wie Erastin und Sorafenib. Messwerte für Eisen, oxidativen Stress und antioxidative Balance verschoben sich in eine Richtung, die zu erhöhter Ferroptose passt, sowohl in kultivierten Zellen als auch in Maus-Tumormodellen.
Eine neu entdeckte RNA, die den Schutz verstärkt
Die Forschenden fragten dann, warum MICAL2 in diesen Tumoren so reichlich vorhanden ist. Sie entdeckten eine bisher uncharakterisierte lange nicht-kodierende RNA mit dem Namen LINC-AC092535.5, die in Kopf- und Halstumoren stark erhöht ist und parallel zu den MICAL2-Spiegeln verläuft. Im Gegensatz zu RNAs, die Proteine kodieren, wirkt diese RNA als Regulator. Sie bindet physisch an die MICAL2-Botschafts-RNA und steigert deren Produktion auf zwei Wegen: Sie erhöht die Aktivität des Promotors des MICAL2-Gens und verlangsamt den Abbau der MICAL2-mRNA. Wenn LINC-AC092535.5 stummgeschaltet wurde, sanken die MICAL2-Spiegel, Ferroptose-Marker stiegen, und Tumorzellen wurden anfälliger für eisengetriebene oxidative Schäden. Die Wiederherstellung von MICAL2 konnte diese Effekte teilweise rückgängig machen, was zeigt, dass diese RNA und MICAL2 zusammen als ein verstärkender Regelkreis wirken, der Krebszellen vor Ferroptose schützt.
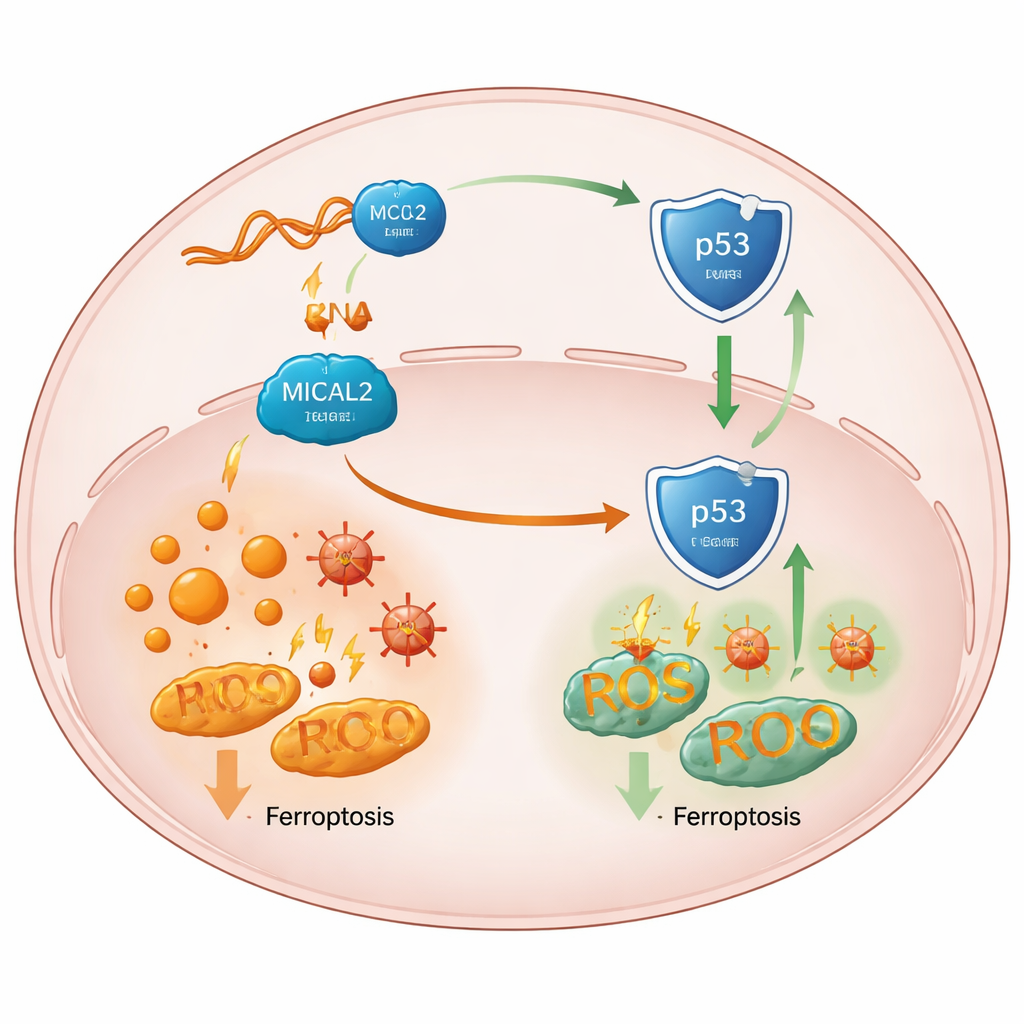
Wie der Schutz einen wichtigen Tumorwächter schwächt
Bei tiefergehenden Untersuchungen verfolgte das Team die Wirkung von MICAL2 bis zu p53, einem zentralen "Wächter"-Protein, das normalerweise Tumoren vorbeugt und in gestressten Zellen Ferroptose fördern kann. Hohe MICAL2-Aktivität dämpfte den p53-Signalweg, während der Verlust von MICAL2 das p53-Protein stabilisierte und erhöhte, ohne die Genaktivität von p53 zu verändern. Die Forschenden zeigten, dass MICAL2 physisch mit p53 und mit MDM2 assoziiert, einem Protein, das p53 für den Abbau markiert. MICAL2 erleichtert es MDM2, mehr dieser Markierungen anzubringen, wodurch p53 an das zelluläre Abbausystem geschickt und aus dem Zellkern transportiert wird, wo es sonst schützende Gene einschalten würde. Wenn MICAL2 oder LINC-AC092535.5 herunterreguliert wurden, akkumulierte p53 im Zellkern, seine nachgeschalteten Signale verschoben sich zugunsten der Ferroptose, und Krebszellen verschiedener Tumortypen zeigten vermehrt eisenabhängigen Tod — es sei denn, p53 selbst wurde entfernt.
Was das für künftige Behandlungen bedeutet
Insgesamt skizziert die Arbeit eine neue Kontrollachse beim Nasopharynxkarzinom: Die RNA LINC-AC092535.5 steigert MICAL2, und MICAL2 wiederum hilft, den schützenden Einfluss von p53 zu schwächen, wodurch Tumorzellen der Ferroptose widerstehen können. Die Unterbrechung dieser Achse — durch Hemmung der RNA, Blockade von MICAL2 oder Verhinderung des p53-Abbaus — könnte den eisengetriebenen Zelltod wiederherstellen und bestehende Ferroptose-induzierende Medikamente wirksamer machen. Für Patientinnen und Patienten mit rezidivierendem oder therapieresistentem Nasopharynxkarzinom könnten solche Kombinationen eines Tages ermöglichen, den körpereigenen Eisen- und oxidativen Stress gegen den Tumor auszuspielen.
Zitation: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Schlüsselwörter: Nasopharynxkarzinom, Ferroptose, p53, lange nicht-kodierende RNA, MICAL2