Clear Sky Science · sv
LINC-AC092535.5 reglerar MICAL2-mRNA-nivåer för att hämma p53-medierad ferroptos i nasofaryngeal karcinom
Varför denna studie är viktig
Nasofaryngealt karcinom är en cancer som uppstår bakom näsan och ovanför halsen och är svår att bota när den återkommer eller sprider sig. Denna studie avslöjar en dold molekylär "broms" som hjälper tumörceller att undvika en nyligen identifierad form av celldöd kallad ferroptos, vilken är beroende av järn och oxidativ skada. Genom att exponera denna broms pekar forskarna på nya strategier för att göra svårbehandlade nasofaryngeala tumörer mer sårbara för behandling.
Ett annat sätt för cancerceller att dö
De flesta cancerläkemedel försöker döda tumörceller genom att utlösa välkända dödsprogram som apoptos. Tumörer lär sig dock ofta att undvika dessa vägar. Ferroptos är en distinkt typ av celldöd driven av järn och utbrott av reaktiva syremolekyler som förstör cellmembran, särskilt i mitokondrierna, cellens kraftverk. Många cancerformer som är resistenta mot standardbehandlingar kan ändå pressas in i ferroptos. Nasofaryngeala karcinomceller är särskilt känsliga för läkemedel som utlöser denna process, vilket tyder på att ferroptos skulle kunna bli ett terapeutiskt fördelaktigt verktyg—om forskare kan förstå vad som håller tillbaka processen.
Ett protein som skyddar tumörer från järndriven skada
Genom att söka i stora genetiska databaser och tumörprover från patienter fokuserade teamet på ett protein kallat MICAL2, tidigare kopplat till cancertillväxt och oxidativ kemi. De fann att MICAL2-nivåerna är avsevärt högre i nasofaryngeala tumörer än i normal vävnad, och patienter med mer MICAL2 tenderar att ha mer avancerad sjukdom, fler metastaser och sämre överlevnad. När forskarna minskade MICAL2-nivåerna i nasofaryngeala cancercellinjer växte och spreds cellerna mindre lätt, och de blev mycket mer känsliga för ferroptos-inducerande läkemedel som Erastin och Sorafenib. Mått på järn, oxidativ stress och antioxidantbalans förändrades på ett sätt som överensstämmer med ökad ferroptos, både i odlade celler och i musmodeller för tumörväxt.
Ett nyligen upptäckt RNA som förstärker skyddet
Forskarna undrade sedan varför MICAL2 är så rikligt förekommande i dessa tumörer. De upptäckte ett tidigare okarakteriserat långt icke-kodande RNA, kallat LINC-AC092535.5, som är starkt uppreglerat i huvud- och halscancer och speglar MICAL2-nivåerna. Till skillnad från RNA som kodar för proteiner fungerar detta RNA som en regulator. Det binder fysiskt till MICAL2:s budbärarmolekyl och ökar dess produktion på två sätt: det förstärker aktiviteten i MICAL2-genens promotor och det bromsar nedbrytningen av MICAL2-messenger-RNA. När LINC-AC092535.5 tystades, sjönk MICAL2-nivåerna, ferroptosmarkörer ökade och tumörceller blev mer sårbara för järndriven oxidativ skada. Återställande av MICAL2 kunde delvis återställa dessa effekter, vilket visar att detta RNA och MICAL2 fungerar tillsammans i ett förstärkande kretslopp som skyddar cancerceller från ferroptos.
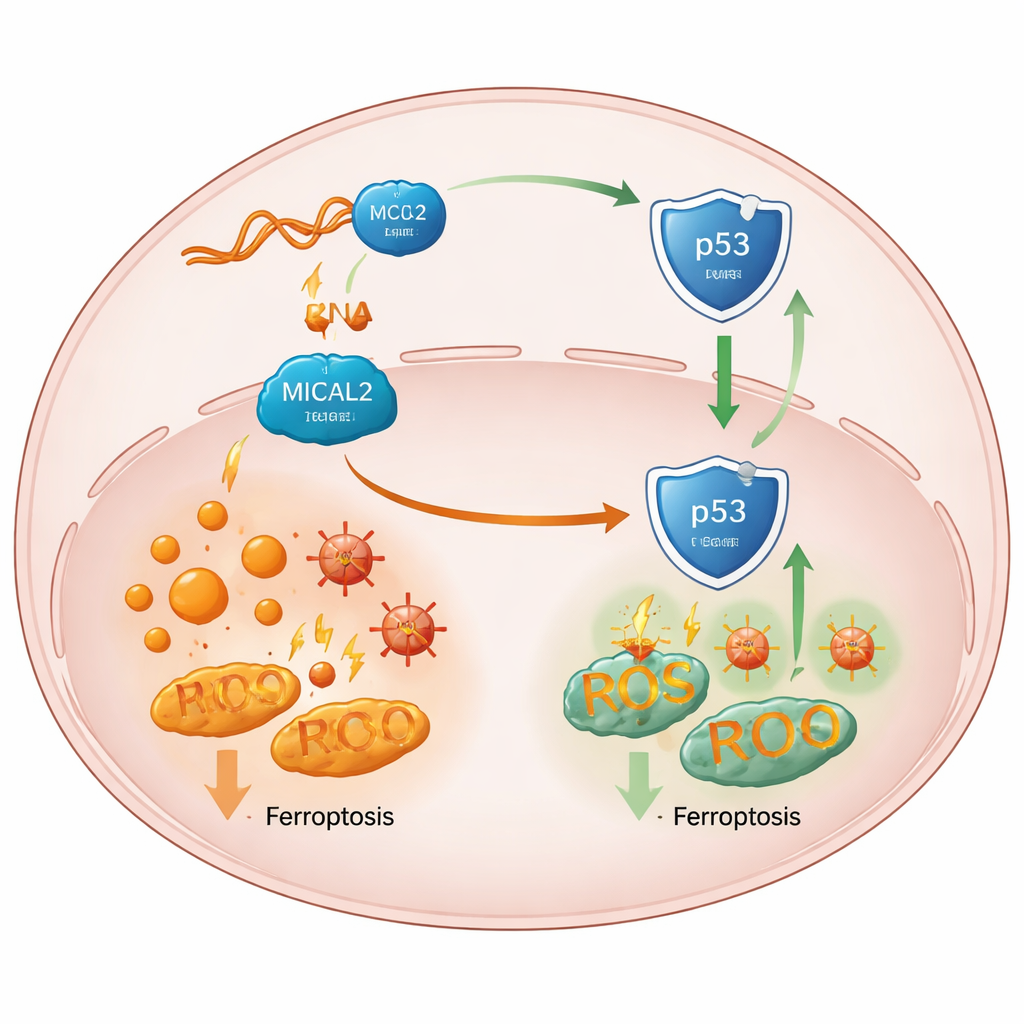
Hur skyddet försvagar en viktig tumörvakt
Vid en närmare genomgång spårade teamet MICAL2:s effekt till p53, ett centralt "vakt"-protein som normalt hjälper till att förebygga tumörer och kan främja ferroptos i stressade celler. Hög MICAL2-aktivitet dämpade p53:s väg, medan förlust av MICAL2 stabiliserade och ökade p53-proteinet utan att förändra genens aktivitet. Forskarna visade att MICAL2 fysiskt associerar med p53 och med MDM2, ett protein som märker p53 för nedbrytning. MICAL2 hjälper MDM2 att fästa fler sådana märken, vilket skickar p53 till cellens avfallssystem och transporterar det ut ur kärnan, där det annars skulle aktivera skyddande gener. När MICAL2 eller LINC-AC092535.5 slogs ner, ackumulerades p53 i kärnan, dess signaler försköts mot ferroptos, och cancerceller över flera tumörtyper visade mer järndriven död—om inte p53 självt togs bort.
Vad detta betyder för framtida behandlingar
Sammantaget beskriver arbetet en ny kontrollaxel i nasofaryngealt karcinom: RNA:t LINC-AC092535.5 ökar MICAL2, och MICAL2 hjälper i sin tur till att avlägsna p53:s skyddande inflytande, vilket tillåter tumörceller att motstå ferroptos. Att bryta denna axel—genom att hämma RNA:t, blockera MICAL2 eller förhindra p53-nedbrytning—kan återställa järndriven celldöd och göra befintliga ferroptos-inducerande läkemedel mer effektiva. För patienter med återfall eller behandlingsresistent nasofaryngeal cancer kan sådana kombinationer en dag erbjuda ett sätt att vända cancerens eget järn och oxidativa stress mot den.
Citering: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Nyckelord: nasofaryngealt karcinom, ferroptos, p53, lång icke-kodande RNA, MICAL2