Clear Sky Science · tr
LINC-AC092535.5, MICAL2 mRNA düzeyini düzenleyerek nazofaringeal karsinomda p53 aracılı ferroptozisi engeller
Bu çalışma neden önemli
Nazofaringeal karsinom, burnun arkasında ve boğazın üstünde ortaya çıkan bir kanserdir ve nüks ettiğinde veya yayıldığında tedavisi hâlâ zordur. Bu çalışma, demir ve oksidatif hasara dayanan yeni tanımlanmış bir hücre ölümü biçimi olan ferroptozisi atlatmaya yardımcı olan gizli bir moleküler “fren”i ortaya koyuyor. Bu freni açığa çıkararak araştırmacılar, inatçı nazofaringeal tümörleri tedaviye karşı daha savunmasız hâle getirmeye yönelik yeni stratejilere işaret ediyor.
Tümör hücrelerinin ölmesinin farklı bir yolu
Çoğu kanser ilacı, tümör hücrelerini apoptoz gibi bilinen ölüm programlarını tetikleyerek yok etmeye çalışır. Ancak tümörler sıklıkla bu yolları atlatmayı öğrenir. Ferroptozis, özellikle mitokondriler dahil hücre zarlarını yok eden demir ve reaktif oksijen moleküllerindeki patlamalar tarafından yönlendirilen ayrı bir hücre ölümü türüdür. Standart tedavilere dirençli birçok kanser hâlâ ferroptozise yönlendirilebilir. Nazofaringeal karsinom hücreleri, bu süreci tetikleyen ilaçlara özellikle duyarlıdır; bu da, araştırmacılar neyin bunu engellediğini anlayabilirse, ferroptozisin terapötik bir avantaja dönüştürülebileceğini gösterir.
Tümörleri demir kaynaklı hasardan koruyan bir protein
Büyük genetik veri tabanları ve hastalardan alınan tümör örneklerini tarayan ekip, daha önce kanser büyümesi ve oksidatif kimya ile ilişkilendirilmiş MICAL2 adlı bir proteine odaklandı. MICAL2 düzeylerinin nazofaringeal tümörlerde normal dokuya göre belirgin şekilde yüksek olduğunu ve daha fazla MICAL2 olan hastaların genellikle daha ileri evre hastalığa, daha fazla metastaza ve daha kötü sağkalıma sahip olduğunu buldular. Araştırmacılar MICAL2 düzeylerini nazofaringeal kanser hücre hatlarında azalttıklarında, hücrelerin büyüme ve yayılma yeteneği azaldı ve Erastin ve Sorafenib gibi ferroptozis indükleyici ilaçlara çok daha duyarlı hale geldiler. Demir, oksidatif stres ve antioksidan dengesine ilişkin ölçümler, hem kültür hücrelerinde hem de fare tümör modellerinde artmış ferroptozise uygun şekilde değişti.
Koruyucuyu güçlendiren yeni keşfedilmiş bir RNA
Araştırmacılar neden MICAL2’nin bu tümörlerde bu kadar bol olduğunu merak ettiler. Baş ve boyun kanserlerinde güçlü şekilde yükselmiş ve MICAL2 düzeyleriyle paralellik gösteren daha önce tanımlanmamış bir uzun kodlamayan RNA olan LINC-AC092535.5’i keşfettiler. Protein kodlayan RNA’ların aksine bu RNA bir düzenleyici olarak işlev görüyor. MICAL2’nin bilgi taşıyıcısına fiziksel olarak bağlanıyor ve iki yolla üretimini artırıyor: MICAL2 geninin promotör aktivitesini yükseltiyor ve MICAL2 mesajcı RNA’sının yıkımını yavaşlatıyor. LINC-AC092535.5 susturulduğunda MICAL2 düzeyleri düştü, ferroptozis belirteçleri arttı ve tümör hücreleri demir kaynaklı oksidatif hasara karşı daha savunmasız hâle geldi. MICAL2’nin yeniden sağlanması bu etkileri kısmen geri çevirebildi; bu da bu RNA ile MICAL2’nin ferroptozisten koruyan güçlendirici bir devre olarak birlikte çalıştığını gösteriyor.
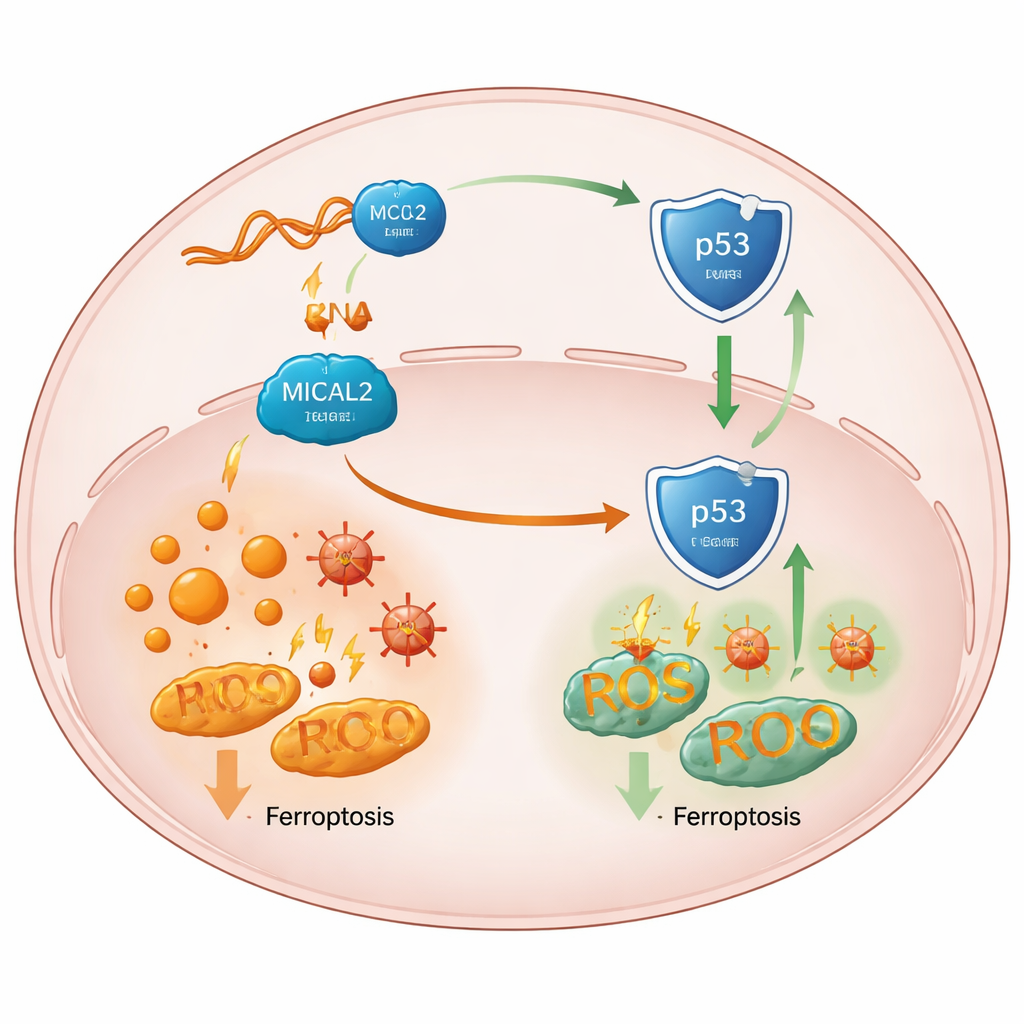
Kalkanın önemli bir tümör bekçisini nasıl zayıflattığı
Daha derine indiklerinde ekip, MICAL2’nin etkisini p53’e, normalde tümörleri önlemeye yardımcı olan ve stres altındaki hücrelerde ferroptozisi teşvik edebilen merkezi “bekçi” proteine kadar izledi. Yüksek MICAL2 aktivitesi p53 yolunu bastırırken, MICAL2 kaybı p53 proteininin stabilizasyonuna ve artışına yol açtı; gen aktivitesini değiştirmeden. Araştırmacılar MICAL2’nin p53 ve p53’ü yok etme etiketi koyan MDM2 proteini ile fiziksel ilişki içinde olduğunu gösterdiler. MICAL2, MDM2’nin bu etiketleri daha fazla takmasına yardımcı oluyor, p53’ü hücresel atık sistemine gönderiyor ve çekirdekten uzaklaştırıyor; aksi takdirde p53 koruyucu genleri aktive ederdi. MICAL2 veya LINC-AC092535.5 indirildiğinde p53 çekirdekte birikti, aşağı akış sinyalleri ferroptozise kaydı ve çeşitli tümör tiplerindeki kanser hücrelerinde demir kaynaklı ölüm arttı—p53 kendisi ortadan kaldırılmadığı sürece.
Gelecek tedaviler için ne anlama geliyor
Birlikte ele alındığında çalışma, nazofaringeal karsinomda yeni bir kontrol ekseni tanımlıyor: LINC-AC092535.5 RNA’sı MICAL2’yi artırıyor ve MICAL2 da p53’ün koruyucu etkisini ortadan kaldırarak tümör hücrelerinin ferroptozise direnmesine izin veriyor. Bu ekseni engellemek—RNA’yı hedefleyerek, MICAL2’yi bloke ederek veya p53 yıkımını önleyerek—demir kaynaklı hücre ölümünü yeniden sağlayabilir ve mevcut ferroptozis indükleyici ilaçları daha etkili kılabilir. Nüks etmiş veya tedaviye dirençli nazofaringeal kanseri olan hastalar için bu tür kombinasyonlar bir gün tümörün kendi demirini ve oksidatif stresini aleyhine çevirmeye yarayan bir yol sunabilir.
Atıf: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Anahtar kelimeler: nazofaringeal karsinom, ferroptozis, p53, uzun kodlamayan RNA, MICAL2