Clear Sky Science · ru
LINC-AC092535.5 регулирует уровень мРНК MICAL2, чтобы подавлять p53-опосредованный ферроптоз при назофарингеальной карциноме
Почему это исследование важно
Назофарингеальная карцинома — опухоль, возникающая позади носа и над горлом, и она остается трудной для лечения при рецидиве или метастазировании. В этом исследовании обнаружен скрытый молекулярный «тормоз», который помогает опухолевым клеткам уклоняться от недавно описанного типа гибели клеток — ферроптоза, зависящего от железа и окислительного повреждения. Выявив этот тормоз, авторы указывают на новые стратегии, которые могут сделать упорные назофарингеальные опухоли более уязвимыми к лечению.
Другой путь гибели раковых клеток
Большинство противораковых препаратов пытаются убить опухолевые клетки, запуская хорошо известные программы гибели, такие как апоптоз. Однако опухоли часто учатся избегать этих путей. Ферроптоз — это особый тип гибели клеток, вызванный железом и вспышками реактивных кислородных молекул, которые разрушают клеточные мембраны, особенно в митохондриях, энергетических станциях клетки. Многие опухоли, устойчивые к стандартной терапии, тем не менее поддаются индукции ферроптоза. Клетки назофарингеальной карциномы особенно чувствительны к препаратам, провоцирующим этот процесс, что делает ферроптоз потенциальным терапевтическим преимуществом — при условии, что учёные поймут, что его сдерживает.
Белок, защищающий опухоли от повреждений, вызванных железом
Исключая большие генетические базы данных и образцы опухолей пациентов, команда сосредоточилась на белке MICAL2, ранее связанном с ростом опухолей и окислительной химией. Они обнаружили, что уровень MICAL2 существенно выше в назофарингеальных опухолях по сравнению с нормальной тканью, а у пациентов с повышенным MICAL2 чаще наблюдаются более прогрессирующее заболевание, большее число метастазов и худшая выживаемость. При снижении уровня MICAL2 в клеточных линиях назофарингеальной карциномы клетки росли и распространялись менее активно и становились значительно более чувствительными к препаратам, индуцирующим ферроптоз, таким как эрастин и сорафениб. Показатели железа, окислительного стресса и антиоксидантного баланса изменялись в сторону усиленного ферроптоза как в культурах клеток, так и в мышиных моделях опухолей.
Недавно обнаруженная РНК, усиливающая щит
Затем исследователи задали вопрос, почему MICAL2 так обилен в этих опухолях. Они обнаружили ранее неохарактеризованную длинную некодирующую РНК, названную LINC-AC092535.5, которая существенно повышена при опухолях головы и шеи и коррелирует с уровнем MICAL2. В отличие от РНК, кодирующих белки, эта РНК действует как регулятор. Она физически связывается с матрицей (молекулой-иммейджером) MICAL2 и усиливает его экспрессию двумя способами: повышает активность промотора гена MICAL2 и замедляет распад МРНК MICAL2. При подавлении LINC-AC092535.5 уровень MICAL2 снижался, маркеры ферроптоза увеличивались, и опухолевые клетки становились более уязвимы к железозависимому окислительному повреждению. Восстановление уровня MICAL2 частично отменяло эти эффекты, что демонстрирует, что эта РНК и MICAL2 работают вместе в укрепляющем контуре, защищающем клетки от ферроптоза.
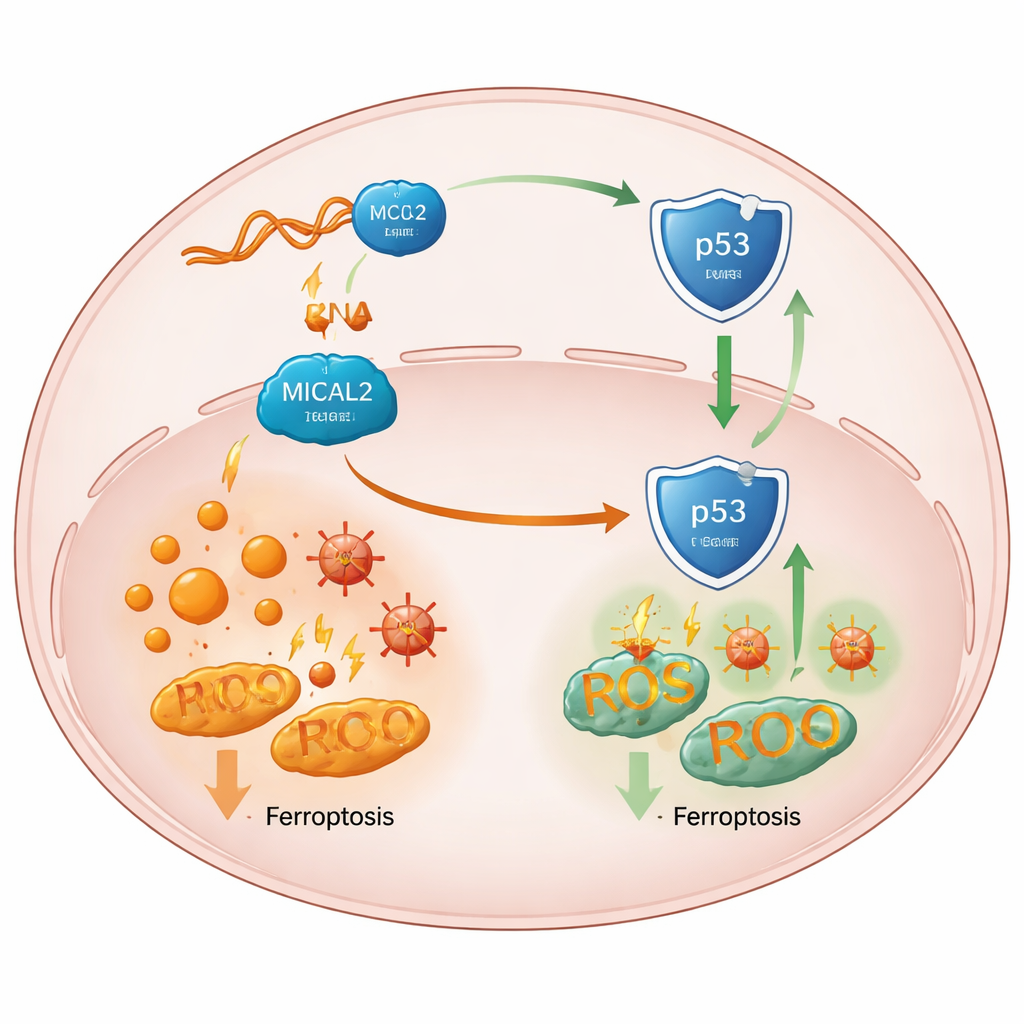
Как «щит» ослабляет ключевого стража опухоли
Углубив анализ, команда проследила влияние MICAL2 до p53 — центрального «стража», который обычно помогает предотвращать опухолеобразование и может стимулировать ферроптоз в стрессированных клетках. Высокая активность MICAL2 подавляла путь p53, тогда как утрата MICAL2 стабилизировала и повышала уровень белка p53 без изменения активности его гена. Исследователи показали, что MICAL2 физически взаимодействует с p53 и с MDM2 — белком, отмечающим p53 для разрушения. MICAL2 способствует тому, чтобы MDM2 прикреплял больше таких меток, направляя p53 в систему утилизации клетки и выталкивая его из ядра, где он в противном случае активировал бы защитные гены. При подавлении MICAL2 или LINC-AC092535.5 p53 накапливался в ядре, его сигналы смещались в сторону ферроптоза, и раковые клетки разных типов демонстрировали повышенную железозависимую гибель — если только сам p53 не удаляли.
Что это означает для будущего лечения
В совокупности работа описывает новую контрольную ось в назофарингеальной карциноме: РНК LINC-AC092535.5 усиливает MICAL2, а MICAL2 в свою очередь помогает лишать p53 его защитного влияния, позволяя опухолевым клеткам сопротивляться ферроптозу. Прерывание этой оси — путем ингибирования РНК, блокирования MICAL2 или предотвращения деградации p53 — может восстановить железозависимую гибель клеток и повысить эффективность существующих препаратов, индуцирующих ферроптоз. Для пациентов с рецидивирующей или резистентной к терапии назофарингеальной карциномой такие комбинации однажды могут предложить способ использовать собственное железо и окислительный стресс опухоли против неё самой.
Цитирование: Zhang, S., Chen, W., Yang, J. et al. LINC-AC092535.5 regulates MICAL2 mRNA level to inhibit p53-mediated ferroptosis in nasopharyngeal carcinoma. Oncogene 45, 1260–1274 (2026). https://doi.org/10.1038/s41388-026-03714-y
Ключевые слова: назофарингеальная карцинома, ферроптоз, p53, длинная некодирующая РНК, MICAL2