Clear Sky Science · zh
PROTAC MDM2 降解剂在原代白血病细胞和 PDX 模型中的活性
对顽固性血液癌的新希望
许多被诊断为急性髓性白血病(AML)的成人面临有限的治疗选择并且复发风险高。本研究探讨了一种新一代药物策略,不仅仅是阻断致癌蛋白,而是直接在白血病细胞内将其摧毁。研究人员针对一个通常抑制机体主要肿瘤抑制蛋白的关键调控因子,展示了一种能够唤醒细胞自身抗癌防线的方法,同时在很大程度上保留健康骨髓的功能。
白血病如何劫持安全开关
我们的细胞依赖一种名为 p53 的守护蛋白来暂停细胞生长、修复 DNA 损伤或在严重异常时触发细胞自杀。在许多癌症中,p53 本身发生突变而失去功能。然而在 AML 中,p53 常常仍然完好,但被另一种蛋白 MDM2 所抑制,MDM2 会标记 p53 使其被降解。许多白血病细胞产生过多的 MDM2,有效地压制了 p53 的警报系统。以往的药物尝试阻断 MDM2 与 p53 的相互作用,但这种方法有一个问题:随着 p53 的短暂恢复,它实际上会促使细胞产生更多的 MDM2,形成一个内在的反馈回路,可能限制这些药物的疗效。
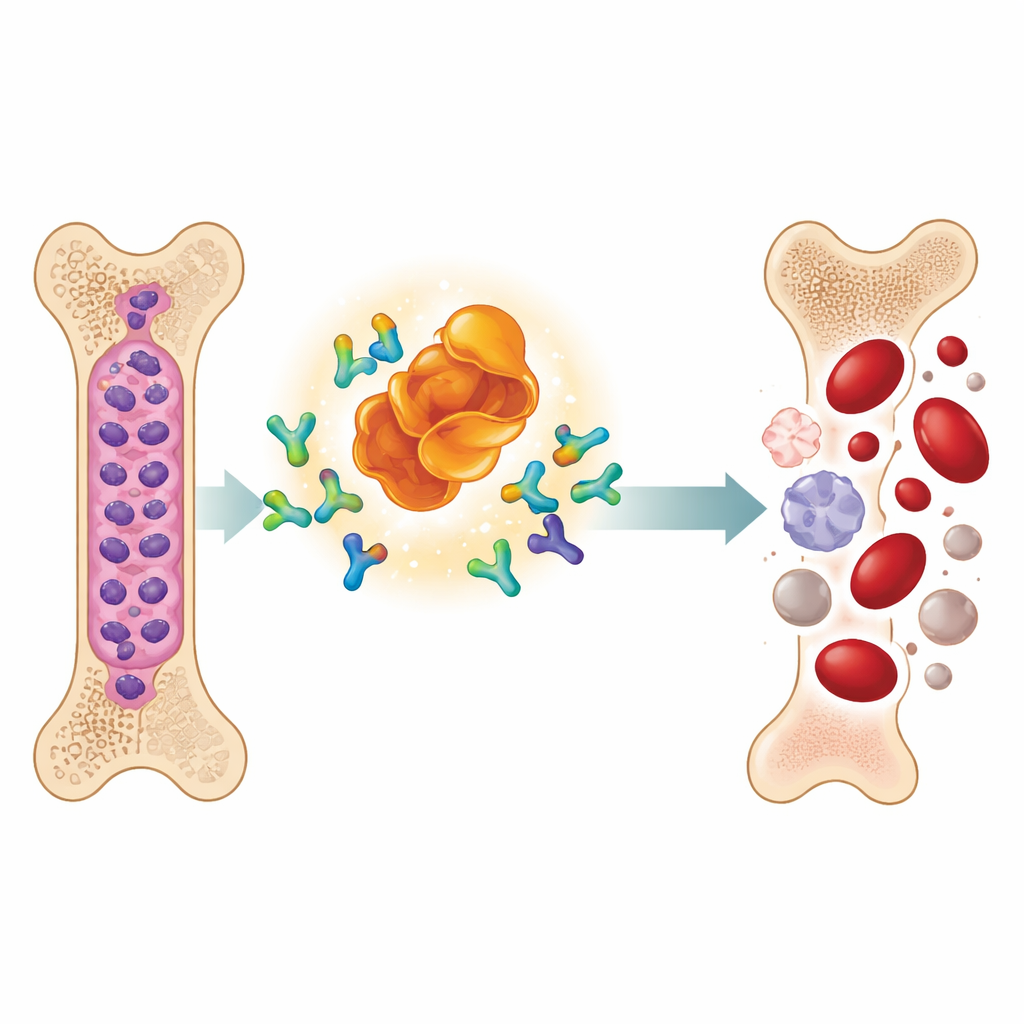
一种让癌症蛋白消失的新型药物
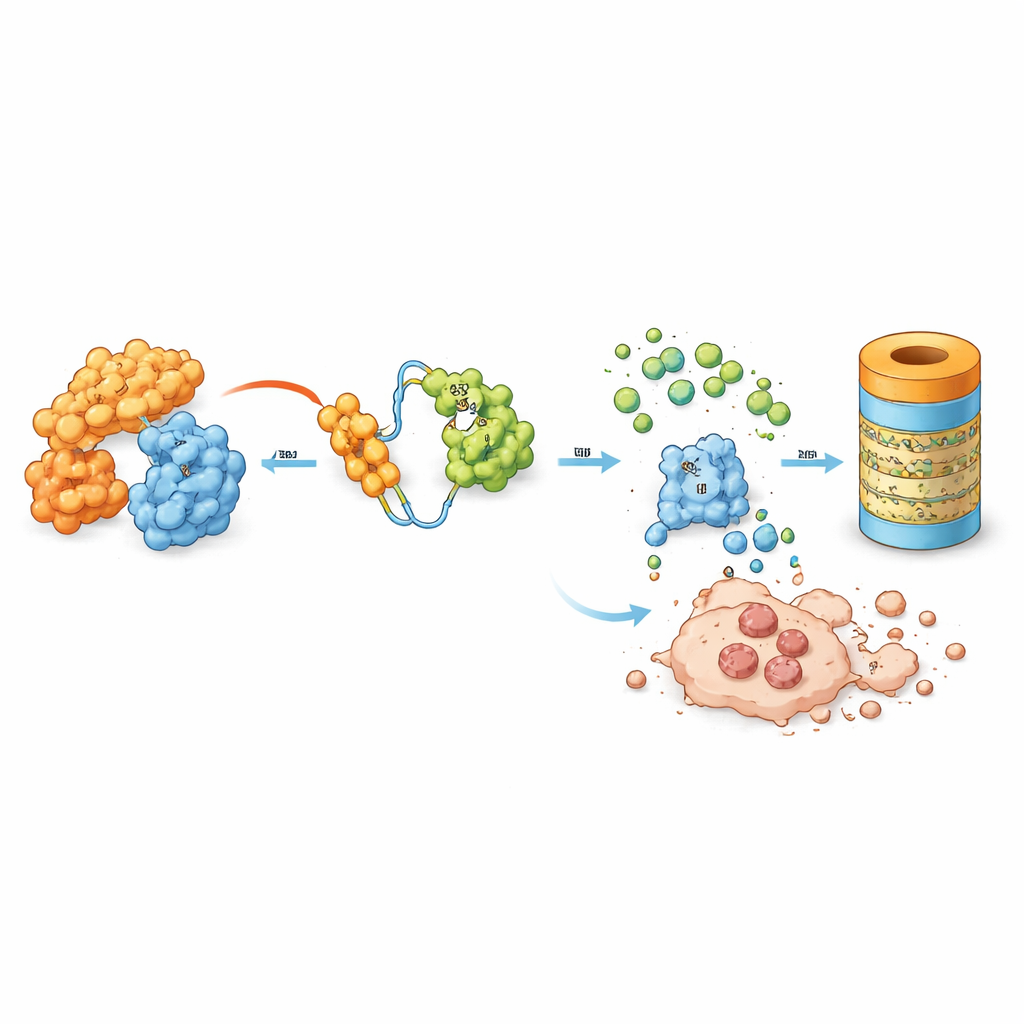
研究团队研究了一种名为 MD‑265 的设计分子,它属于日益增多的 PROTAC 药物类别。MD‑265 并非仅仅黏附在 MDM2 上使其失活,而更像分子牵线者。一端结合 MDM2,另一端招募细胞的天然清除系统。这将 MDM2 带到标记并降解不需要蛋白的机器旁,使细胞将 MDM2 裁剪降解,而不仅仅是阻断它。在对来自 100 名 AML 患者的白血病干细胞进行的体外测试中,MD‑265 在杀伤癌细胞时所需的浓度约为基于相同核心化学骨架的传统 MDM2 抑制剂的千分之一。对降解剂有反应的白血病样本通常也会对抑制剂有反应,但降解剂的效力远高于抑制剂。
比健康细胞更重击癌细胞
任何抗癌药物的一大关注点是对正常组织的损伤,尤其是产生健康血细胞的骨髓细胞。研究者比较了 MD‑265 对白血病干细胞和来自健康供者的造血干细胞的影响。正常细胞对该降解剂的敏感性约比白血病细胞低一百倍,这提示存在有意义的治疗窗。当团队在允许细胞形成集落的培养皿中生长细胞时,MD‑265 显著减少了对敏感 AML 样本的集落形成,而对正常干细胞的影响则要温和得多。那部分对治疗耐受的白血病通常携带受损的 p53 或仅产生很少的 MDM2 及其近亲 MDM4,这也提示了哪些患者可能不会从该策略中受益。
在小鼠中检验该药物
为更贴近人体疾病,研究人员将患者的白血病干细胞移植到特殊的免疫缺陷小鼠中,建立了患者来源的异种移植(PDX)模型。在人体白血病细胞在血液中建立后,给小鼠分别用 MD‑265、一种已进入临床试验的强效口服 MDM2 抑制剂或对照溶液进行治疗。两种药物最初都缩小了白血病负荷,但随时间出现了重要差异。数周后停止治疗,在接受抑制剂的小鼠中白血病迅速反弹,而接受降解剂治疗的小鼠则显示出更慢的再生并总体存活时间更长。值得注意的是,MD‑265 未导致长期抑制剂治疗所见的体重下降,提示耐受性更好。
这对患者意味着什么
综合来看,研究结果表明,直接降解 MDM2 比单纯阻断它更能有效恢复 p53 的抗肿瘤活性,至少在那些仍携带正常 p53 并依赖 MDM2 将其沉默的 AML 细胞中是如此。MD‑265 在非常低的剂量下发挥作用,对白血病细胞的打击远大于对健康造血细胞的影响,避免了老药所引起的 MDM2 不受控上升,并在由患者样本建立的鼠模型中显著延长了生存期。尽管这项工作仍属临床前研究,且未来需仔细评估安全性与耐药性,但它指向了一类有前景的新型白血病治疗方法:通过拆除一个关键的癌症帮手而非仅仅阻拦其作用来施治。
引用: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
关键词: 急性髓性白血病, p53 与 MDM2, PROTAC 降解剂, 靶向蛋白降解, 白血病干细胞