Clear Sky Science · ar
نشاط محلل البروتين PROTAC لمُدرِج MDM2 في خلايا اللوكيميا الأولية ونماذج PDX
أمل جديد في مواجهة سرطانات الدم المقاومة
يواجه العديد من البالغين الذين يُشخَّصون باللوكيميا النخاعية الحادة (AML) خيارات علاجية محدودة واحتمالًا عاليًا للانتكاس. تستكشف هذه الدراسة استراتيجية دوائية من الجيل القادم لا تكتفي بإعاقة بروتين مُسبِّب للسرطان بل تدمره داخل خلايا اللوكيميا. من خلال استهداف منظم رئيسي يبقي عادةً المُكافح الرئيسي للأورام في الجسم تحت السيطرة، يبيّن الباحثون طريقة لإيقاظ دفاعات الخلية ضد السرطان مع حفاظ كبير على نقي العظام الصحي.
كيف تختطف اللوكيميا مفتاح أمان الخلية
تعتمد خلايانا على بروتين حارس يُدعى p53 لإيقاف نمو الخلية، وإصلاح تلف الحمض النووي، أو تحفيز انتحار الخلية عندما تسوء الأمور. في العديد من السرطانات، يتعرض p53 لطفرات ويفقد وظيفته. في حالة AML، غالبًا ما يبقى p53 سليمًا لكنه مكبوت بواسطة بروتين آخر، MDM2، الذي يعلّم p53 على التدمير. تنتج العديد من خلايا اللوكيميا كمية زائدة من MDM2، مما يخمد عمليًا نظام إنذار p53. حاولت الأدوية السابقة حجب تفاعل MDM2 مع p53، لكن لهذه المقاربة مشكلة: عندما يتعافى p53 مؤقتًا، فإنه يحفز الخلايا على إنتاج المزيد من MDM2، ما يخلق حلقة تغذية راجعة تحد من فعالية هذه الأدوية.
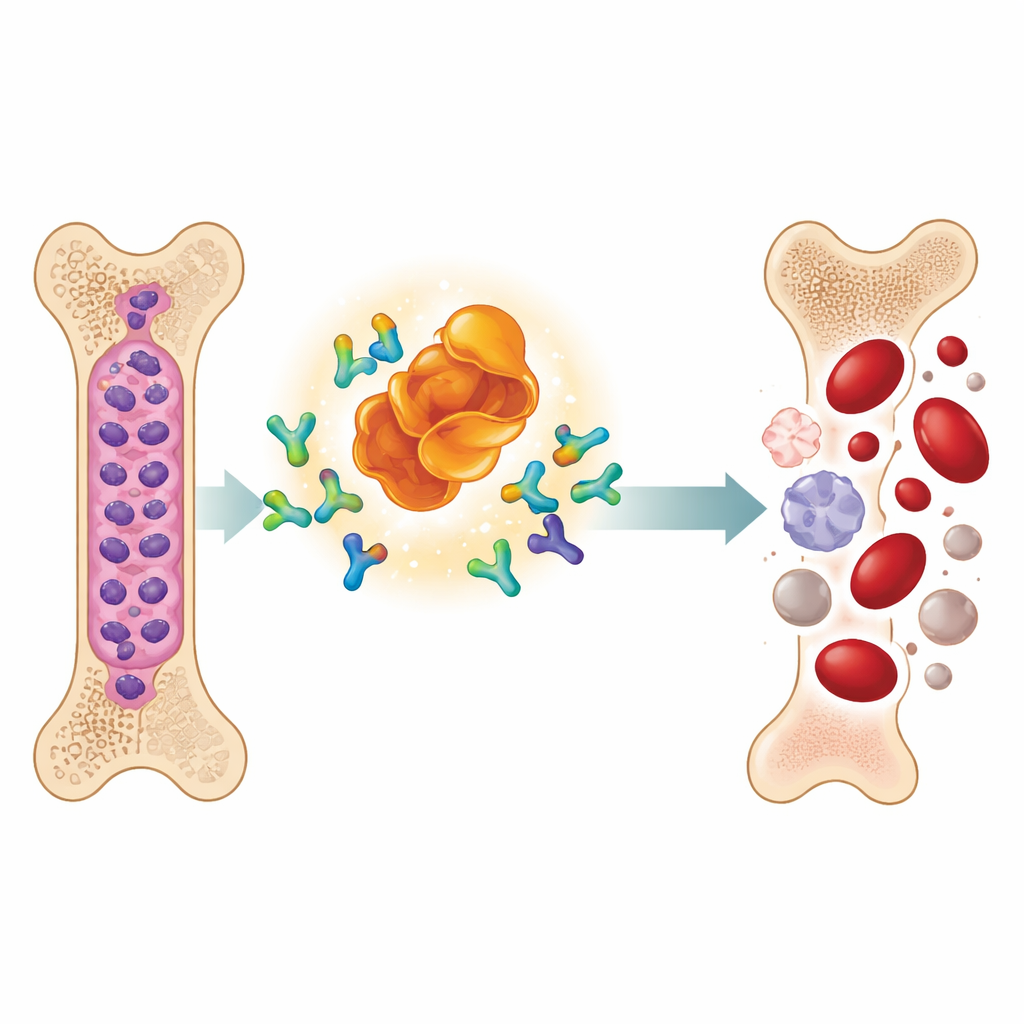
نوع جديد من الأدوية يجعل بروتينات السرطان تختفي
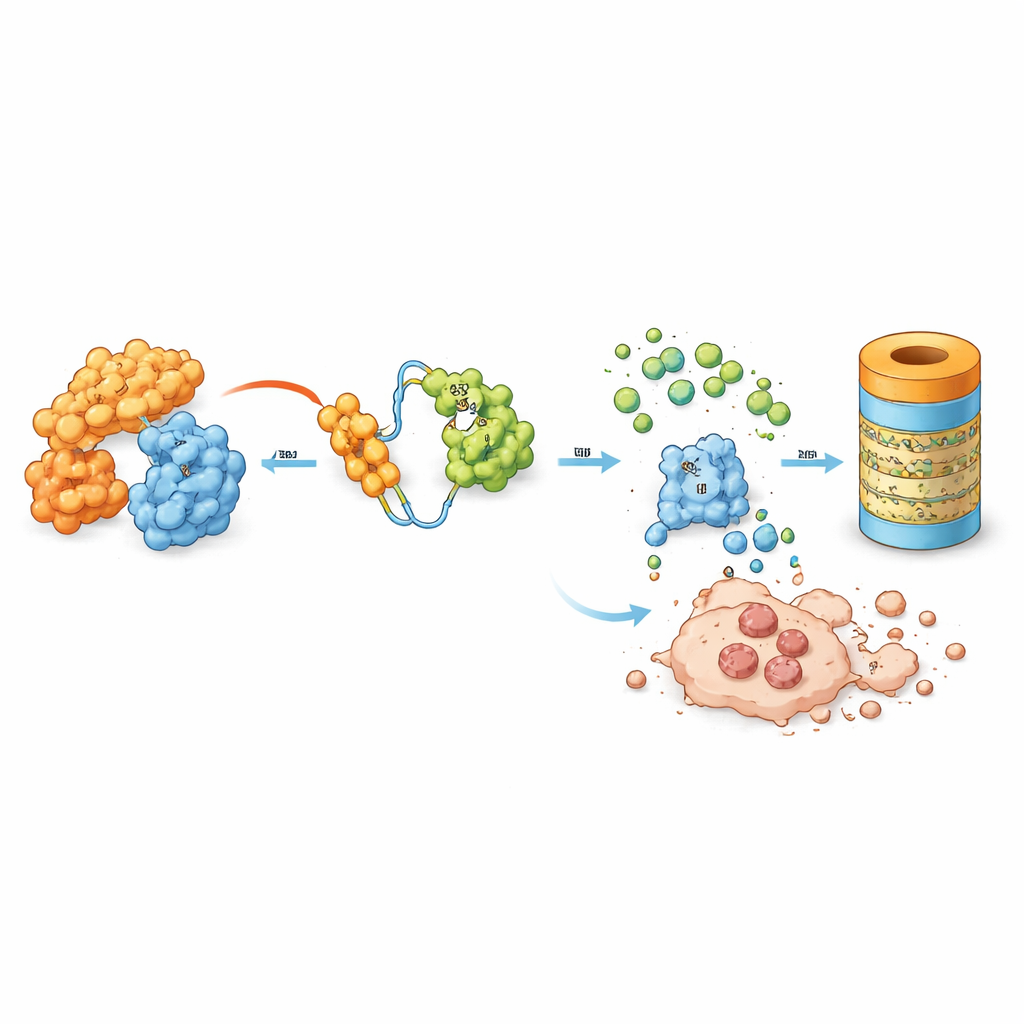
درس الفريق جزيئًا مصممًا يُدعى MD‑265، وهو جزء من فئة متنامية من الأدوية تُعرف باسم PROTACs. بدلًا من الارتباط بـMDM2 وتعطيله فقط، يعمل MD‑265 كوسيط جزيئي. أحد طرفيه يرتبط بـMDM2، والطرف الآخر يستدعي نظام التخلص الخلوي الطبيعي. هذا يقرب MDM2 من الآلية التي توسم البروتينات غير المرغوب فيها للتحلل، مما يؤدي بالخلية إلى تفكيك MDM2 بدلًا من مجرد حظره. في اختبارات مخبرية على خلايا جذعية للوكيميا مأخوذة من 100 مريض بالـAML، قضى MD‑265 على خلايا السرطان بتركيزات أقل بحوالي ألف مرة من مُثبِّط تقليدي لـMDM2 مبني على نفس السقالة الكيميائية الأساسية. كانت عينات اللوكيميا المستجيبة للمحلل تميل أيضًا إلى الاستجابة للمُثبِّط، لكن المحلل كان أقوى بكثير.
ضرب خلايا السرطان أقوى من سلامة الخلايا السليمة
من أكبر المخاوف مع أي دواء مضاد للسرطان هو تلف الأنسجة الطبيعية، لا سيما خلايا نقي العظام التي تُنتِج الدم السليم. قارن الباحثون كيف أثر MD‑265 على خلايا جذعية للوكيميا وخلايا جذعية مكوِّنة للدم من متبرعين أصحّاء. كانت الخلايا الطبيعية أقل حساسية للمحلل بحوالي مئة مرة من خلايا اللوكيميا، ما يشير إلى نافذة علاجية ذات مغزى. عندما نَمَّت الخلايا في طبق يسمح بتكوين المستعمرات، قلّل MD‑265 بشكل حاد من تكوّن المستعمرات في عينات AML الحسّاسة لكنه كان له تأثيرات أخف بكثير على الخلايا الجذعية الطبيعية. المجموعة الصغيرة من حالات اللوكيميا المقاومة للعلاج كانت عموماً تحمل p53 متضررًا أو تنتج كمية قليلة جدًا من MDM2 وشريكها الوثيق MDM4، مما يوضّح أي المرضى قد لا يستفيدون من هذه الاستراتيجية.
اختبار الدواء في الفئران
لمحاكاة المرض البشري بشكل أوثق، زرع الباحثون خلايا جذعية للوكيميا من مرضى في فئران متخصصة ناقصة المناعة، مكوِّنين نماذج زرع خبيثة مشتقة من المرضى (PDX). بعد أن استقرّت خلايا اللوكيميا البشرية في الدم، عولجت الفئران إما بـMD‑265 أو بمثبِّط فموي قوي لـMDM2 يجري اختباره سريريًا، أو بمحلول تحكم. كلا الدواءين قلّلا في البداية العبء اللوكيمياوي، لكن ظهرت اختلافات مهمة مع الوقت. بعد عدة أسابيع، أُوقف العلاج. انتعشت اللوكيميا بسرعة في الفئران التي تلقت المُثبِّط، بينما أظهرت الفئران المعالجة بالمحلل نموًا بطيئًا للخلايا وعايشة أطول بشكل عام. ومن اللافت أن MD‑265 لم يسبب فقدان الوزن الذي لوحظ مع المعالجة المطولة بالمُثبِّط، مما يشير إلى احتمال تحمل أفضل.
ماذا قد يعني هذا للمرضى
مجتمعة، تُظهر النتائج أن تكسير MDM2 مباشرة يمكن أن يعيد تنشيط قوة p53 المضادة للأورام بفعالية أكبر من حجبه فقط، على الأقل في خلايا AML التي لا تزال تحمل p53 طبيعيًا وتعتمد على MDM2 لإسكاته. عمل MD‑265 بجرعات منخفضة جدًا، واستهدف خلايا اللوكيميا بقوة أكبر من خلايا تكوين الدم السليمة، وتجنّب الارتفاع غير المرغوب في MDM2 الذي تسبّب به الأدوية الأقدم، ووسّع البقاء بشكل كبير في نماذج الفئران المبنية من عينات المرضى. وبينما لا تزال هذه الأعمال قبل سريرية ويجب دراسة السلامة والمقاومة بعناية في تجارب لاحقة، فهي تشير إلى فئة واعدة جديدة من علاجات اللوكيميا التي تعمل بتفكيك مساعد رئيسي للسرطان بدلًا من مجرد الوقوف في طريقه.
الاستشهاد: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
الكلمات المفتاحية: اللوكيميا النخاعية الحادة, p53 و MDM2, محلل PROTAC, تحلل البروتين المستهدف, خلايا جذعية للوكيميا