Clear Sky Science · ru
Активность деградерa PROTAC против MDM2 в первичных клетках лейкемии и моделях PDX
Новая надежда для тяжелых кровяных раков
Многие взрослые с диагнозом острый миелобластный лейкоз (ОМЛ) сталкиваются с ограниченными вариантами лечения и высоким риском рецидива. В этом исследовании изучают лекарственную стратегию нового поколения, которая не просто блокирует белок, ведущий к раку, а фактически уничтожает его внутри лейкозных клеток. Нацеливаясь на ключевой регулятор, который обычно сдерживает главный опухолевый супрессор организма, авторы показывают способ снова пробудить собственную защиту клетки от рака при одновременном сохранении большей части здорового костного мозга.
Как лейкемия угнетает аварийный переключатель
Наши клетки зависят от «сторожевого» белка p53, который останавливает рост клетки, восстанавливает поврежденную ДНК или запускает самоуничтожение, когда что‑то идет серьезно не так. Во многих опухолях p53 мутирует и перестает работать. В ОМЛ, однако, p53 часто остается интактным, но его подавляет другой белок, MDM2, помечающий p53 для разрушения. Многие лейкозные клетки вырабатывают слишком много MDM2, эффективно заглушая систему оповещения p53. Ранние препараты пытались блокировать взаимодействие MDM2 и p53, но у этого подхода есть подвох: по мере кратковременного восстановления p53 он сам стимулирует синтез большего количества MDM2, создавая встроенную петлю обратной связи, которая может ограничивать эффективность таких лекарств.
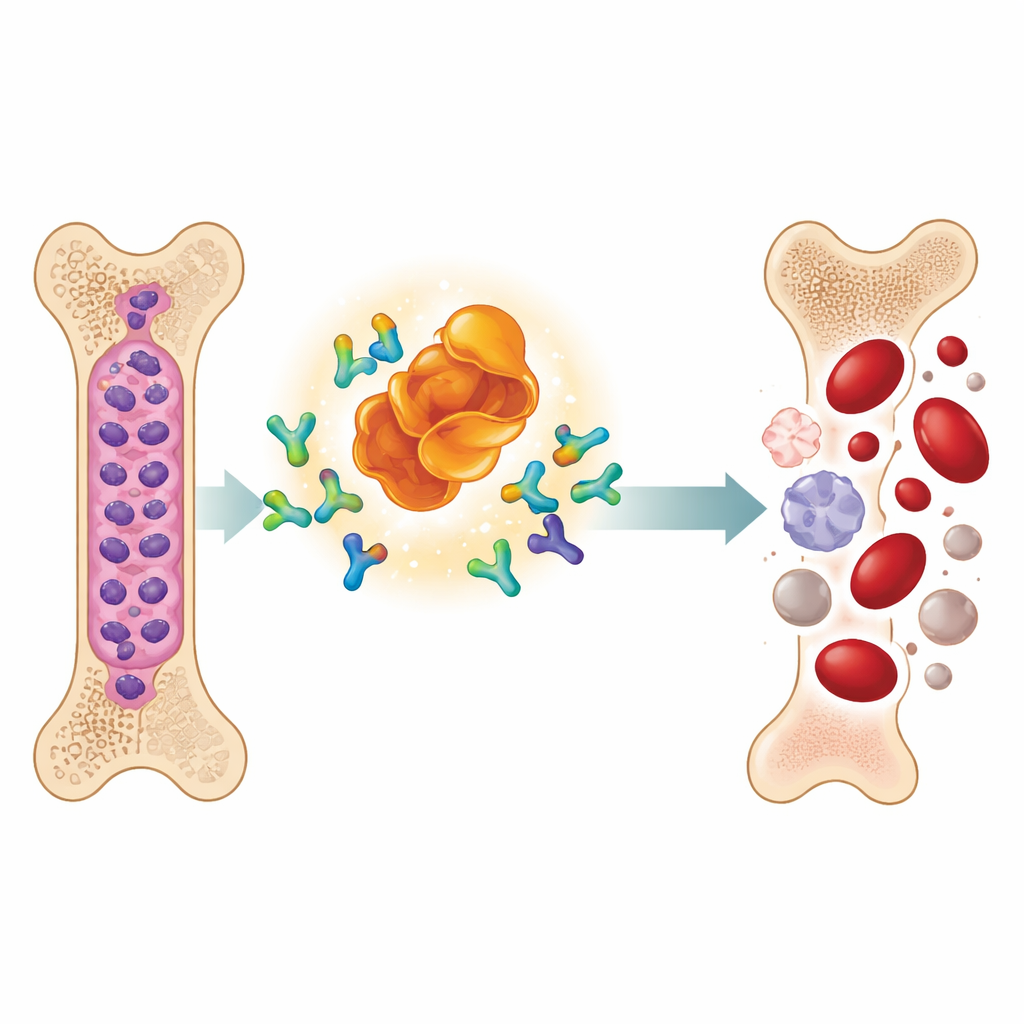
Новый тип препарата, заставляющий онкобелки исчезать
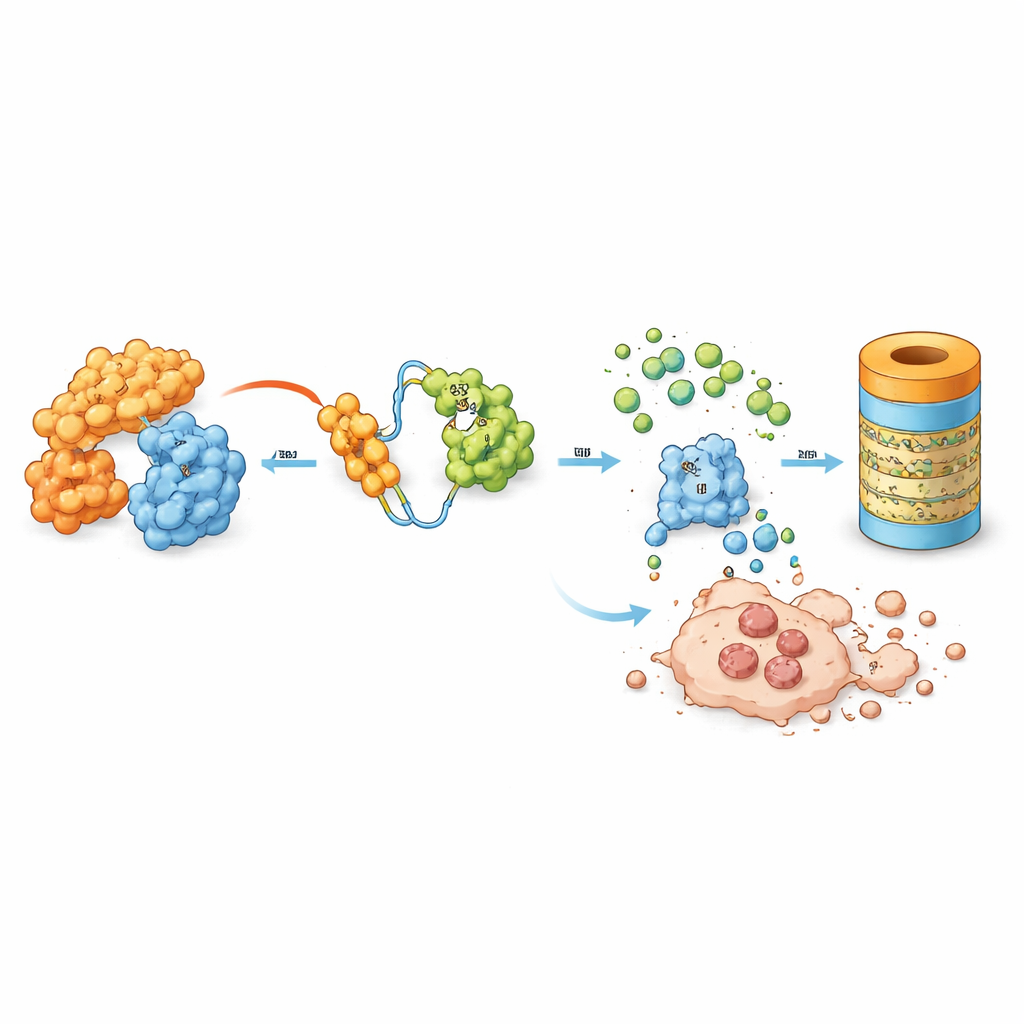
Группа изучала дизайнерскую молекулу MD‑265, которая относится к растущему классу препаратов, известных как PROTAC. Вместо того чтобы просто связываться с MDM2 и отключать его, MD‑265 действует как молекулярный сваха: один конец связывается с MDM2, другой привлекает природную клеточную систему утилизации. Это сближает MDM2 с механизмами, помечающими нежелательные белки для разрушения, в результате чего клетка не блокирует, а расщепляет MDM2. В лабораторных испытаниях на стволовых клетках лейкемии, взятых у 100 пациентов с ОМЛ, MD‑265 убивал раковые клетки при концентрациях примерно в тысячу раз ниже, чем обычный ингибитор MDM2, построенный на той же химической основе. Образцы лейкемии, чувствительные к деградеру, как правило, также реагировали на ингибитор, но деградер оказался значительно более мощным.
Наносить удар по раковым клеткам сильнее, чем по здоровым
Главное опасение любого противоракового препарата — повреждение нормальных тканей, особенно клеток костного мозга, производящих здоровую кровь. Исследователи сравнили влияние MD‑265 на стволовые клетки лейкемии и на нормальные гемопоэтические стволовые клетки доноров. Нормальные клетки были примерно в сто раз менее чувствительны к деградеру, чем лейкозные, что указывает на значимое терапевтическое окно. Когда команды выращивали клетки в среде, позволяющей им формировать колонии, MD‑265 резко снижал образование колоний в чувствительных образцах ОМЛ, тогда как влияние на нормальные стволовые клетки было гораздо слабее. Небольшая группа лейкозов, устойчивых к лечению, как правило, несла поврежденный p53 или вырабатывала очень мало MDM2 и его близкого партнера MDM4, что указывает, какие пациенты, вероятно, не получат пользы от этой стратегии.
Испытание препарата на мышах
Чтобы лучше имитировать человеческое заболевание, исследователи трансплантировали стволовые клетки лейкемии пациентов в специализированных иммунодефицитных мышей, создав модели ксенотрансплантатов, полученных от пациентов (PDX). После того как человеческие лейкозные клетки прижились в крови мышей, животных лечили либо MD‑265, либо мощным пероральным ингибитором MDM2, уже находящимся в клинических испытаниях, либо контрольным раствором. Оба препарата изначально уменьшали нагрузку лейкемии, но со временем проявились важные различия. Через несколько недель лечение прекратили. У мышей, получавших ингибитор, лейкемия быстро рецидивировала, тогда как у тех, кого лечили деградером, регенерация была намного медленнее, а продолжительность жизни в целом — больше. Примечательно, что MD‑265 не вызывал потери веса, наблюдавшейся при длительном лечении ингибитором, что говорит о лучшей переносимости.
Что это может значить для пациентов
В сумме результаты показывают, что прямое разрушение MDM2 может эффективнее возродить антипухолевую функцию p53, чем простое его блокирование, по крайней мере в тех клетках ОМЛ, где p53 остается нормальным и зависит от MDM2 для своего подавления. MD‑265 работал при очень низких дозах, поражал лейкозные клетки гораздо сильнее, чем нормальные гемопоэтические клетки, избегал нежелательного всплеска MDM2, вызванного старыми препаратами, и значительно продлевал выживание в моделях мышей, созданных на основе образцов пациентов. Хотя это исследование пока доклиническое и безопасность и развитие резистентности должны быть тщательно изучены в будущих испытаниях, оно указывает на перспективный новый класс препаратов против лейкемии, действующих путем разрушения ключевого «помощника» рака, а не лишь мешая ему.
Цитирование: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
Ключевые слова: острый миелобластный лейкоз, p53 и MDM2, деградер PROTAC, таргетное разрушение белков, стволовые клетки лейкемии