Clear Sky Science · pt
Atividade de degrader PROTAC de MDM2 em células primárias de leucemia e modelos PDX
Nova esperança para cânceres sanguíneos difíceis
Muitos adultos diagnosticados com leucemia mieloide aguda (LMA) enfrentam opções de tratamento limitadas e alta probabilidade de recaída. Este estudo investiga uma estratégia farmacológica de próxima geração que não apenas bloqueia uma proteína que impulsiona o câncer, mas a destrói dentro das células leucêmicas. Ao mirar um regulador chave que normalmente mantém o principal supressor tumoral do corpo sob controle, os pesquisadores mostram uma maneira de reativar as defesas celulares contra o câncer enquanto preservam grande parte da medula óssea saudável.
Como a leucemia sequestra um interruptor de segurança
Nossas células dependem de uma proteína guardiã chamada p53 para pausar o crescimento celular, reparar danos ao DNA ou desencadear a morte celular quando algo dá muito errado. Em muitos cânceres, o próprio p53 está mutado e já não funciona. Na LMA, entretanto, o p53 frequentemente permanece intacto, mas é mantido sob controle por outra proteína, a MDM2, que marca o p53 para destruição. Muitas células leucêmicas produzem MDM2 em excesso, efetivamente abafando o sistema de alarme do p53. Drogas anteriores tentaram bloquear a interação entre MDM2 e p53, mas essa abordagem tem um problema: à medida que o p53 se recupera temporariamente, ele estimula a produção de mais MDM2, criando um loop de retroalimentação que pode limitar a eficácia desses medicamentos.
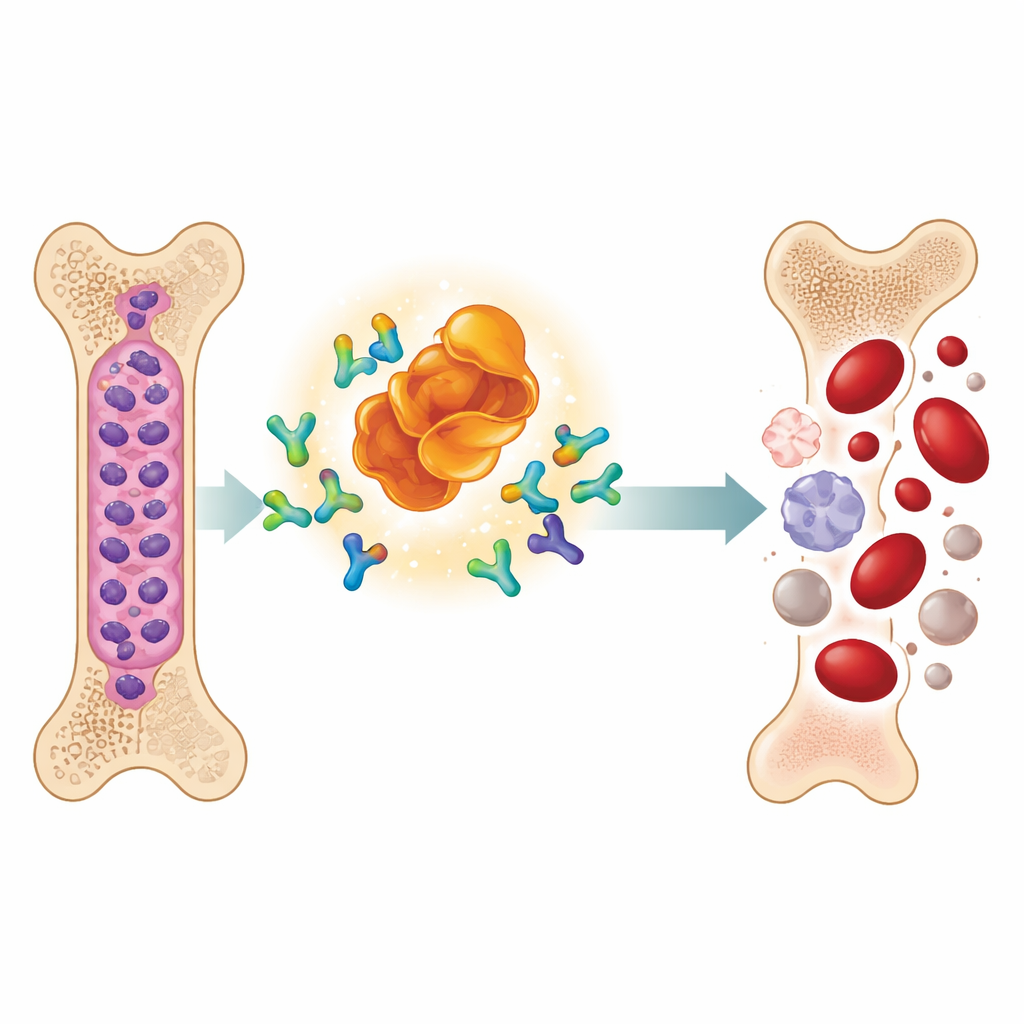
Um novo tipo de droga que faz proteínas cancerígenas desaparecerem
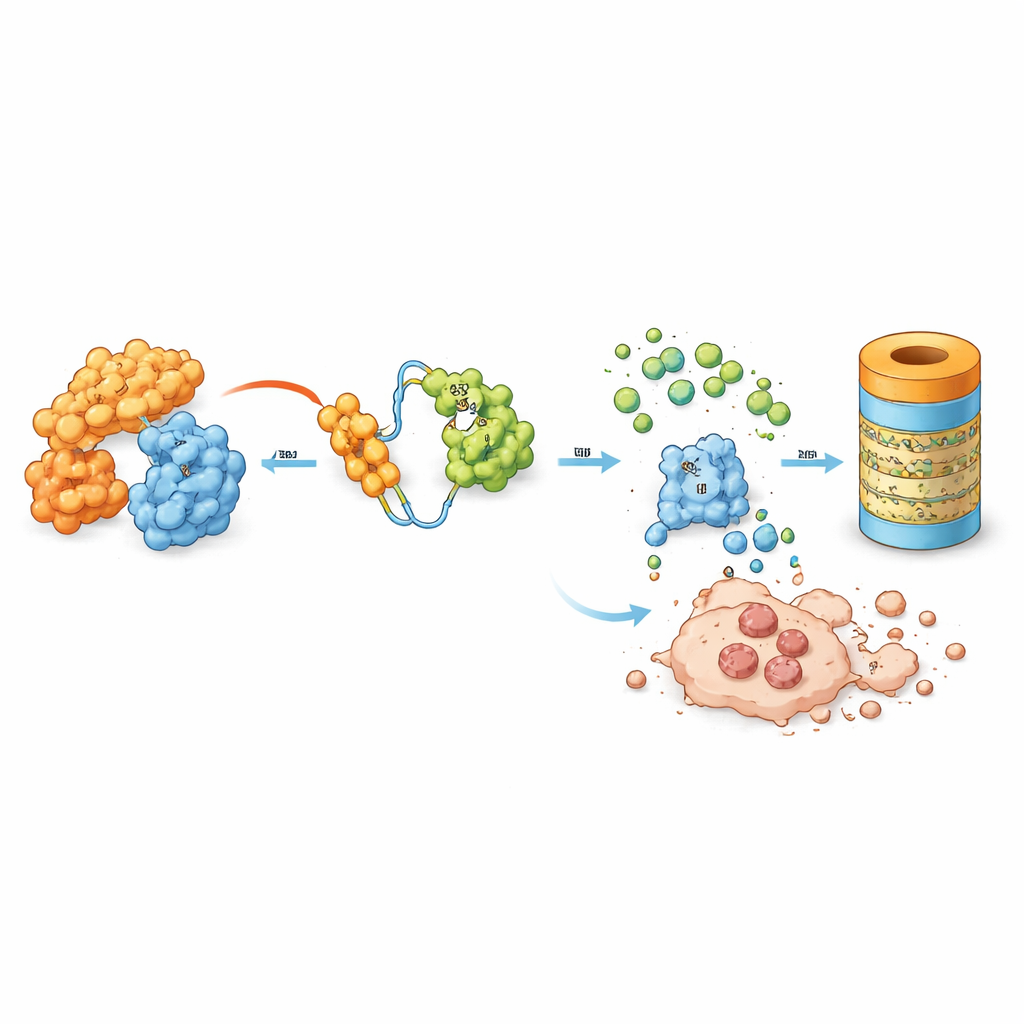
A equipe estudou uma molécula desenhada chamada MD‑265, parte de uma classe crescente de fármacos conhecidos como PROTACs. Em vez de simplesmente aderir à MDM2 e desativá‑la, o MD‑265 age como um casamenteiro molecular. Uma extremidade liga‑se à MDM2, a outra recruta um sistema natural de descarte celular. Isso aproxima a MDM2 das máquinas que marcam proteínas indesejadas para degradação, levando a célula a degradar a MDM2 em vez de apenas bloqueá‑la. Em testes laboratoriais com células‑tronco leucêmicas obtidas de 100 pacientes com LMA, o MD‑265 matou células cancerígenas em concentrações aproximadamente mil vezes menores do que um bloqueador convencional de MDM2 construído a partir do mesmo esqueleto químico. Amostras de leucemia que responderam ao degrader também tenderam a responder ao inibidor, mas o degrader foi muito mais potente.
Atacando células cancerígenas com mais força do que células saudáveis
Uma preocupação importante com qualquer droga contra o câncer é o dano aos tecidos normais, especialmente às células da medula óssea que produzem sangue saudável. Os pesquisadores compararam como o MD‑265 afetou células‑tronco leucêmicas e células‑tronco hematopoiéticas normais de doadores saudáveis. As células normais foram cerca de cem vezes menos sensíveis ao degrader do que as leucêmicas, sugerindo uma janela terapêutica relevante. Quando a equipe cultivou células em prato permitindo a formação de colônias, o MD‑265 reduziu fortemente a formação de colônias em amostras de LMA sensíveis, mas teve efeitos muito mais brandos nas células‑tronco normais. O pequeno grupo de leucemias que resistiu ao tratamento geralmente carregava p53 danificado ou produzia muito pouca MDM2 e sua parceira próxima MDM4, evidenciando quais pacientes podem não se beneficiar dessa estratégia.
Testando a droga em camundongos
Para mimetizar mais de perto a doença humana, os investigadores transplantaram células‑tronco leucêmicas de pacientes em camundongos especializados com deficiência imunológica, criando modelos xenotransplantados derivados de pacientes (PDX). Uma vez que as células leucêmicas humanas se estabeleceram no sangue, os camundongos foram tratados com MD‑265, com um potente inibidor oral de MDM2 já em testes clínicos, ou com uma solução controle. Ambos os fármacos reduziram inicialmente a carga leucêmica, mas diferenças importantes emergiram ao longo do tempo. Após várias semanas, o tratamento foi interrompido. A leucemia retornou rapidamente nos camundongos que receberam o inibidor, enquanto aqueles tratados com o degrader apresentaram recrescimento muito mais lento e viveram mais tempo no geral. Notavelmente, o MD‑265 não causou a perda de peso observada com o tratamento prolongado pelo inibidor, sugerindo melhor tolerabilidade.
O que isso pode significar para pacientes
Em conjunto, os achados mostram que degradar diretamente a MDM2 pode reavivar com mais eficácia o poder antitumoral do p53 do que simplesmente bloqueá‑lo, ao menos em células de LMA que ainda possuem p53 normal e dependem da MDM2 para silenciá‑lo. O MD‑265 atuou em doses muito baixas, afetou as células leucêmicas muito mais fortemente do que as células hematopoiéticas saudáveis, evitou o aumento indesejado de MDM2 causado por drogas antigas e estendeu significativamente a sobrevida em modelos murinos derivados de amostras de pacientes. Embora este trabalho ainda seja pré‑clínico e a segurança e resistência precisem ser avaliadas cuidadosamente em ensaios futuros, ele aponta para uma promissora nova classe de tratamentos contra a leucemia que funcionam desmontando um ajudante chave do câncer em vez de apenas atrapalhá‑lo.
Citação: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
Palavras-chave: leucemia mieloide aguda, p53 e MDM2, degrader PROTAC, degradação proteica direcionada, células‑tronco da leucemia