Clear Sky Science · sv
Aktivitet hos PROTAC‑nedbrytare av MDM2 i primära leukemiceller och PDX‑modeller
Nytt hopp för svåra blodcancerformer
Många vuxna som får diagnosen akut myeloisk leukemi (AML) har begränsade behandlingsalternativ och hög risk för återfall. Denna studie undersöker en nästa generations läkemedelsstrategi som inte bara blockerar ett cancerdrivande protein utan faktiskt förstör det inne i leukemicellerna. Genom att rikta in sig på en nyckelregulator som normalt håller kroppens främsta tumörsuppressor i schack visar forskarna ett sätt att återväcka cellens egna försvar mot cancer samtidigt som stor del av den friska benmärgen sparas.
Hur leukemin kapar en säkerhetsbrytare
Våra celler är beroende av ett väktarprotein kallat p53 för att pausa celldelning, reparera DNA‑skada eller utlösa celldöd när något går allvarligt fel. I många cancerformer är p53 själv muterat och fungerar inte längre. I AML är p53 däremot ofta intakt men hålls ned av ett annat protein, MDM2, som märker p53 för nedbrytning. Många leukemiceller producerar för mycket MDM2 och tystar därigenom p53:s larmsystem. Tidigare läkemedel försökte blockera interaktionen mellan MDM2 och p53, men denna strategi har en hake: när p53 tillfälligt återhämtar sig driver det faktiskt cellerna att producera mer MDM2, vilket skapar en inbyggd återkopplingsslinga som kan begränsa hur väl dessa mediciner fungerar.
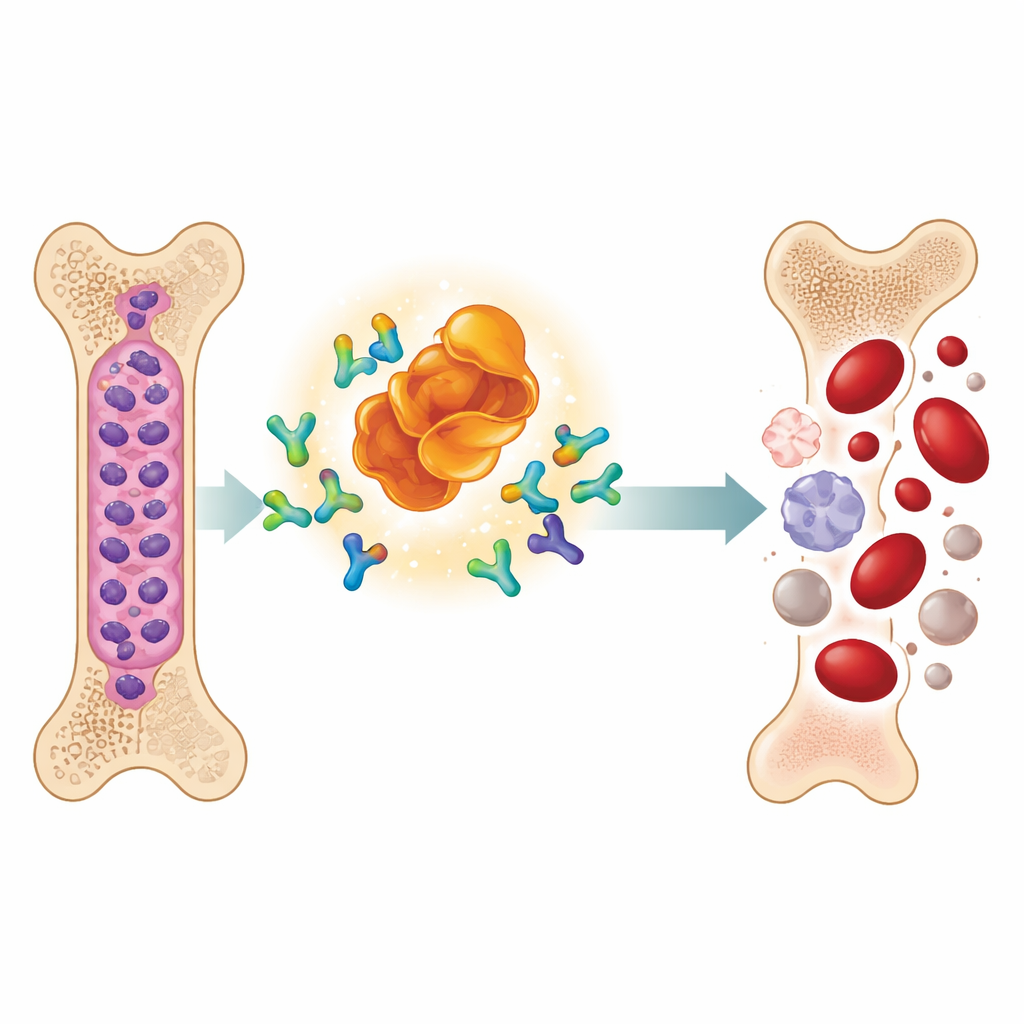
En ny typ av läkemedel som får cancerproteiner att försvinna
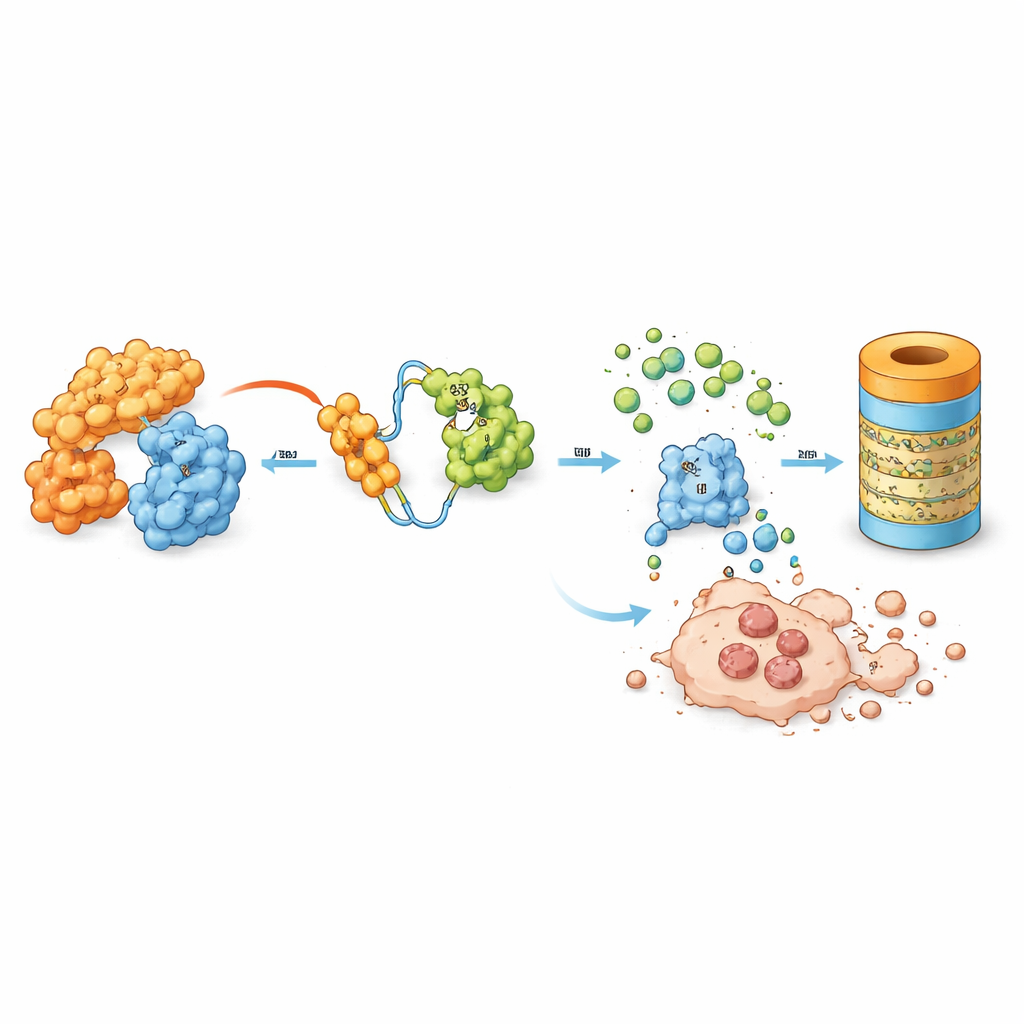
Forskargruppen studerade en designer‑molekyl kallad MD‑265, en del av en växande klass läkemedel kända som PROTACs. I stället för att bara fästa vid MDM2 och inaktivera det fungerar MD‑265 som en molekylär matchmakare. Den ena änden binder MDM2, den andra rekryterar cellens egna avfallshanteringssystem. Detta för MDM2 i nära kontakt med maskineriet som märker oönskade proteiner för nedbrytning, vilket leder till att cellen sönderdelar MDM2 i stället för att bara blockera det. I laboratorietester på leukemistamceller tagna från 100 AML‑patienter dödade MD‑265 cancerceller vid koncentrationer ungefär tusen gånger lägre än en konventionell MDM2‑hämmare byggd på samma kemiska kärna. Leukemiprover som svarade på nedbrytaren tenderade också att svara på hämmaren, men nedbrytaren var långt mer potent.
Att slå hårdare mot cancerceller än mot friska celler
En stor oro med alla cancerläkemedel är skada på normala vävnader, särskilt benmärgscellerna som bildar friska blodkroppar. Forskarna jämförde hur MD‑265 påverkade leukemistamceller och normala blodbildande stamceller från friska givare. Normala celler var ungefär hundra gånger mindre känsliga för nedbrytaren än leukemiceller, vilket tyder på ett meningsfullt terapeutiskt fönster. När teamet odlade cellerna i en rätt som tillåter kolonibildning minskade MD‑265 kraftigt kolonibildningen i känsliga AML‑prover men hade mycket mildare effekter på normala stamceller. Den lilla grupp leukemier som var resistenta bar ofta skadat p53 eller producerade mycket lite MDM2 och dess närstående partner MDM4, vilket belyser vilka patienter som sannolikt inte skulle dra nytta av denna strategi.
Test av läkemedlet i möss
För att efterlikna människosjukdomen bättre transplanterade forskarna leukemistamceller från patienter till specialiserade immundefekta möss och skapade patient‑deriverade xenograft‑modeller (PDX). När mänskliga leukemiceller etablerat sig i blodet behandlades mössen antingen med MD‑265, med en potent oral MDM2‑hämmare som redan prövas i kliniska studier, eller med en kontrolllösning. Båda läkemedlen minskade inledningsvis leukemibördan, men viktiga skillnader framträdde över tid. Efter flera veckor stoppades behandlingen. Leukemin återkom snabbt i möss som fått hämmaren, medan de som behandlats med nedbrytaren visade mycket långsammare återväxt och levde längre totalt sett. Noterbart var att MD‑265 inte orsakade den viktnedgång som sågs vid långvarig hämmarbehandling, vilket tyder på bättre tolerabilitet.
Vad detta kan innebära för patienter
Tillsammans visar resultaten att direkt nedbrytning av MDM2 kan återuppliva p53:s tumörbekämpande kraft mer effektivt än att bara blockera det, åtminstone i AML‑celler som fortfarande bär normalt p53 och förlitar sig på MDM2 för att tysta det. MD‑265 fungerade i mycket låga doser, träffade leukemiceller betydligt hårdare än friska blodbildande celler, undvek den oönskade ökningen av MDM2 som äldre läkemedel ger och förlängde betydligt överlevnaden i musemodeller byggda från patientprover. Även om detta arbete fortfarande är prekliniskt och säkerhet samt resistens måste studeras noggrant i kommande studier pekar det mot en lovande ny klass av leukemibehandlingar som verkar genom att montera ner en nyckelhjälpare för cancer i stället för att bara stå i vägen för den.
Citering: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
Nyckelord: akut myeloisk leukemi, p53 och MDM2, PROTAC‑nedbrytare, målinriktad proteinnedbrytning, lektiska stamceller