Clear Sky Science · pl
Działanie degradatora PROTAC MDM2 w pierwotnych komórkach białaczkowych i modelach PDX
Nowa nadzieja dla opornych nowotworów krwi
Wiele dorosłych osób z rozpoznaną ostrą białaczką szpikową (AML) dysponuje ograniczonymi opcjami leczenia i ma wysokie ryzyko nawrotu. Badanie to analizuje strategię lekową nowej generacji, która nie tylko blokuje białko napędzające nowotwór, lecz rzeczywiście je niszczy w komórkach białaczkowych. Celując w kluczowy regulator, który zwykle tłumi główny supresor nowotworowy organizmu, autorzy pokazują sposób na ponowne uruchomienie własnych mechanizmów obronnych komórki przy jednoczesnym oszczędzaniu dużej części zdrowej szpiku kostnego.
Jak białaczka przejmuje wyłącznik bezpieczeństwa
Nasze komórki polegają na białku‑strażniku zwanym p53, które potrafi zatrzymać wzrost komórkowy, naprawić uszkodzenia DNA lub wywołać apoptozę, gdy coś idzie nie tak. W wielu nowotworach p53 jest sam w sobie zmutowany i przestaje działać. W AML jednak p53 często pozostaje nienaruszony, lecz jest tłumiony przez inne białko — MDM2 — które oznacza p53 do degradacji. Wiele komórek białaczkowych produkuje nadmiar MDM2, skutecznie wyciszając alarm p53. Wcześniejsze leki próbowały blokować interakcję MDM2 z p53, ale to podejście ma wadę: gdy p53 chwilowo wraca do działania, napędza produkcję większej ilości MDM2, tworząc sprzężenie zwrotne, które może ograniczać skuteczność tych środków.
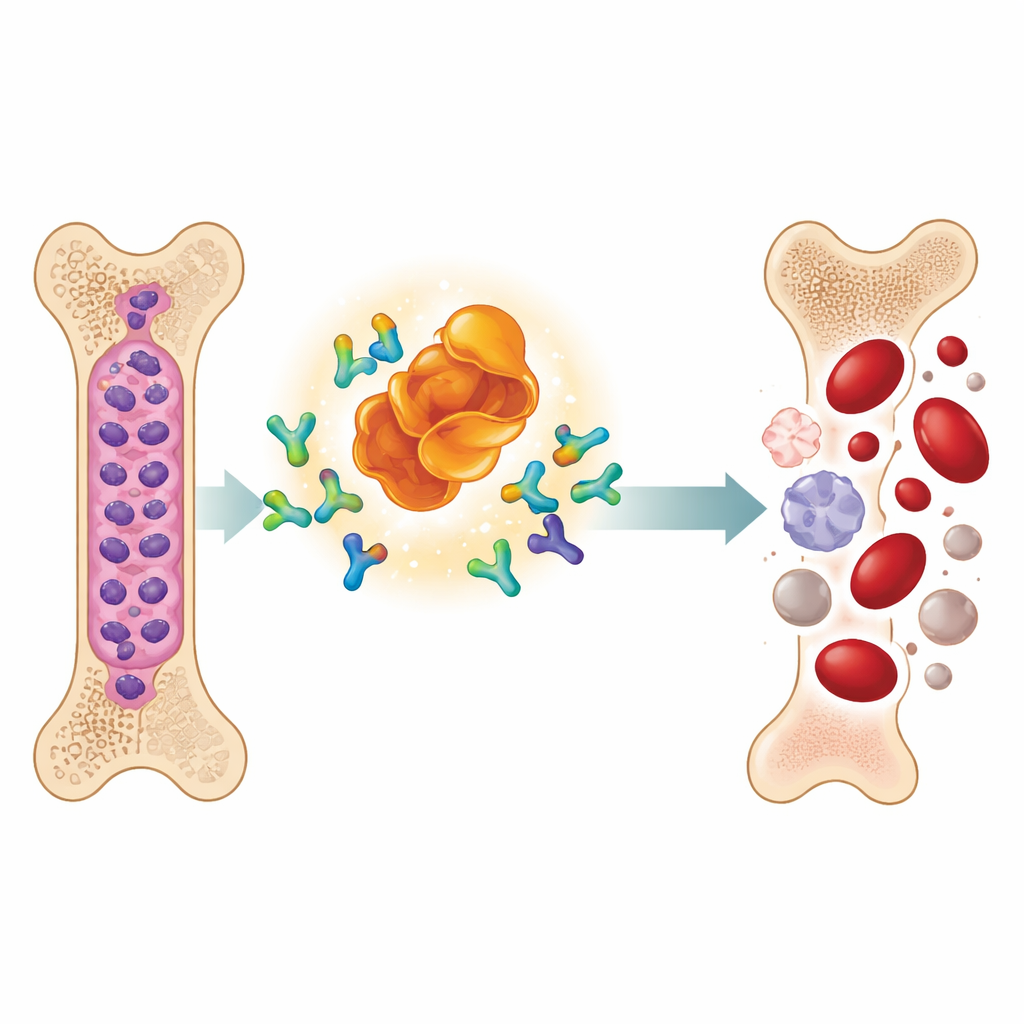
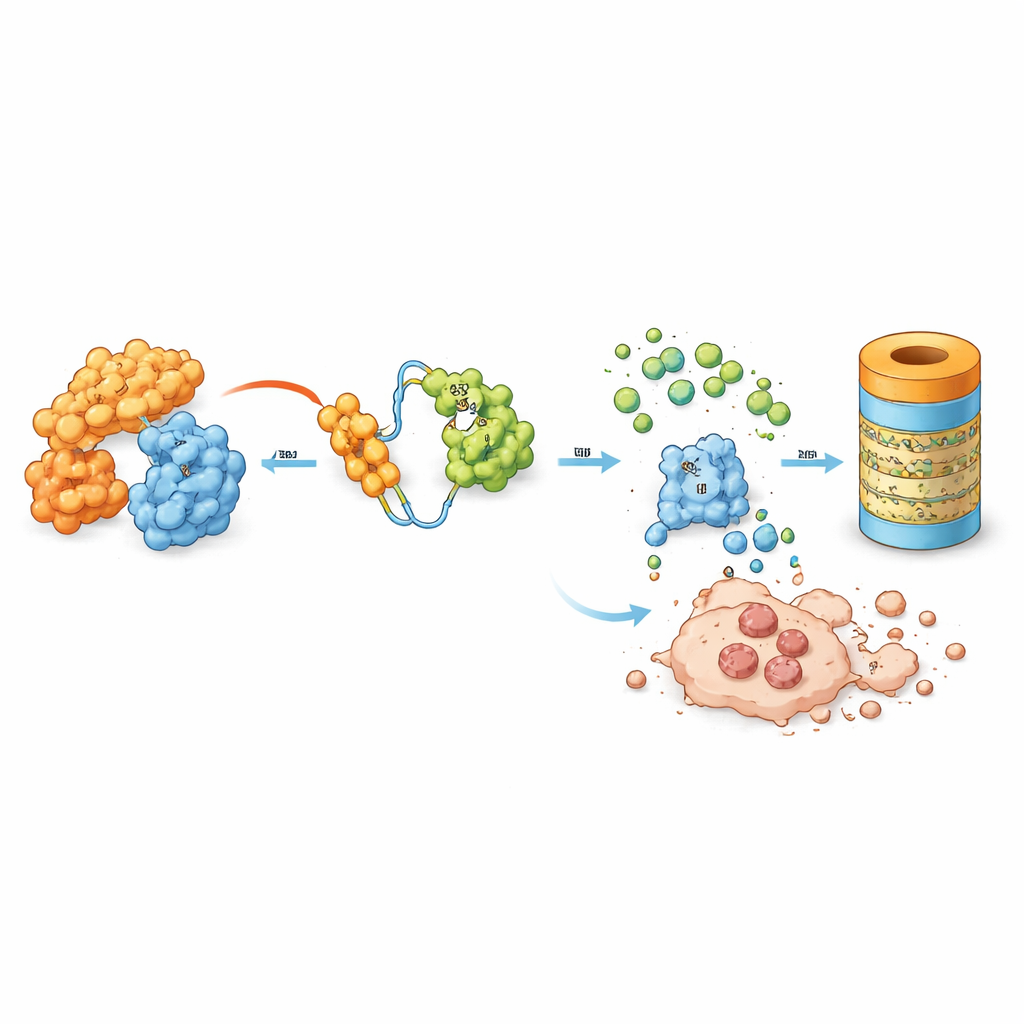
Nowy rodzaj leku, który sprawia, że białka nowotworowe znikają
Zespół badał zaprojektowaną cząsteczkę nazwaną MD‑265, należącą do rosnącej klasy leków znanych jako PROTAC. Zamiast jedynie przyłączać się do MDM2 i go unieszkodliwiać, MD‑265 działa jak molekularny swat. Jeden koniec wiąże się z MDM2, drugi rekrutuje naturalny komórkowy system utylizacji. To sprowadza MDM2 w bliski kontakt z maszynerią oznaczającą niechciane białka do rozkładu, co prowadzi do przetworzenia MDM2 zamiast jego prostego zablokowania. W testach laboratoryjnych na komórkach macierzystych białaczki pobranych od 100 pacjentów z AML, MD‑265 zabijał komórki nowotworowe w stężeniach około tysiąc razy niższych niż konwencjonalny inhibitor MDM2 zbudowany z tego samego rdzenia chemicznego. Próbki białaczki reagujące na degradator zwykle też reagowały na inhibitor, lecz degradator okazywał się znacznie bardziej aktywny.
Silniejsze uderzenie w komórki nowotworowe niż w zdrowe
Głównym zmartwieniem każdego leku przeciwnowotworowego jest uszkodzenie tkanek normalnych, zwłaszcza komórek szpiku odpowiedzialnych za produkcję zdrowej krwi. Badacze porównali wpływ MD‑265 na komórki macierzyste białaczki i normalne komórki krwiotwórcze od zdrowych dawców. Komórki normalne były około sto razy mniej wrażliwe na degradator niż komórki białaczkowe, co sugeruje istotne okno terapeutyczne. Gdy zespół hodował komórki na pożywce w taki sposób, że tworzyły kolonie, MD‑265 znacząco zmniejszał formowanie kolonii w wrażliwych próbkach AML, podczas gdy wpływ na normalne komórki macierzyste był znacznie łagodniejszy. Mała grupa białaczek opornych na leczenie zazwyczaj miała uszkodzony p53 lub wytwarzała bardzo mało MDM2 i jego bliskiego partnera MDM4, co wskazuje, którzy pacjenci mogą nie odnieść korzyści z tej strategii.
Testowanie leku na myszach
Aby jak najlepiej odzwierciedlić ludzką chorobę, badacze przeszczepili komórki macierzyste białaczki od pacjentów do specjalnych myszy z defektem układu odpornościowego, tworząc modele xenograftów pochodzących od pacjentów (PDX). Gdy ludzkie komórki białaczkowe zadomowiły się we krwi, myszy leczono MD‑265, silnym doustnym inhibitorem MDM2 będącym już w badaniach klinicznych lub kontrolnym roztworem. Oba leki początkowo zmniejszały obciążenie białaczką, ale z czasem ujawniły się istotne różnice. Po kilku tygodniach leczenie przerwano. Białaczka szybko odrastała u mysz leczonych inhibitorem, podczas gdy u zwierząt otrzymujących degradator wzrost był dużo wolniejszy, a żywotność ogólnie dłuższa. Warto zauważyć, że MD‑265 nie powodował utraty masy ciała obserwowanej przy długotrwałym podawaniu inhibitora, co sugeruje lepszą tolerancję.
Co to może znaczyć dla pacjentów
Sumarycznie wyniki pokazują, że bezpośrednie rozkładanie MDM2 może skuteczniej przywrócić przeciwnowotworową funkcję p53 niż jego zwykłe blokowanie, przynajmniej w komórkach AML, które wciąż mają prawidłowy p53 i polegają na MDM2, by go uciszyć. MD‑265 działał w bardzo niskich dawkach, uderzał w komórki białaczkowe znacznie mocniej niż w zdrowe komórki krwiotwórcze, unikał niepożądanego wzrostu MDM2 wywoływanego przez starsze leki i istotnie wydłużał przeżycie w modelach mysich opartych na próbkach pacjentów. Choć prace te pozostają przedkliniczne i bezpieczeństwo oraz mechanizmy oporności będą wymagać dokładnych badań w przyszłych próbach, wskazują na obiecującą nową klasę terapii białaczki, które działają poprzez demontaż kluczowego pomocnika nowotworu, zamiast jedynie mu przeszkadzać.
Cytowanie: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
Słowa kluczowe: ostra białaczka szpikowa, p53 i MDM2, degradator PROTAC, celowane niszczenie białek, komórki macierzyste białaczki