Clear Sky Science · he
פעילות של מפגע PROTAC נגד MDM2 בתאי לוקמיה ראשוניים ובמודלי PDX
תקווה חדשה לסוגי סרטן דם עמידים
מבוגרים שאובחנו עם לויקמיה מיאלואידית חריפה (AML) לעיתים קרובות עומדים בפני אפשרויות טיפול מוגבלות וסיכון גבוה להישנות. המחקר הזה בוחן אסטרטגיית תרופות דור הבא שאינה רק חוסמת חלבון שמניע סרטן, אלא מכריתה אותו בתוך תאי הלוקמיה. על ידי מיקוד בוויסת מרכזי שמעכב בדרך‑כלל את המדכא הגידולי העיקרי של הגוף, החוקרים מראים דרך להעיר מחדש את המערך ההגנתי התאי נגד הסרטן תוך שמירה על מרבית מח העצם הבריא.
איך הלוקמיה חוטפת מתג בטיחות
התאים שלנו תלויים בחלבון שומר בשם p53 שיכול לעצור גדילה תאית, לתקן נזק ל‑DNA או לגרום למות מתוכנן של התא כאשר משהו משתבש. ברבות מהמחלות הסרטניות p53 עצמו מוטנט ואינו תקין. ב‑AML, עם זאת, p53 לעתים קרובות נשאר שלם אך מדוכא על‑ידי חלבון אחר, MDM2, שמסמן את p53 להרס. רבים מתאי הלוקמיה מייצרים MDM2 בכמויות מופרזות, ובכך מחלישים את מערכת האזעקה של p53. תרופות קודמות ניסו לחסום את האינטראקציה בין MDM2 ל‑p53, אבל לשיטה זו יש בעיה: כאשר p53 מתאושש לרגע, הוא בעצם מגרה ביטוי מוגבר של MDM2, ויוצר לולאת משוב פנימית שיכולה להגביל את יעילות התרופות.
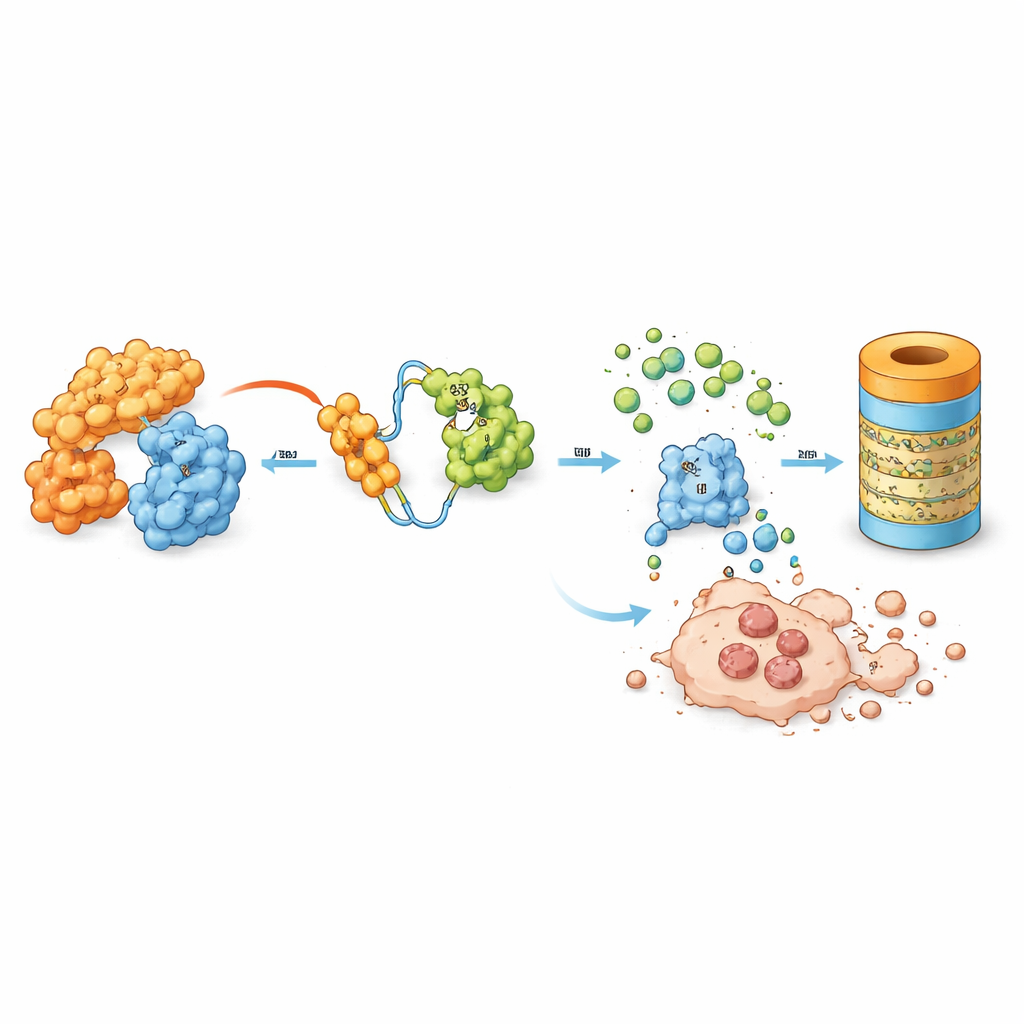
סוג חדש של תרופה שהופכת חלבוני סרטן ללא קיום
הצוות חקר מולקולה מעוצבת בשם MD‑265, המשתייכת למחלקה מתפתחת של תרופות המכונות PROTACs. במקום פשוט להיצמד ל‑MDM2 ולנטרלו, MD‑265 פועל כמתווך מולקולרי: קצה אחד נקשר ל‑MDM2, והקצה השני מושך מערכת פירוק תאית טבעית. זה מביא את MDM2 במגע צמוד עם המכונות המסמנות חלבונים מיותרים לפירוק, מה שמוביל לכך שהתא מפורר את MDM2 במקום רק לחסום אותו. במבחני מעבדה על תאי גזע של לוקמיה שנלקחו מ‑100 חולי AML, MD‑265 הרג תאי סרטן בריכוזים הנמוכים בערך אלף פעמים מאשר מושתק MDM2 מקובל המבוסס על אותו שלד כימי. דגימות לוקמיה שהגיבו לדגרדר נוטות גם להגיב למעכב, אך הדגרדר היה בעל עוצמה רבה בהרבה.
מכת מוות חזקה יותר בתאי סרטן מאשר בתאים בריאים
חשש מרכזי בכל תרופת סרטן הוא נזק לרקמות נורמליות, ובמיוחד לתאי מח עצם המייצרים דם בריא. החוקרים השוו כיצד MD‑265 השפיע על תאי גזע של לוקמיה ועל תאי גזע מייצרי דם נורמליים מתורמים בריאים. התאים הנורמליים היו פחות רגישים לדגרדר בכ‑מאה פעמים מאשר תאי הלוקמיה, מה שמרמז על חלון תרפויטי משמעותי. כאשר הצוות גידל תאים במנה שמאפשרת להם ליצור מושבות, MD‑265 הקטין באופן חד את יצירת המושבות בדגימות AML הרגישות אך היו לו השפעות מתונות בהרבה על תאים גזעיים נורמליים. קבוצת קטנה של לוקמיות שהתנגדו לטיפול נשא בדרך‑כלל p53 פגום או ייצרו מעט מאוד MDM2 ואת השותף הקרוב שלו MDM4, מה שמבליט אילו חולים כנראה לא יפיקו תועלת מאסטרטגיה זו.
בדיקת התרופה בעכברים
כדי לדמות את מחלת האדם באופן קרוב יותר, החוקרים השתילו תאי גזע של לוקמיה ממטופלים בעכברים חסרי מערכת חיסון מיוחדים, ויצרו דגמי קסנוגרפטים שמקורם בחולה (PDX). לאחר שתאי הלוקמיה האנושיים השתלבו בדם, העכברים טופלו ב‑MD‑265, במעכב MDM2 אורלי חזק שכבר נמצא בניסויים קליניים, או בתמיסה בקרה. שתי התרופות הצטמקו בתחילה את עומס הלוקמיה, אך עם הזמן הופיעו הבדלים משמעותיים. לאחר כמה שבועות הטיפולים הופסקו. הלוקמיה חזרה במהירות בעכברים שקיבלו את המעכב, בעוד אלה שטופלו בדגרדר הראו גדילה איטית יותר וחיו זמן ארוך יותר בסך הכל. באופן בולט, MD‑265 לא גרם לאובדן משקל כפי שנצפה בטיפול ממושך במעכב, מה שמרמז על סבילות טובה יותר.
מה זה עשוי להעניק לחולים
לסיכום, הממצאים מראים כי פירוק ישיר של MDM2 יכול להחזיר את כוח הלחימה של p53 ביעילות רבה יותר מאשר חסימתו בלבד, לפחות בתאי AML שעדיין נושאים p53 תקין ותלויים ב‑MDM2 כדי להשקיטו. MD‑265 פעל במנות נמוכות מאוד, פגע בתאי לוקמיה בחוזקה רבה יותר מאשר בתאים מייצרי דם בריאים, נמנע מהעלייה הלא רצויה ב‑MDM2 שגורמות תרופות ישנות והאריך באופן משמעותי את ההישרדות במודלי עכבר שמקורם בדגימות מטופלים. על אף שעבודה זו עדיין לפני‑קלינית ויש לבחון היטב בטיחות והתנגדות בניסויים עתידיים, היא מצביעה על כיוון מבטיח של טיפולים חדשים ללוקמיה הפועלים על ידי פירוק סייענית מרכזית של הסרטן במקום רק להפריע לה.
ציטוט: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
מילות מפתח: לויקמיה מיאלואידית חריפה, p53 ו‑MDM2, מפגע PROTAC, דגרדציה ממוקדת של חלבונים, תאי גזע של לוקמיה