Clear Sky Science · es
Actividad de un degradador PROTAC de MDM2 en células leucémicas primarias y modelos PDX
Nueva esperanza para cánceres sanguíneos difíciles
Muchos adultos diagnosticados con leucemia mieloide aguda (LMA) se enfrentan a opciones limitadas de tratamiento y a una alta probabilidad de recaída. Este estudio explora una estrategia farmacológica de nueva generación que no solo bloquea una proteína impulsora del cáncer, sino que la destruye dentro de las células leucémicas. Al dirigirse a un regulador clave que normalmente mantiene a raya al principal supresor tumoral del organismo, los investigadores muestran una forma de reactivar las defensas celulares contra el cáncer mientras se preserva gran parte de la médula ósea sana.
Cómo la leucemia secuestra un interruptor de seguridad
Nuestras células dependen de una proteína guardiana llamada p53 para pausar el crecimiento celular, reparar el daño en el ADN o desencadenar la muerte celular cuando algo sale muy mal. En muchos cánceres, p53 está mutada y deja de funcionar. En la LMA, sin embargo, p53 a menudo permanece intacta pero está reprimida por otra proteína, MDM2, que etiqueta a p53 para su destrucción. Muchas células leucémicas producen demasiado MDM2, acallando efectivamente el sistema de alarma de p53. Fármacos anteriores intentaron bloquear la interacción entre MDM2 y p53, pero este enfoque tiene una pega: cuando p53 se recupera brevemente, en realidad induce la producción de más MDM2, creando un bucle de retroalimentación que puede limitar la eficacia de esos medicamentos.
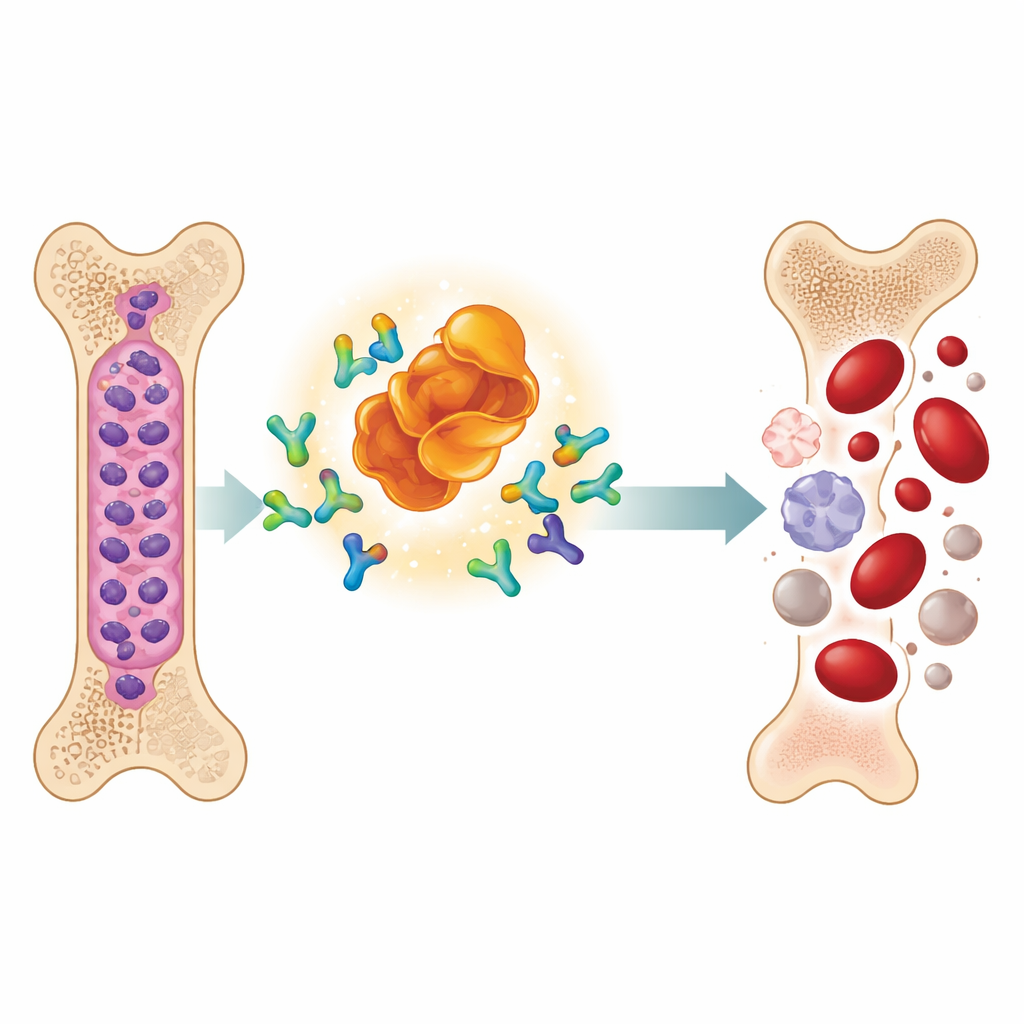
Un nuevo tipo de fármaco que hace desaparecer proteínas cancerosas
El equipo estudió una molécula diseñada llamada MD‑265, parte de una clase creciente de fármacos conocidos como PROTACs. En lugar de simplemente unirse a MDM2 y desactivarlo, MD‑265 actúa como un casamentero molecular. Un extremo se une a MDM2 y el otro recluta un sistema celular natural de eliminación. Esto aproxima a MDM2 con la maquinaria que marca proteínas no deseadas para su degradación, llevando a la célula a deshacerse de MDM2 en lugar de solo bloquearlo. En pruebas de laboratorio con células madre leucémicas tomadas de 100 pacientes con LMA, MD‑265 eliminó las células cancerosas a concentraciones aproximadamente mil veces inferiores a las de un inhibidor convencional de MDM2 basado en el mismo andamio químico. Las muestras de leucemia que respondieron al degradador también tendieron a responder al inhibidor, pero el degradador fue mucho más potente.
Golpeando más fuerte a las células cancerosas que a las sanas
Una preocupación importante con cualquier fármaco contra el cáncer es el daño a tejidos normales, en especial a las células de la médula ósea que generan la sangre sana. Los investigadores compararon cómo afectaba MD‑265 a las células madre leucémicas y a las células madre hematopoyéticas normales de donantes sanos. Las células normales fueron aproximadamente cien veces menos sensibles al degradador que las células leucémicas, lo que sugiere una ventana terapéutica significativa. Cuando el equipo cultivó células en un medio que permite la formación de colonias, MD‑265 redujo drásticamente la formación de colonias en las muestras de LMA sensibles, pero tuvo efectos mucho más leves en las células madre normales. El pequeño grupo de leucemias que resistieron el tratamiento presentaba, por lo general, p53 dañada o producían muy poco MDM2 y su homólogo MDM4, lo que indica qué pacientes podrían no beneficiarse de esta estrategia.
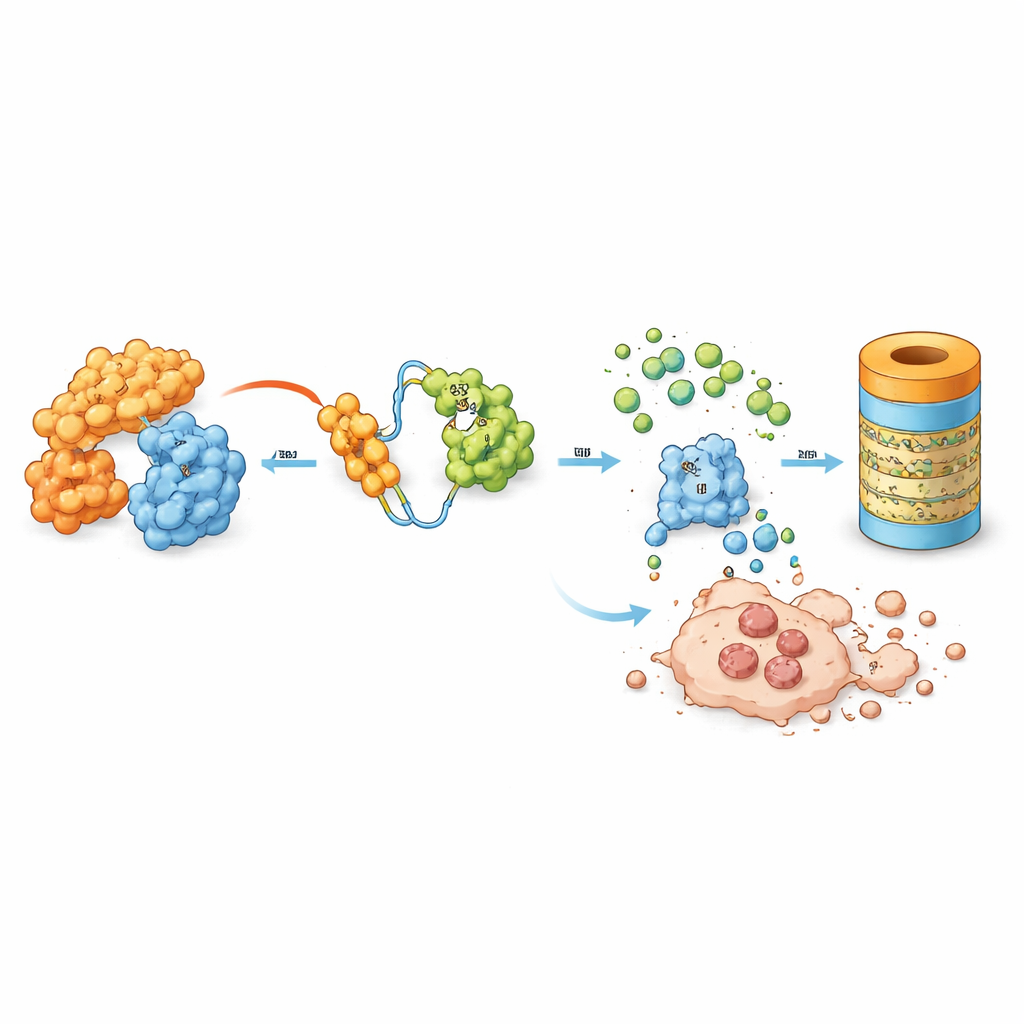
Poniendo a prueba el fármaco en ratones
Para imitar la enfermedad humana más de cerca, los investigadores trasplantaron células madre leucémicas de pacientes en ratones especializados inmunodeficientes, creando modelos de xenoinjerto derivados de pacientes (PDX). Una vez que las células leucémicas humanas se establecieron en la sangre, los ratones fueron tratados con MD‑265, con un potente inhibidor oral de MDM2 que ya está en ensayos clínicos, o con una solución de control. Ambos fármacos redujeron inicialmente la carga leucémica, pero surgieron diferencias importantes con el tiempo. Tras varias semanas, se interrumpió el tratamiento. La leucemia rebrotó rápidamente en los ratones que habían recibido el inhibidor, mientras que aquellos tratados con el degradador mostraron un crecimiento mucho más lento y vivieron más tiempo en general. Es notable que MD‑265 no provocó la pérdida de peso observada con el tratamiento prolongado con el inhibidor, lo que sugiere mejor tolerabilidad.
Qué podría significar esto para los pacientes
En conjunto, los hallazgos muestran que descomponer directamente MDM2 puede reactivar con mayor eficacia el poder antitumoral de p53 que simplemente bloquearlo, al menos en células de LMA que conservan p53 normal y dependen de MDM2 para silenciarlo. MD‑265 funcionó a dosis muy bajas, afectó mucho más a las células leucémicas que a las células hematopoyéticas sanas, evitó el aumento no deseado de MDM2 causado por fármacos anteriores y prolongó significativamente la supervivencia en modelos murinos derivados de muestras de pacientes. Aunque este trabajo sigue siendo preclínico y la seguridad y la resistencia deben estudiarse detenidamente en ensayos futuros, apunta hacia una prometedora nueva clase de tratamientos para la leucemia que actúan desmantelando a un colaborador clave del cáncer en lugar de limitarse a entorpecerlo.
Cita: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
Palabras clave: leucemia mieloide aguda, p53 y MDM2, degradador PROTAC, degradación proteica dirigida, células madre de la leucemia