Clear Sky Science · de
Wirkung eines PROTAC‑MDM2‑Degraders in primären Leukämiezellen und PDX‑Modellen
Neue Hoffnung für schwer behandelbare Blutkrebserkrankungen
Viele Erwachsene, bei denen eine akute myeloische Leukämie (AML) diagnostiziert wird, haben nur begrenzte Therapieoptionen und ein hohes Rückfallrisiko. Diese Studie untersucht eine nächste Generation von Wirkstoffen, die nicht nur ein krebsförderndes Protein blockieren, sondern es innerhalb der Leukämiezellen tatsächlich zerstören. Indem sie einen Schlüsselfaktor ins Visier nimmt, der normalerweise das wichtigste Tumorsuppressor‑Protein des Körpers in Schach hält, zeigen die Forschenden einen Weg, die zellulären Selbstverteidigungsmechanismen gegen Krebs wieder zu aktivieren und gleichzeitig viel des gesunden Knochenmarks zu schonen.
Wie Leukämie einen Sicherheitsschalter kapert
Unsere Zellen sind auf ein Wächterprotein namens p53 angewiesen, das das Zellwachstum anhält, DNA‑Schäden reparieren oder bei schweren Defekten den programmierten Zelltod auslösen kann. In vielen Krebsarten ist p53 selbst verändert und funktioniert nicht mehr. Bei AML ist p53 jedoch häufig intakt, wird aber von einem anderen Protein, MDM2, unterdrückt, das p53 zum Abbau markiert. Viele Leukämiezellen produzieren zu viel MDM2 und dämpfen damit effektiv den Alarmmechanismus von p53. Frühere Medikamente versuchten, die Interaktion zwischen MDM2 und p53 zu blockieren, doch dieser Ansatz hat einen Haken: Wenn p53 kurz wiederhergestellt wird, treibt es die Zellen tatsächlich dazu, mehr MDM2 zu produzieren, wodurch eine eingebaute Rückkopplung entsteht, die die Wirksamkeit solcher Arzneien begrenzen kann.
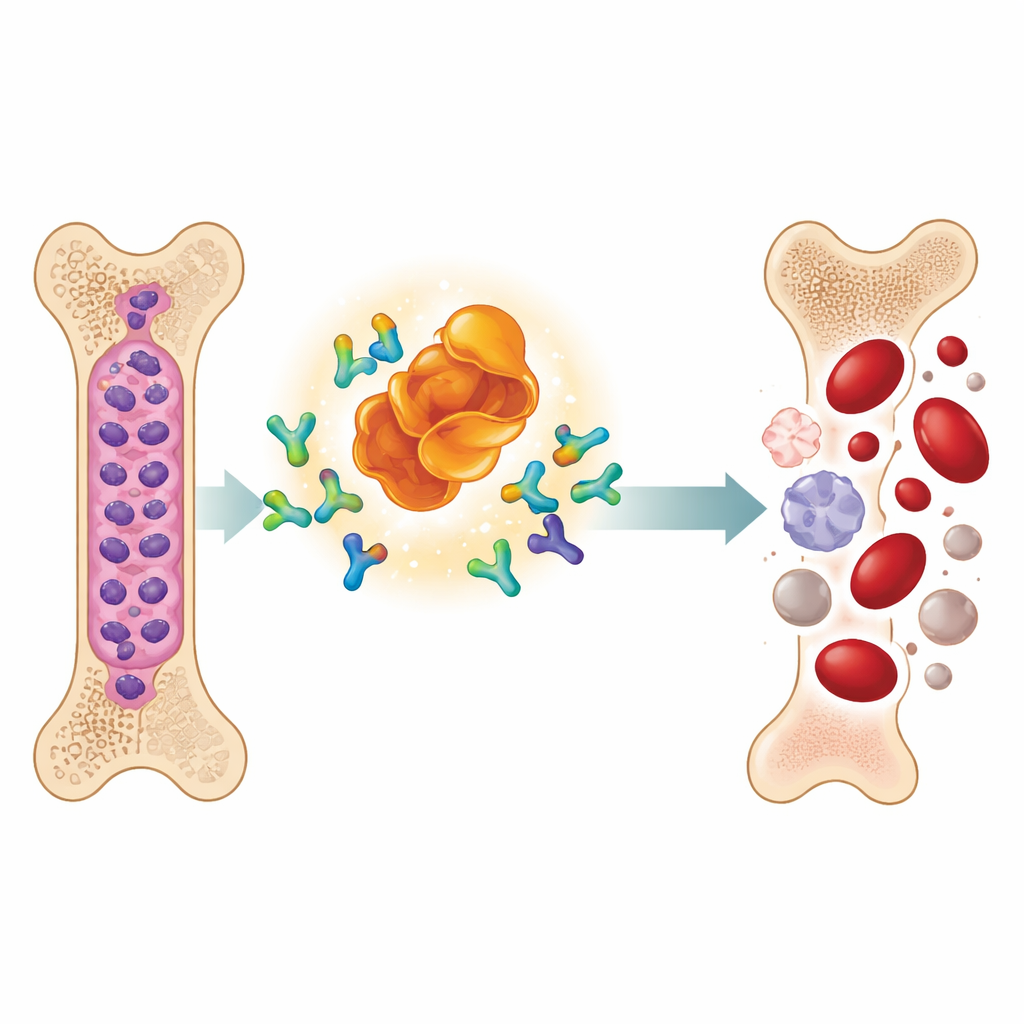
Ein neuer Wirkstofftyp, der Krebsproteine verschwinden lässt
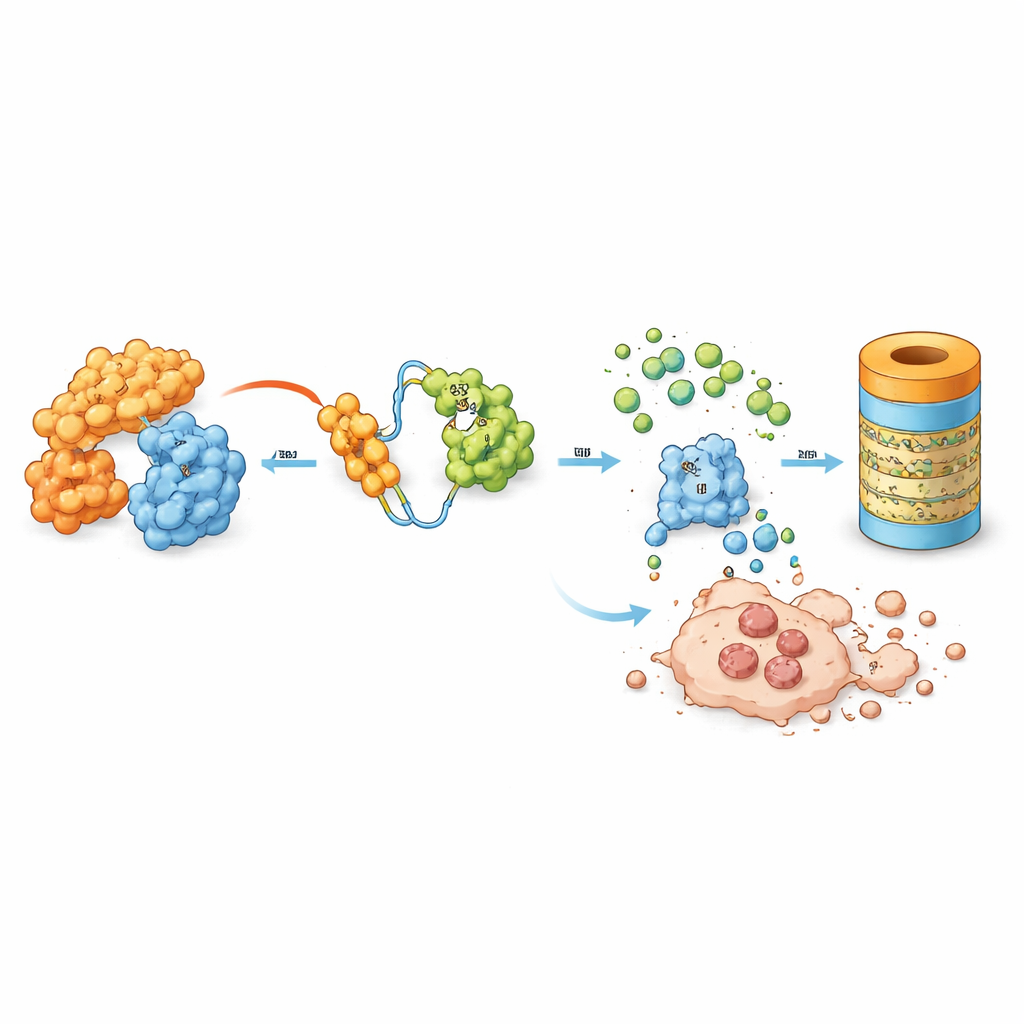
Das Team untersuchte ein konstruiertes Molekül namens MD‑265, das zu einer wachsenden Wirkstoffklasse gehört, die als PROTACs bekannt ist. Anstatt sich nur an MDM2 zu heften und es zu deaktivieren, wirkt MD‑265 wie ein molekularer Kuppler. Ein Ende bindet MDM2, das andere rekrutiert das natürliche zelluläre Entsorgungssystem. So wird MDM2 in die Nähe der Maschinerie gebracht, die unerwünschte Proteine zum Abbau markiert, was dazu führt, dass die Zelle MDM2 zerschreddert, anstatt es lediglich zu blockieren. In Labortests an Leukämie‑Stammzellen von 100 AML‑Patienten tötete MD‑265 Krebszellen bei Konzentrationen, die etwa tausendfach geringer waren als ein herkömmlicher MDM2‑Hemmer, der auf dem gleichen chemischen Gerüst basiert. Leukämieproben, die auf den Degrader ansprachen, reagierten in der Regel auch auf den Inhibitor, doch der Degrader war deutlich wirksamer.
Krebszellen stärker treffen als gesunde Zellen
Ein zentrales Anliegen bei jedem Krebsmedikament ist die Schädigung normaler Gewebe, insbesondere der Knochenmarkszellen, die gesundes Blut bilden. Die Forschenden verglichen, wie MD‑265 Leukämie‑Stammzellen und normale blutbildende Stammzellen gesunder Spender beeinflusst. Normale Zellen waren gegenüber dem Degrader etwa hundertfach weniger empfindlich als Leukämiezellen, was auf ein bedeutsames therapeutisches Fenster hindeutet. In Kulturversuchen, in denen Zellen Kolonien bilden können, verringerte MD‑265 die Koloniebildung in empfindlichen AML‑Proben stark, hatte aber deutlich mildere Effekte auf normale Stammzellen. Die kleine Gruppe von Leukämien, die resistent war, trug meist beschädigtes p53 oder produzierte nur sehr wenig MDM2 und das nahe verwandte MDM4, was Hinweise darauf gibt, welche Patienten von dieser Strategie vermutlich nicht profitieren würden.
Der Wirkstoff im Test an Mäusen
Um die menschliche Erkrankung besser nachzubilden, transplantierten die Forschenden Leukämie‑Stammzellen von Patientinnen und Patienten in speziell immundefiziente Mäuse und erzeugten so patientenabgeleitete Xenograft‑(PDX‑)Modelle. Sobald sich menschliche Leukämiezellen im Blut etabliert hatten, wurden die Mäuse entweder mit MD‑265, mit einem bereits klinisch geprüften, starken oralen MDM2‑Inhibitor oder mit einer Kontrolllösung behandelt. Beide Wirkstoffe verringerten zunächst die Leukämielast, doch im Zeitverlauf zeigten sich wichtige Unterschiede. Nach mehreren Wochen wurde die Behandlung gestoppt. Bei den Mäusen, die den Inhibitor erhalten hatten, setzte die Leukämie schnell wieder ein, während diejenigen, die mit dem Degrader behandelt worden waren, deutlich langsamer nachwuchsen und insgesamt länger überlebten. Bemerkenswert war, dass MD‑265 nicht den Gewichtsverlust verursachte, der bei länger andauernder Inhibitorbehandlung beobachtet wurde, was auf eine bessere Verträglichkeit hindeutet.
Was das für Patienten bedeuten könnte
Insgesamt zeigen die Ergebnisse, dass der direkte Abbau von MDM2 p53s tumorbekämpfende Funktion effektiver reaktivieren kann als eine bloße Blockade, zumindest in AML‑Zellen, die noch normales p53 tragen und auf MDM2 angewiesen sind, um es zu unterdrücken. MD‑265 wirkte in sehr niedrigen Dosen, traf Leukämiezellen deutlich stärker als gesunde blutbildende Zellen, vermied den unerwünschten MDM2‑Anstieg, den ältere Wirkstoffe hervorrufen, und verlängerte in Mausmodellen aus Patientenproben das Überleben signifikant. Zwar ist diese Arbeit noch präklinisch und Sicherheit sowie Resistenzmechanismen müssen in künftigen Studien sorgfältig untersucht werden, doch sie weist auf eine vielversprechende neue Klasse von Leukämietherapien hin, die durch den Abbau eines wichtigen Krebshelfers wirken, anstatt ihm nur entgegenzuwirken.
Zitation: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
Schlüsselwörter: akute myeloische Leukämie, p53 und MDM2, PROTAC‑Degrader, gezielte Proteinabbau, Leukämie‑Stammzellen