Clear Sky Science · it
Attività del degradatore PROTAC di MDM2 in cellule leucemiche primarie e modelli PDX
Una nuova speranza per i tumori del sangue difficili
Molti adulti diagnosticati con leucemia mieloide acuta (LMA) affrontano opzioni terapeutiche limitate e un alto rischio di recidiva. Questo studio esplora una strategia farmacologica di nuova generazione che non si limita a bloccare una proteina che guida il cancro, ma la distrugge all’interno delle cellule leucemiche. Mirando a un regolatore chiave che normalmente tiene sotto controllo il principale soppressore tumorale dell’organismo, i ricercatori mostrano un modo per riattivare le difese cellulari contro il cancro preservando gran parte del midollo osseo sano.
Come la leucemia dirotta un interruttore di sicurezza
Le nostre cellule dipendono da una proteina guardiana chiamata p53 per fermare la crescita cellulare, riparare il DNA danneggiato o innescare il suicidio cellulare quando qualcosa va storto. In molti tumori p53 è mutata e non funziona più. Nella LMA, tuttavia, p53 è spesso ancora intatta ma viene repressa da un’altra proteina, MDM2, che segnala p53 per la distruzione. Molte cellule leucemiche producono troppo MDM2, silenziando di fatto il sistema d’allarme di p53. Farmaci precedenti hanno cercato di bloccare l’interazione fra MDM2 e p53, ma questo approccio ha un limite: quando p53 recupera brevemente attività, induce a sua volta la produzione di più MDM2, creando un circuito di retroazione che può ridurre l’efficacia di questi medicinali.
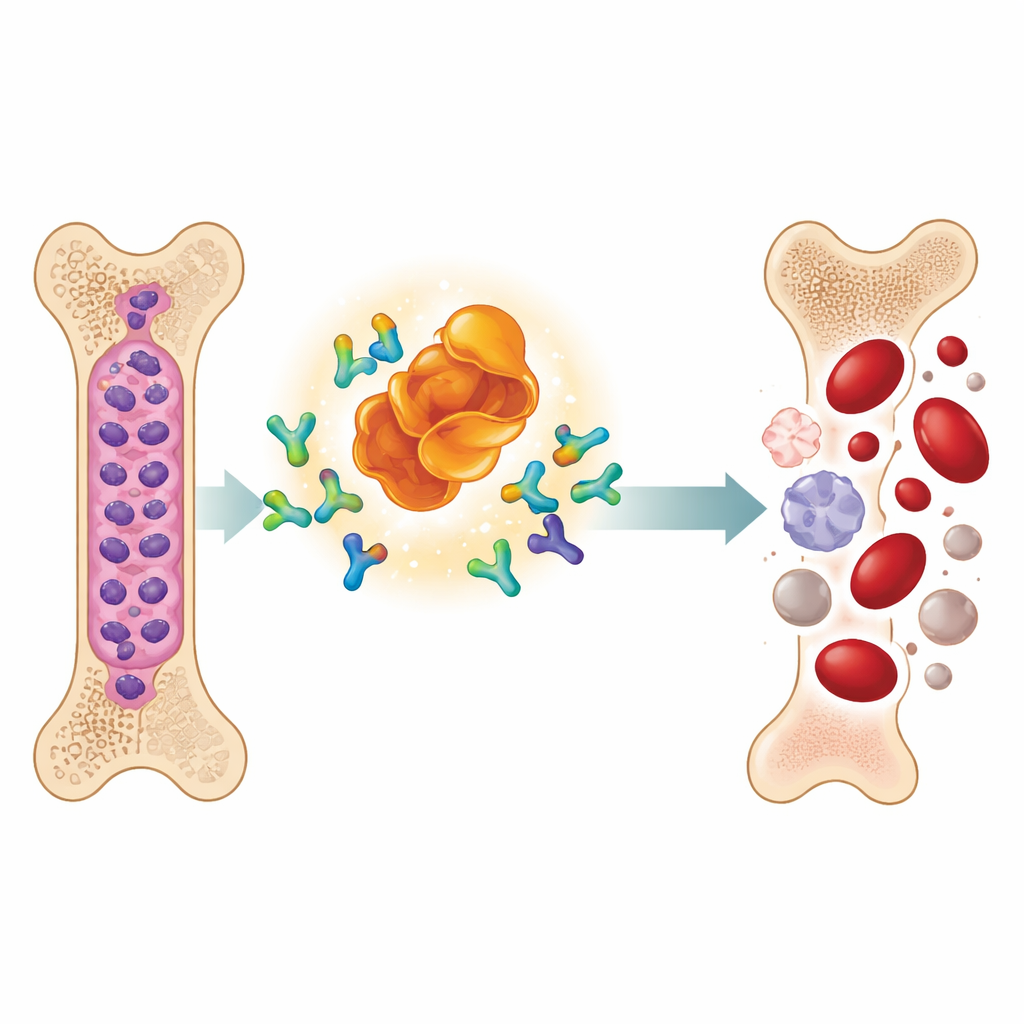
Un nuovo tipo di farmaco che fa sparire le proteine cancerose
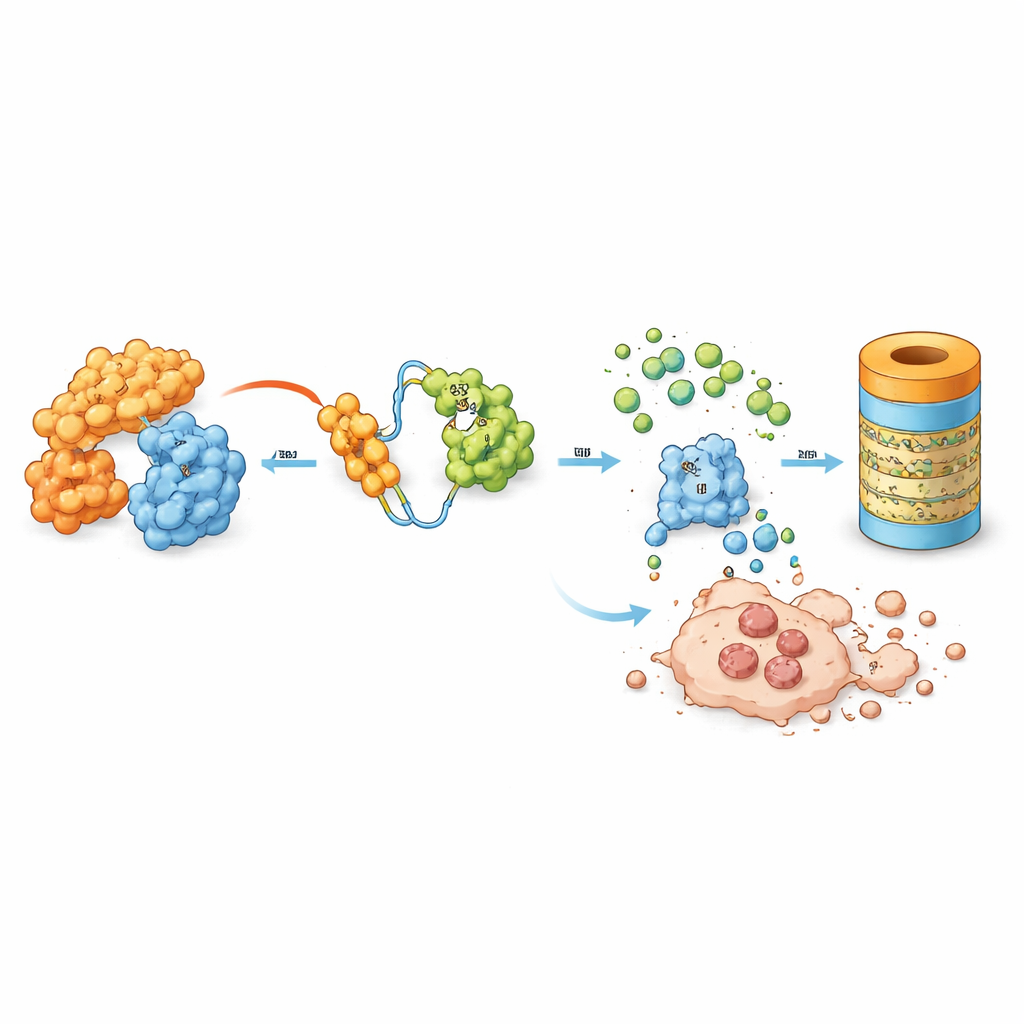
Il team ha studiato una molecola progettata chiamata MD-265, parte di una classe crescente di farmaci nota come PROTAC. Invece di limitarsi ad attaccarsi a MDM2 e disabilitarla, MD-265 agisce come un mediatore molecolare. Un’estremità si lega a MDM2, l’altra recluta un sistema naturale di smaltimento cellulare. Questo avvicina MDM2 alla macchina che marca le proteine indesiderate per la degradazione, portando la cellula a scomporre MDM2 invece di semplicemente bloccarla. Nei test in laboratorio su cellule staminali leucemiche prelevate da 100 pazienti con LMA, MD-265 ha ucciso le cellule tumorali a concentrazioni circa mille volte inferiori rispetto a un inibitore tradizionale di MDM2 costruito sullo stesso impalcatura chimica. I campioni leucemici che rispondevano al degradatore tendevano anche a rispondere all’inibitore, ma il degradatore era di gran lunga più potente.
Colpire le cellule tumorali più duramente che quelle sane
Una preoccupazione importante per qualsiasi farmaco oncologico è il danno ai tessuti normali, in particolare alle cellule del midollo osseo che producono il sangue sano. I ricercatori hanno confrontato come MD-265 influenzava le cellule staminali leucemiche e le cellule staminali ematopoietiche normali di donatori sani. Le cellule normali risultavano circa cento volte meno sensibili al degradatore rispetto alle cellule leucemiche, suggerendo una finestra terapeutica significativa. Quando il team ha coltivato le cellule in piastre per valutare la formazione di colonie, MD-265 ha ridotto drasticamente la formazione di colonie nei campioni di LMA sensibili ma ha avuto effetti molto più lievi sulle cellule staminali normali. Il piccolo gruppo di leucemie resistenti al trattamento presentava in genere p53 danneggiata o produceva pochissimo MDM2 e il suo partner MDM4, evidenziando quali pazienti potrebbero non beneficiare di questa strategia.
Mettere il farmaco alla prova nei topi
Per imitare più da vicino la malattia umana, gli investigatori hanno trapiantato cellule staminali leucemiche dei pazienti in topi specializzati immunodeficienti, creando modelli xenotrapiantati derivati da pazienti (PDX). Una volta che le cellule leucemiche umane si erano stabilite nel sangue, i topi sono stati trattati con MD-265, con un potente inibitore orale di MDM2 già in studi clinici, o con una soluzione di controllo. Entrambi i farmaci hanno inizialmente ridotto il carico leucemico, ma sono emerse differenze rilevanti nel tempo. Dopo alcune settimane il trattamento è stato interrotto. La leucemia è ricomparsa rapidamente nei topi trattati con l’inibitore, mentre quelli trattati con il degradatore hanno mostrato una ricrescita molto più lenta e una sopravvivenza complessiva maggiore. È notevole che MD-265 non abbia causato la perdita di peso osservata con il trattamento prolungato con l’inibitore, suggerendo una migliore tollerabilità.
Cosa potrebbe significare per i pazienti
Nel complesso, i risultati mostrano che degradare direttamente MDM2 può riattivare più efficacemente la potenza antitumorale di p53 rispetto al semplice blocco, almeno nelle cellule di LMA che conservano p53 normale e dipendono da MDM2 per silenziarla. MD-265 ha funzionato a dosi molto basse, ha colpito le cellule leucemiche molto più duramente rispetto alle cellule ematopoietiche sane, ha evitato il rialzo indesiderato di MDM2 causato dai farmaci più vecchi e ha esteso significativamente la sopravvivenza nei modelli murini derivati da campioni di pazienti. Sebbene questo lavoro sia ancora preclinico e sicurezza e resistenza debbano essere studiate attentamente in futuri trial, indica una promettente nuova classe di terapie per la leucemia che agiscono smantellando un aiutante chiave del cancro piuttosto che limitarsi a ostacolarlo.
Citazione: Kandarpa, M., Peterson, L.F., Potu, H. et al. Activity of PROTAC MDM2 degrader in primary leukemia cells and PDX models. Leukemia 40, 918–924 (2026). https://doi.org/10.1038/s41375-026-02957-8
Parole chiave: leucemia mieloide acuta, p53 e MDM2, degradatore PROTAC, degradazione proteica mirata, cellule staminali leucemiche