Clear Sky Science · tr
Bağlantılı MS-genomik ve dil/dönüştürücü tabanlı modellerle doğal ürün keşfini hızlandırmak
Neden yeni ilaçlar göz önünde saklıdır
Antibiyotikler ve kanser ilaçları da dahil olmak üzere en önemli ilaçlarımızın birçoğu, karmaşık doğal kimyasallar üreten küçük mikroplardan geliyor. Ancak bu gizli eczanelerde yeni moleküller bulmak yavaş ve pahalı; çünkü araştırmacılar devasa mikroorganizma kütüphanelerini taramak ve hangilerinin denenmeye değer olduğunu tahmin etmek zorunda. Bu makale, gelişmiş yapay zekâyla modern laboratuvar ölçümlerinin birleşiminin arayışı nasıl büyük ölçüde hızlandırabileceğini gösteriyor; araştırmacıların zahmetli deneylere başlamadan önce en umut verici mikroplara odaklanmasını sağlıyor. 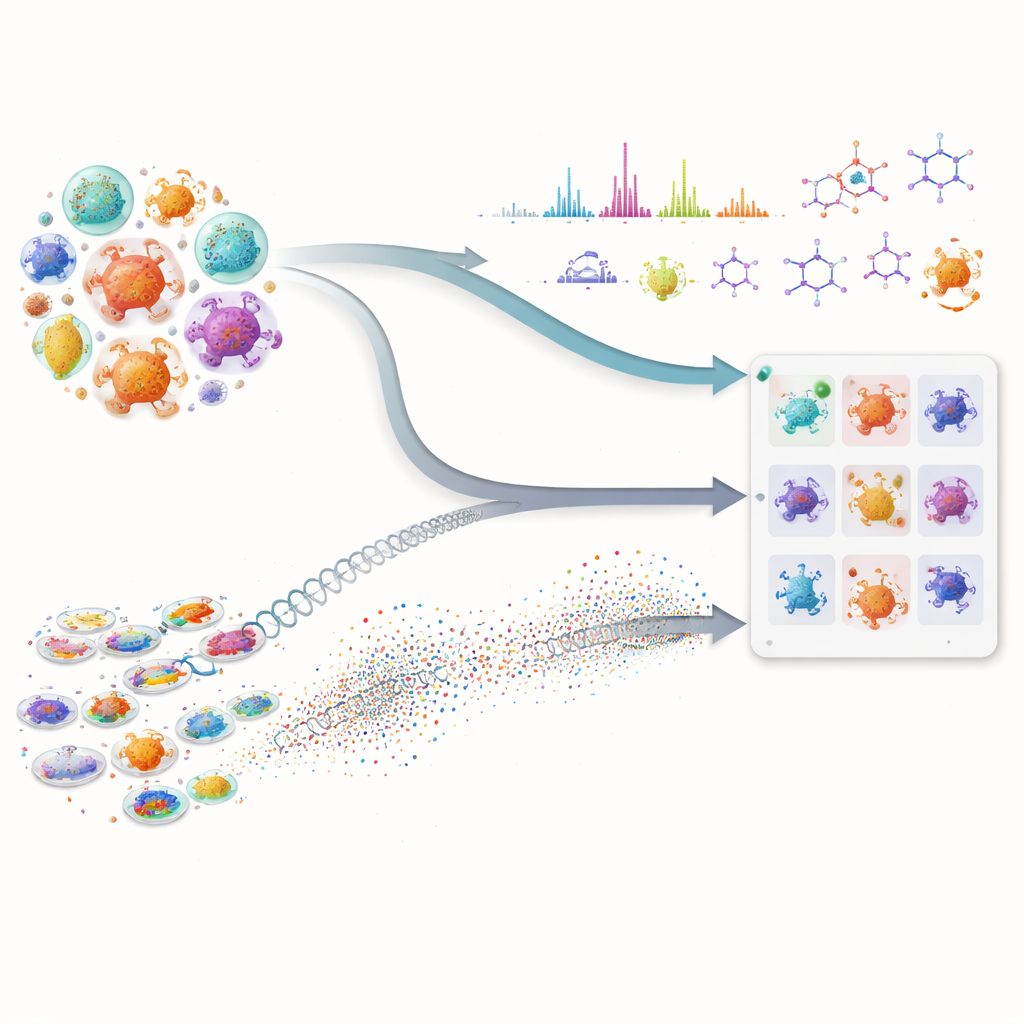
Mikrop DNA’sını aranabilir bir haritaya dönüştürmek
Yöntemin ilk kısmı mikropların genetik “planlarına” bakıyor. Yalnızca geleneksel DNA eşleştirmeye dayanmak yerine ekip, milyonlarca protein dizisi üzerinde desenler öğrenmiş güçlü protein dil modellerini uyguluyor. Bu modeller her biyosentetik proteini yüksek boyutlu sayısal bir parmak izine çeviriyor. Bu, altındaki DNA büyük ölçüde değişmiş veya kaba taslak genomlarda sık görüldüğü gibi parçalara ayrılmış olsa bile uzak işlevsel akrabaların tespit edilmesine olanak tanıyor. Araştırmacılar sonra her mikrobu, hedef bir molekülü yapmak için bilinen bir yoldaki proteinlere ne kadar çok benzediği ve bu benzerliğin ne kadar güçlü olduğu temelinde puanlıyor. Bu bileşik puan, yalnızca bir veya iki ortak, uzmanlaşmamış enzime sahip mikropları göz ardı ederken, birleşik protein seti istenen bileşiği oluşturabilecek gibi görünen suşları öne çıkarıyor.
Yapay zekâ ile karmaşık kimyasal karışımları okumak
İkinci kısım laboratuvarda mikropların gerçekte ne ürettiğine odaklanıyor. Sıvı kromatografisi ve tandem kütle spektrometrisi kullanılarak, fermantasyon özlerinin içindeki moleküllerin ayrıntılı “parmak izleri” kaydediliyor. Yazarların dahili Akıllı Yapısal Aydınlatma İş Akışı (WISE) bu sinyalleri temizliyor, örtüşen pikleri ayırıyor ve ardından her spektruma en iyi uyan moleküler şekilleri tahmin etmek için milyonlarca doğal ürün-benzeri yapı üzerinde eğitilmiş yapay zekâ modellerini kullanıyor. Bir dönüştürücü tabanlı model aday moleküllerin spektroskopik görünümlerinin nasıl olması gerektiğini tahmin ediyor ve gözlemlenen ile tahmin edilen desenlerin ne kadar iyi örtüştüğünü, izotopik düzenler ve kesin kütle gibi ince ayrıntıları da içerecek şekilde ağırlıklandıran birleşik bir puan kullanılıyor. Bu puanların standart bir kıyaslamadaki dağılımını analiz ederek, ekip gerçek eşleşmeleri gürültüden veya benzer görünümlü aldatmacalardan ayıran eşik değerleri belirliyor; bu, bazı yapısal tahminleri yüksek güvenle etiketlemeye ve açıkça yanlış olanları filtrelemeye izin veriyor.
Genleri ve kimyasalları bir araya getirmek
Yöntemin gerçek gücü bu iki bilgi akışını birleştirmekten geliyor. İlgi duyulan herhangi bir molekül için bir mikrop, yalnızca hem genetik potansiyel gösteriyorsa—proteinleri bilinen bir yolun proteinlerine benziyorsa—hem de kimyasal kanıt sunuyorsa—ürettiği spektral özellikler beklenen yapıya uyuyorsa listenin başına yükseliyor. Bu çapraz doğrulama, yalnızca bir tür veride ikna edici görünen yanlış ipuçlarını azaltıyor. Yazarlar, çerçevelerini büyük bir aktinobakteriyel suş ve mutant koleksiyonunda test etti ve valinomisin, surfaktin ve antibiyotik neomisin B olmak üzere birbirinden çok farklı üç antimikrobiyal bileşiğe odaklandı. Sistem, kusursuz genomlara veya eksiksiz spektral kütüphanelere dayanmak yerine, verilerin dağınık veya eksik olduğu durumlarda bile iyi çalışıyor; bu, erken aşama keşif kampanyalarında sık karşılaşılan bir gerçekliktir. 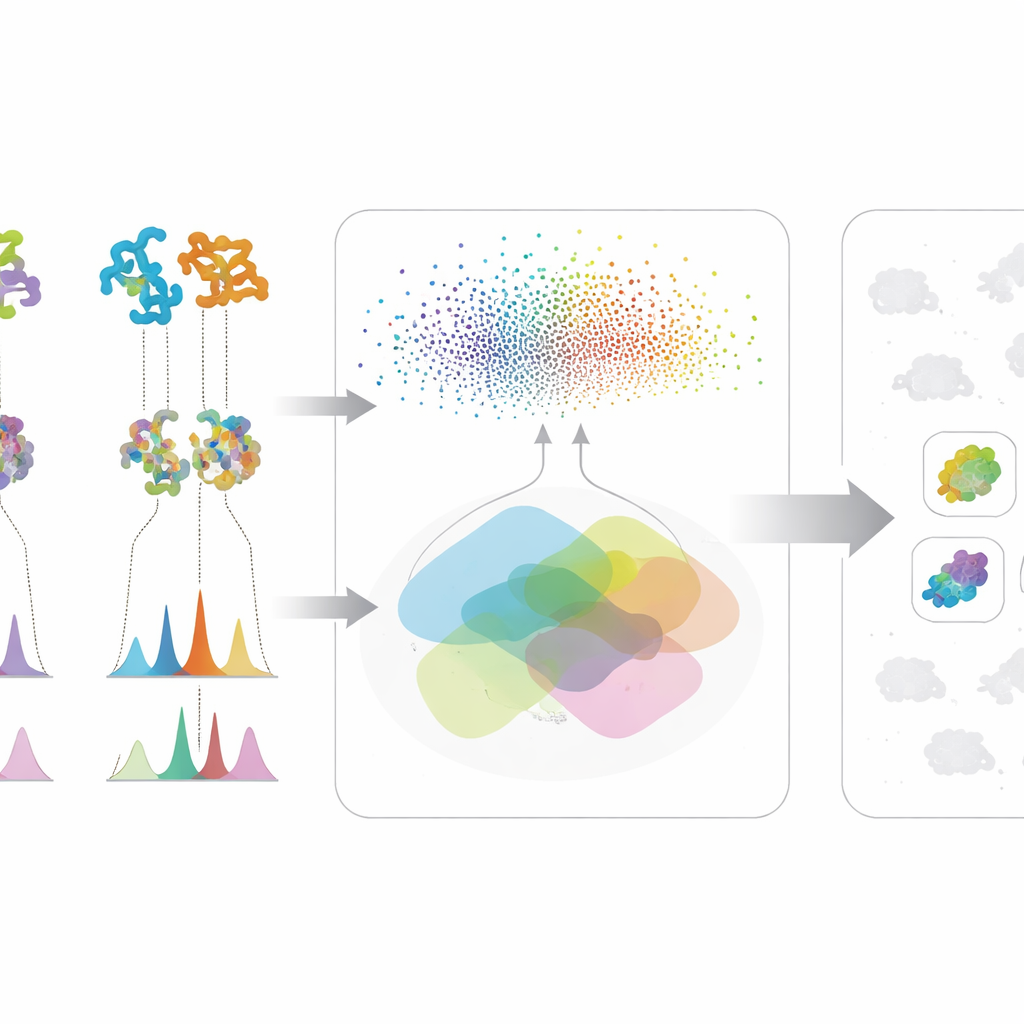
Çerçeveyi teste tabi tutmak
Neomisin B vaka çalışmasında, yapay zekâ önce proteinleri bilinen neomisin yolundakilere benzeyen mikropları aradı, sonra bunların kütle spektrumlarının neomisin-benzeri moleküllerin varlığına işaret edip etmediğini kontrol etti. Dört suş her iki filtreden de geçti; bunların üçü deneysel olarak neomisin B ürettiği doğrulandı ve bunların ikisi daha önce tanınmamış üreticilerdi. Valinomisin ve surfaktin için de çerçeve yüksek doğrulukla üreticileri belirledi; rasgele puanları karıştıran kontrol testi ise çok daha kötü performans gösterdi. Bu sonuçlar, modelin verilerdeki rastgele tesadüflerden ziyade gerçek biyolojik ilişkileri yakaladığını ve araştırmacıları yoğun bir arama alanında en olası hedeflere yönlendirebileceğini gösteriyor.
Gelecekteki ilaç keşfi için ne anlama geliyor
Günlük anlatımla, yazarlar doğal ürün keşfi için akıllı bir öneri motoru inşa ettiler. Her mikrobu ve her kimyasal sinyali kaba kuvvetle test etmek yerine, bilim insanları artık genetik potansiyel ve kimyasal çıktı uyum gösteren kısa bir suş listesine odaklanabilir. Bu, boşa harcanan çabayı büyük ölçüde azaltırken, hâlâ herhangi bir referans kitapta olmayan beklenmedik molekülleri keşfetmeye yer bırakıyor. Yapay zekâ modelleri ve veri setleri geliştikçe, bu tür entegre genomik ve metabolomik akıl yürütme, keşfedilmemiş geniş mikrobiyal kimya bölgelerinin kilidini açabilir ve toplumun en çok ihtiyaç duyduğu anda yeni antibiyotikler ve diğer faydalı bileşenleri ortaya çıkarabilir.
Atıf: Tay, D.W.P., Koh, W., Ang, S.J. et al. Accelerating natural product discovery with linked MS-genomics and language/transformer-based models. npj Antimicrob Resist 4, 31 (2026). https://doi.org/10.1038/s44259-026-00206-7
Anahtar kelimeler: doğal ürün keşfi, mikrobiyal metabolitler, kütle spektrometrisi, protein dil modelleri, ilaç keşfinde yapay zeka