Clear Sky Science · es
Acelerando el descubrimiento de productos naturales con MS-genómica vinculada y modelos de lenguaje/transformer
Por qué los nuevos medicamentos se esconden a simple vista
Muchos de nuestros medicamentos más importantes, incluidos antibióticos y fármacos contra el cáncer, provienen de microbios diminutos que producen químicos naturales complejos. Sin embargo, encontrar nuevas moléculas en esta farmacia oculta es lento y costoso, porque los científicos deben revisar enormes bibliotecas de microbios y adivinar cuáles merecen pruebas. Este trabajo demuestra que combinar inteligencia artificial avanzada con mediciones de laboratorio modernas puede acelerar en gran medida la búsqueda, ayudando a los investigadores a centrarse en los microbios más prometedores antes de realizar experimentos laboriosos. 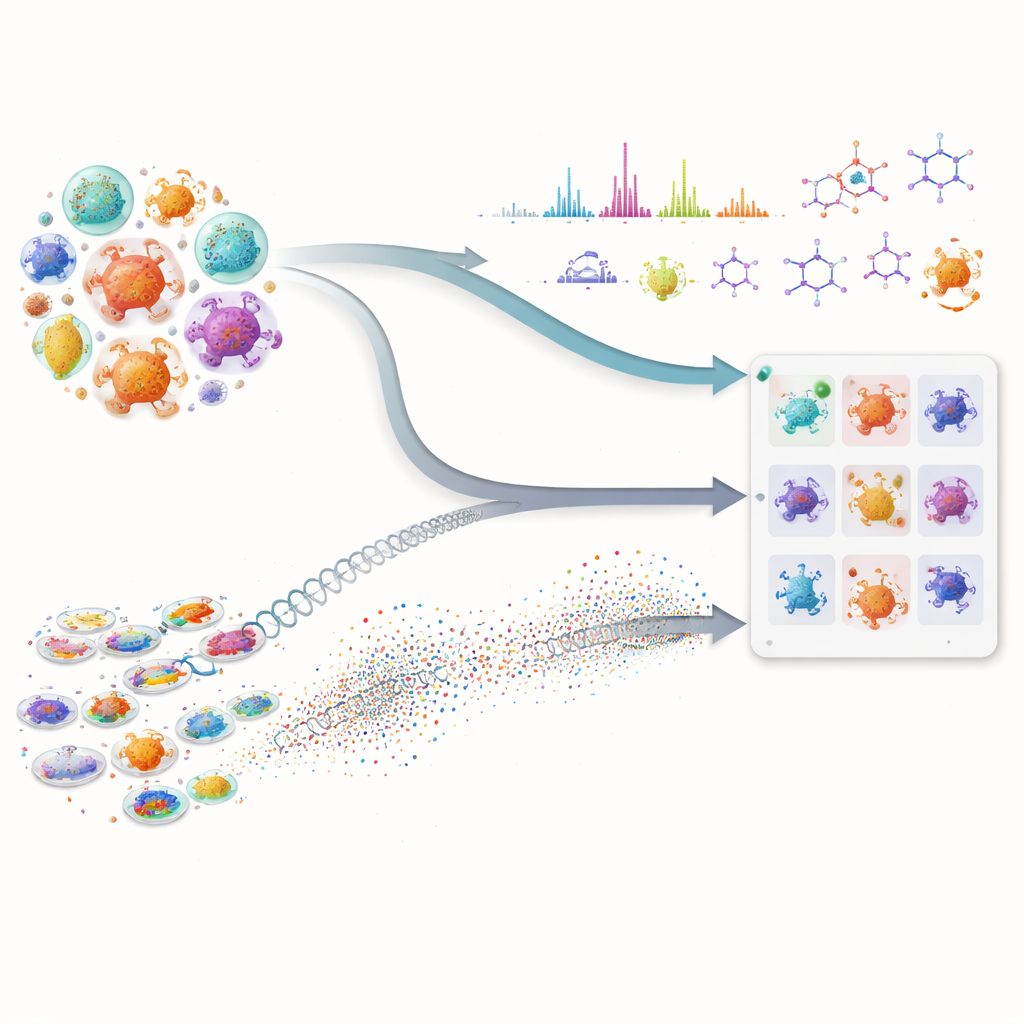
Convertir el ADN microbiano en un mapa buscable
La primera parte del enfoque examina los “planos” genéticos de los microbios. En lugar de usar solo el emparejamiento de ADN tradicional, el equipo aplica potentes modelos de lenguaje para proteínas—sistemas de IA que han aprendido patrones a partir de millones de secuencias proteicas. Estos modelos convierten cada proteína biosintética en una huella numérica de alta dimensión. Eso permite detectar parientes funcionales lejanos incluso cuando el ADN subyacente ha cambiado mucho o está fragmentado, un problema común con genomas en borrador. Los investigadores puntúan luego cada microbio según cuántas de sus proteínas se parecen a las de una vía conocida para fabricar una molécula objetivo y según lo fuerte que es esa similitud en conjunto. Esta puntuación compuesta resalta cepas cuyo conjunto combinado de proteínas parece capaz de construir el compuesto deseado, a la vez que descarta microbios que solo tienen una o dos enzimas comunes y no especializadas.
Leer mezclas químicas complejas con IA
La segunda parte se centra en lo que los microbios realmente producen en el laboratorio. Usando cromatografía líquida y espectrometría de masas en tándem, los científicos registran huellas detalladas de las moléculas en caldos de fermentación. El flujo de trabajo propio de los autores para la Elucidación Estructural Inteligente, o WISE, limpia estas señales, separa picos superpuestos y luego utiliza modelos de IA entrenados con millones de estructuras similares a productos naturales para estimar qué formas moleculares se ajustan mejor a cada espectro. Un modelo basado en transformers predice cómo deberían verse los espectros de moléculas candidatas, y una puntuación combinada valora cuán bien coinciden los patrones observados y predichos, incluyendo detalles finos como patrones isotópicos y masa exacta. Al analizar cómo se distribuyen estas puntuaciones en un referente estándar, el equipo identifica umbrales que separan coincidencias probablemente reales del ruido o los señuelos parecidos, lo que les permite etiquetar algunas conjeturas estructurales como de alta confianza y filtrar las claramente erróneas.
Unir genes y químicos
El verdadero poder del método surge al fusionar estas dos corrientes de información. Para cualquier molécula de interés, un microbio asciende en la lista solo si muestra tanto potencial genético—sus proteínas se parecen a las de una vía conocida—como evidencia química—produce características espectrales que encajan con la estructura esperada. Esta verificación cruzada reduce las falsas pistas que parecen convincentes en un solo tipo de dato. Los autores probaron su marco en una gran colección de cepas y mutantes actinobacterianos, centrándose en tres compuestos antimicrobianos muy diferentes: valinomicina, surfactina y el antibiótico neomicina B. En lugar de depender de genomas perfectos o bibliotecas espectrales completas, el sistema funciona bien incluso cuando los datos son desordenados o incompletos, una realidad común en campañas de descubrimiento en etapas tempranas. 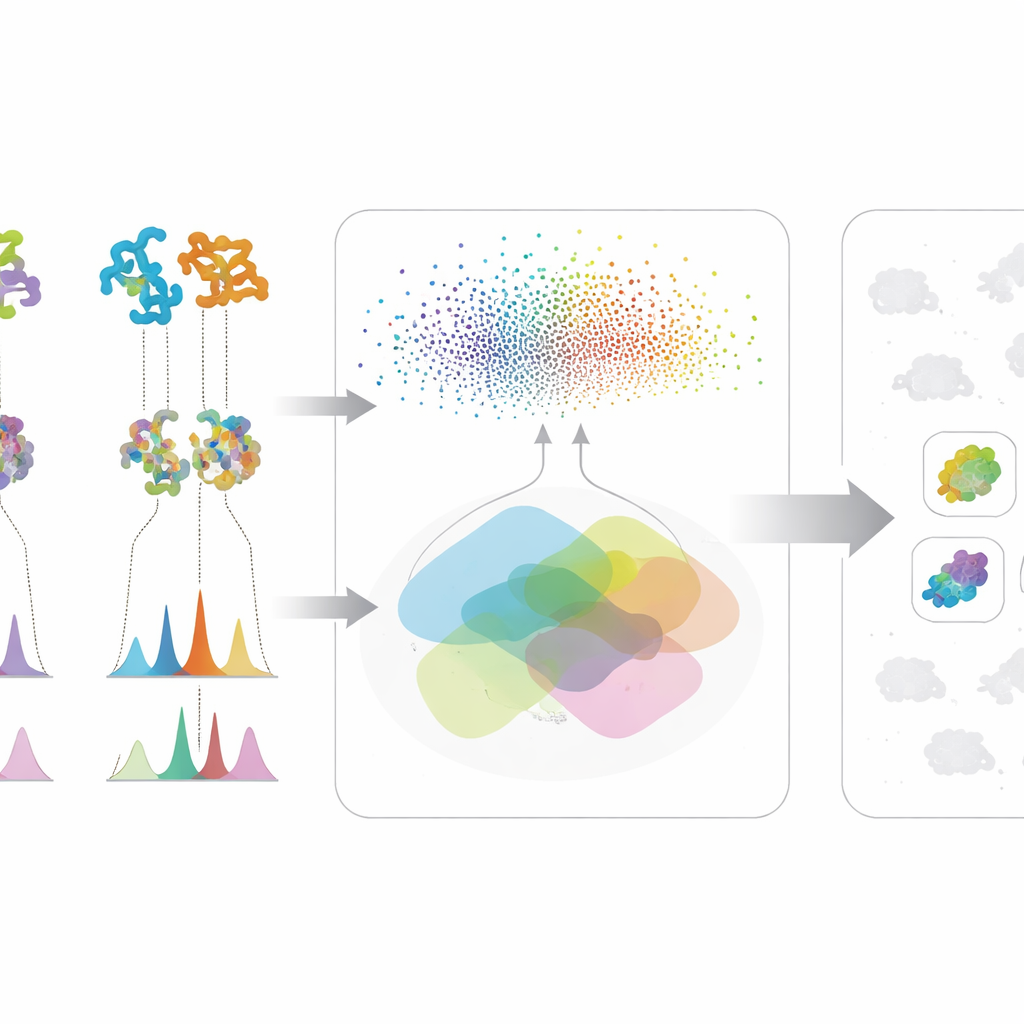
Poner el marco a prueba
En el estudio de caso de neomicina B, la IA buscó primero microbios cuyas proteínas se parecieran a las de la vía conocida de neomicina y luego comprobó si sus espectros de masas sugerían la presencia de moléculas similares a la neomicina. Cuatro cepas superaron ambos filtros; tres de ellas se confirmaron experimentalmente como productoras de neomicina B, incluidas dos productoras no reconocidas previamente. Para valinomicina y surfactina, el marco también identificó productores con alta precisión, mientras que una prueba de control que barajó aleatoriamente las puntuaciones tuvo un rendimiento mucho peor. Estos resultados muestran que el modelo captura relaciones biológicas reales, no solo coincidencias aleatorias en los datos, y que puede guiar con éxito a los investigadores hacia los aciertos más probables en un espacio de búsqueda saturado.
Qué significa esto para el descubrimiento futuro de fármacos
En términos prácticos, los autores han construido un motor de recomendación inteligente para el descubrimiento de productos naturales. En lugar de probar cada microbio y cada señal química de forma exhaustiva, los científicos pueden ahora centrarse en una lista corta de cepas donde el potencial genético y la producción química coinciden. Esto reduce enormemente el esfuerzo desperdiciado, al tiempo que deja espacio para descubrir moléculas inesperadas que aún no figuran en ningún manual de referencia. A medida que los modelos de IA y los conjuntos de datos sigan mejorando, este tipo de razonamiento integrado genómico y metabolómico podría desbloquear vastas regiones de la química microbiana que aún no se han explorado, revelando potencialmente nuevos antibióticos y otros compuestos útiles justo cuando la sociedad más los necesita.
Cita: Tay, D.W.P., Koh, W., Ang, S.J. et al. Accelerating natural product discovery with linked MS-genomics and language/transformer-based models. npj Antimicrob Resist 4, 31 (2026). https://doi.org/10.1038/s44259-026-00206-7
Palabras clave: descubrimiento de productos naturales, metabolitos microbianos, espectrometría de masas, modelos de lenguaje para proteínas, IA en el descubrimiento de fármacos