Clear Sky Science · de
Beschleunigte Entdeckung natürlicher Produkte durch verknüpfte MS-Genomik und sprach-/Transformer-basierte Modelle
Warum neue Medikamente offen sichtbar sind
Viele unserer wichtigsten Medikamente, darunter Antibiotika und Krebsmedikamente, stammen von winzigen Mikroben, die komplexe natürliche Verbindungen herstellen. Die Suche nach neuen Molekülen in dieser verborgenen Apotheke ist jedoch langsam und teuer, weil Forschende riesige Mikrobenbibliotheken durchsieben und erraten müssen, welche Kandidaten eine genauere Prüfung wert sind. Diese Arbeit zeigt, dass die Kombination fortschrittlicher künstlicher Intelligenz mit modernen Labormessungen die Suche erheblich beschleunigen kann, indem sie Forschenden ermöglicht, vielversprechende Mikroben gezielt auszuwählen, bevor aufwändige Experimente durchgeführt werden. 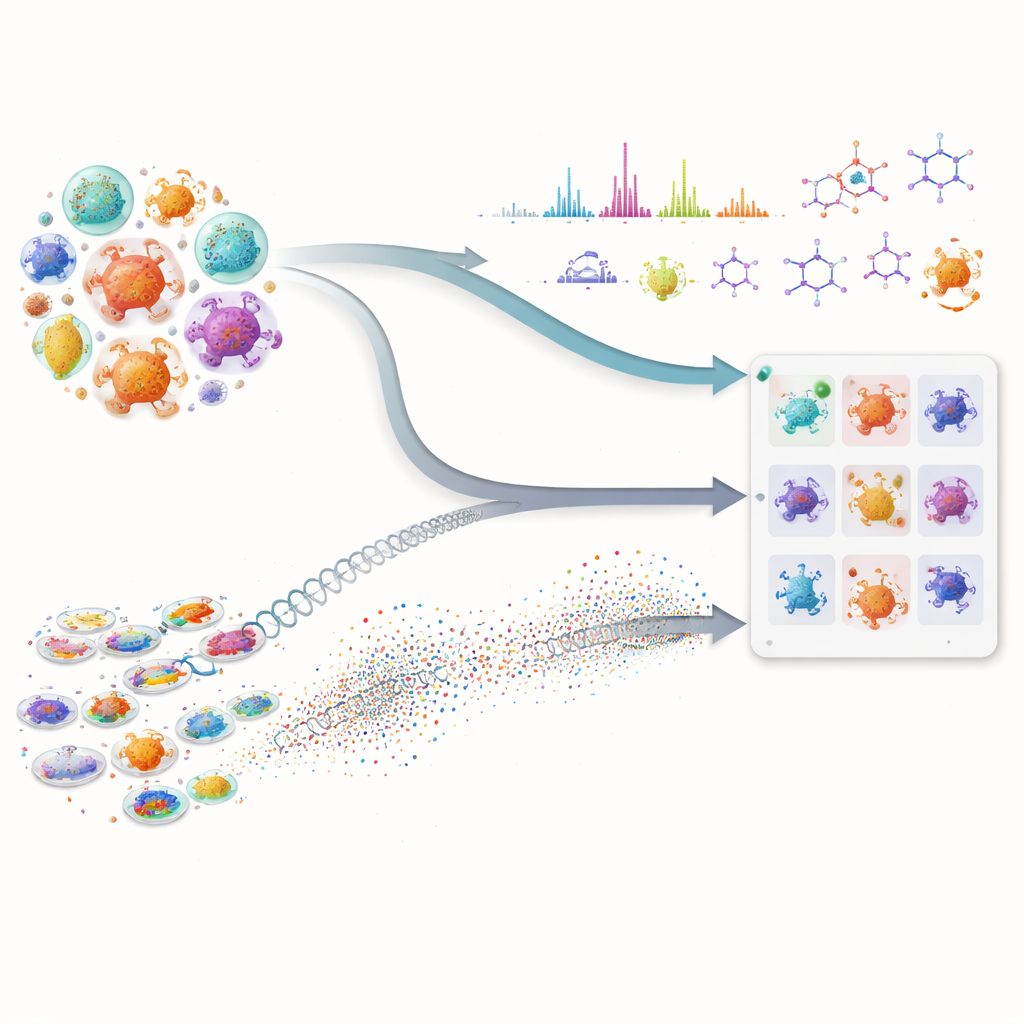
Die DNA von Mikroben in eine durchsuchbare Karte verwandeln
Der erste Teil des Ansatzes betrachtet die genetischen „Baupläne“ der Mikroben. Statt ausschließlich traditionelle DNA-Abgleiche zu verwenden, setzt das Team mächtige Protein-Sprachmodelle ein — KI-Systeme, die Muster in Millionen von Proteinsequenzen gelernt haben. Diese Modelle wandeln jedes biosynthetische Protein in einen hochdimensionalen numerischen Fingerabdruck um. Dadurch können Forschende entfernte funktionelle Verwandte erkennen, selbst wenn die zugrundeliegende DNA stark verändert ist oder über Fragmenten verteilt vorliegt — ein häufiges Problem bei unvollständigen Genomen. Die Forschenden bewerten dann jede Mikrobe danach, wie viele ihrer Proteine denen in einem bekannten Weg zur Herstellung eines Zielmoleküls ähneln und wie stark diese Gesamtähnlichkeit ist. Diese zusammengesetzte Bewertung hebt Stämme hervor, deren kombiniertes Proteinspektrum danach aussieht, als könnte es die gewünschte Verbindung herstellen, während Mikroben, die nur ein oder zwei verbreitete, nicht spezialisierte Enzyme besitzen, herabgestuft werden.
Komplexe chemische Gemische mit KI lesen
Der zweite Teil konzentriert sich darauf, was die Mikroben tatsächlich im Labor produzieren. Mittels Flüssigkeitschromatographie und Tandem-Massenspektrometrie zeichnen Forschende detaillierte „Fingerabdrücke“ der Moleküle in Fermentationsbrühen auf. Der hausinterne Workflow for Intelligent Structural Elucidation (WISE) der Autoren bereinigt diese Signale, trennt überlappende Peaks und verwendet anschließend KI-Modelle, die auf Millionen naturproduktähnlicher Strukturen trainiert wurden, um abzuschätzen, welche Molekülformen am besten zu jedem Spektrum passen. Ein transformerbasiertes Modell sagt vorher, wie die Spektren von Kandidatenmolekülen aussehen sollten, und ein kombinierter Score gewichtet, wie gut die beobachteten und vorhergesagten Muster übereinstimmen — einschließlich feiner Details wie Isotopenmustern und exakter Masse. Durch die Analyse der Verteilung dieser Scores auf einem Standard-Benchmark identifiziert das Team Schwellenwerte, die wahrscheinliche echte Treffer von Rauschen oder ähnlichen Täuschern trennen, sodass einige Strukturvermutungen mit hoher Zuversicht markiert und offensichtlich falsche verworfen werden können.
Gene und Chemie zusammenbringen
Die wirkliche Stärke der Methode liegt in der Verschmelzung dieser beiden Informationsströme. Ein Mikroorganismus landet nur dann weit oben auf der Liste für ein Molekül von Interesse, wenn sowohl genetisches Potenzial vorliegt — seine Proteine ähneln denen eines bekannten Biosynthesewegs — als auch chemische Evidenz — er erzeugt spektrale Merkmale, die zur erwarteten Struktur passen. Diese Kreuzprüfung reduziert falsche Fährten, die in nur einer Datenart überzeugend wirken. Die Autoren testeten ihr Rahmenwerk an einer großen Sammlung actinobakterieller Stämme und Mutanten und konzentrierten sich dabei auf drei sehr unterschiedliche antimikrobielle Verbindungen: Valinomycin, Surfactin und das Antibiotikum Neomycin B. Anstatt auf perfekte Genome oder vollständige Spektralbibliotheken zu bauen, funktioniert das System auch gut, wenn Daten unordentlich oder unvollständig sind — ein häufiger Zustand in frühen Entdeckungsphasen. 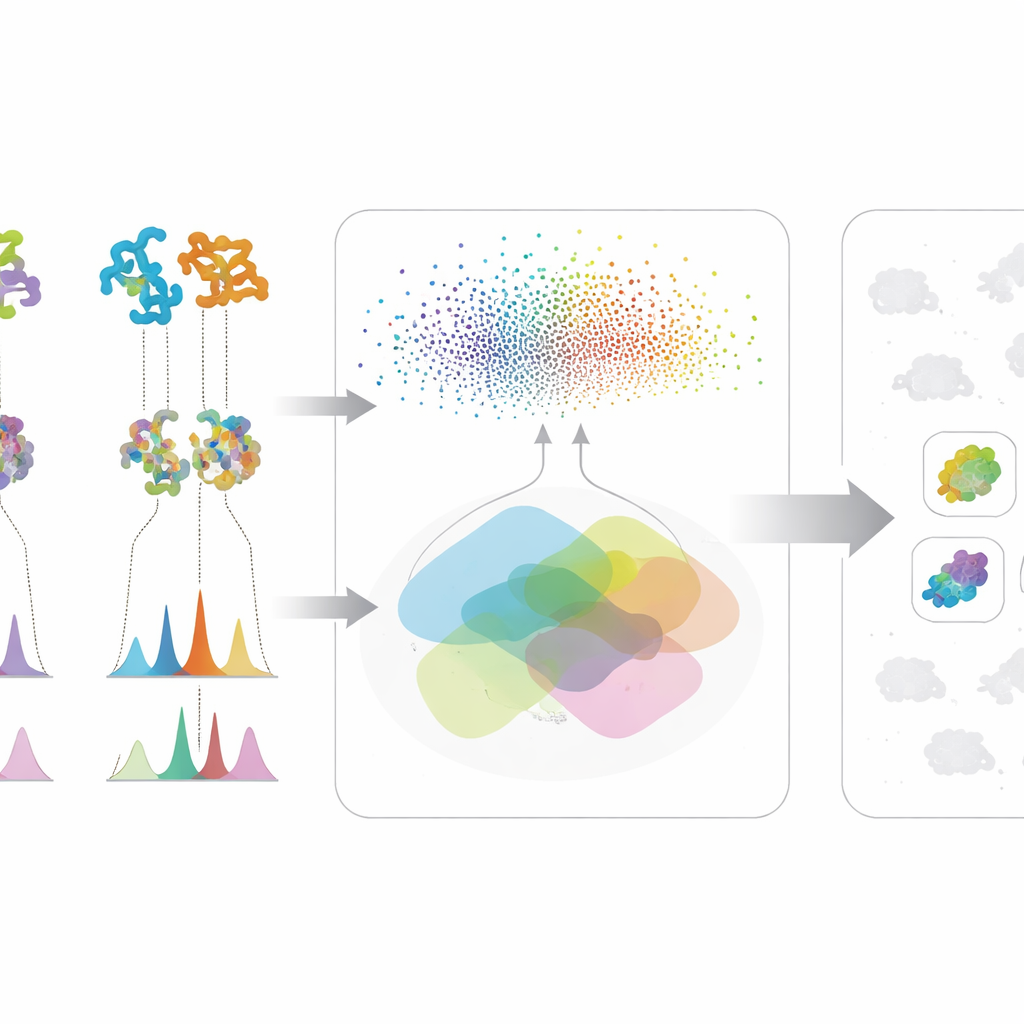
Das Rahmenwerk auf die Probe stellen
Im Fallstudie zu Neomycin B suchte die KI zunächst nach Mikroben, deren Proteine denen im bekannten Neomycin-Weg ähnelten, und prüfte dann, ob ihre Massenspektren Hinweise auf neomycinähnliche Moleküle enthielten. Vier Stämme bestanden beide Filter; drei von ihnen wurden experimentell bestätigt, Neomycin B herzustellen — darunter zwei zuvor unbekannte Produzenten. Für Valinomycin und Surfactin zeigte das Rahmenwerk ebenfalls eine hohe Präzision bei der Identifikation von Produzenten, während ein Kontrolltest mit zufällig vertauschten Scores deutlich schlechter abschnitt. Diese Ergebnisse deuten darauf hin, dass das Modell echte biologische Zusammenhänge erfasst und nicht nur zufällige Übereinstimmungen in den Daten, und dass es Forschende erfolgreich zu den wahrscheinlichsten Treffern in einem überfüllten Suchraum führen kann.
Was das für die zukünftige Arzneimittelentdeckung bedeutet
Alltagssprachlich haben die Autoren eine intelligente Empfehlungsmaschine für die Entdeckung natürlicher Produkte gebaut. Anstatt jede Mikrobe und jedes chemische Signal mit brachialer Gewalt zu testen, können Forschende sich jetzt auf eine kurze Liste von Stämmen konzentrieren, bei denen genetisches Potenzial und chemische Ergebnisse übereinstimmen. Das reduziert verschwendete Arbeit erheblich, lässt aber zugleich Raum, unerwartete Moleküle zu entdecken, die noch in keiner Referenzdatei stehen. Mit weiter verbesserten KI-Modellen und Datensätzen könnte diese Art integrierter genomischer und metabolomischer Analyse weite Bereiche der mikrobiellen Chemie erschließen, die bisher unerforscht sind, und möglicherweise neue Antibiotika und andere nützliche Verbindungen zutage fördern — gerade dann, wenn die Gesellschaft sie am dringendsten braucht.
Zitation: Tay, D.W.P., Koh, W., Ang, S.J. et al. Accelerating natural product discovery with linked MS-genomics and language/transformer-based models. npj Antimicrob Resist 4, 31 (2026). https://doi.org/10.1038/s44259-026-00206-7
Schlüsselwörter: Entdeckung natürlicher Produkte, mikrobielle Metaboliten, Massenpektronomie, Protein-Sprachmodelle, KI in der Arzneimittelforschung