Clear Sky Science · he
האצה של גילוי מוצרים טבעיים באמצעות קישור MS-גנומיקה ומודלים מבוססי שפה/טרנספורמר
מדוע תרופות חדשות מסתתרות מול עינינו
רבים מהתרופות החשובות שלנו, כולל אנטיביוטיקה ולחימת סרטן, מקורן במיקרואורגניזמים זעירים שמייצרים מולקולות טבעיות מורכבות. עם זאת, מציאת מולקולות חדשות בארסנל מוסתר זה איטית ויקרה, כי על המדענים למיין ספריות עצומות של מיקרובים ולנחש אילו מהם שווים בדיקה. המאמר הזה מציג כיצד שילוב בינה מלאכותית מתקדמת עם מדידות מעבדה מודרניות יכול להאיץ במידה ניכרת את החיפוש, ועוזר לחוקרים להתמקד במיקרובים המבטיחים ביותר לפני ביצוע ניסויים מייגעים. 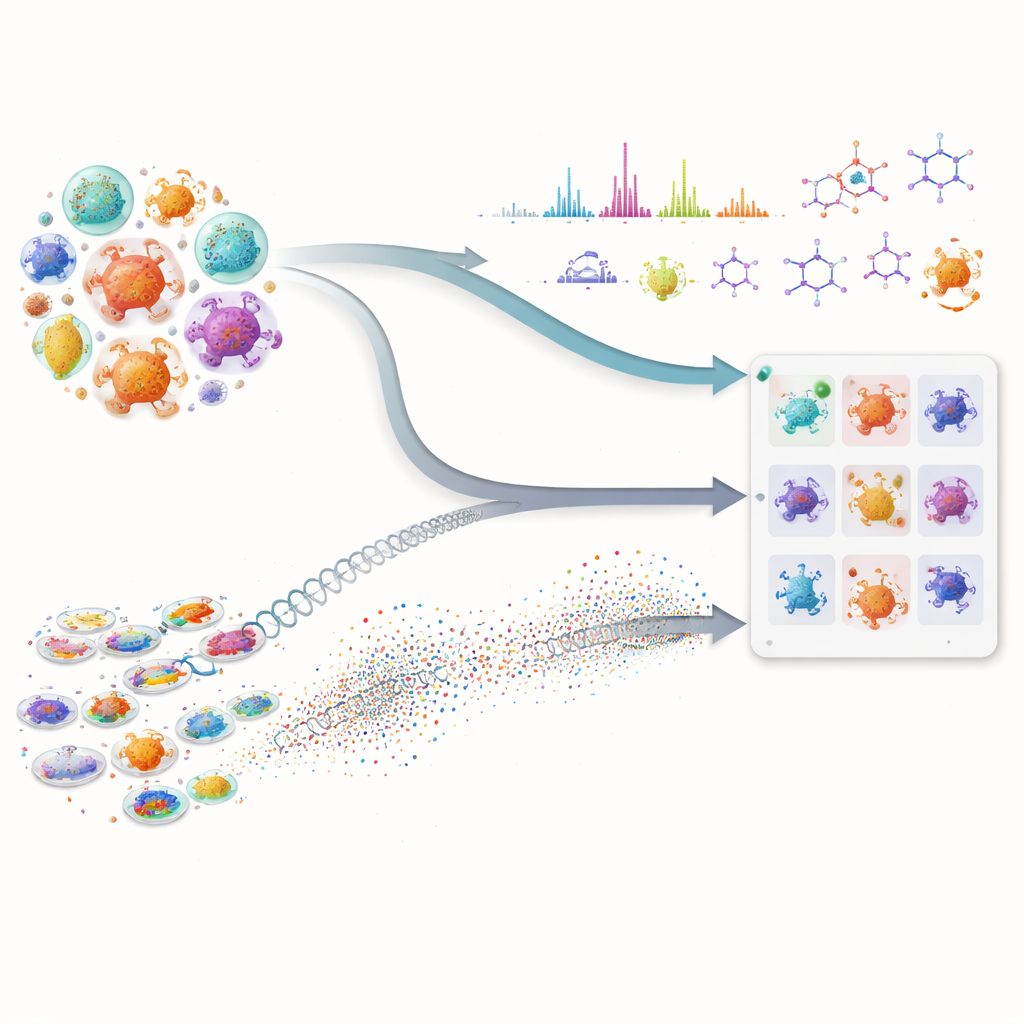
הפיכת DNA של מיקרובים למפה חיפושית
החלק הראשון של הגישה בוחן את "התכניות" הגנטיות של המיקרובים. במקום להסתמך רק על התאמות DNA מסורתיות, הצוות משתמש במודלי שפה לחלבונים חזקים — מערכות בינה מלאכותית שלמדו דפוסים במיליוני רצפי חלבונים. מודלים אלה ממירים כל חלבון ביוסינתטי לטביעת אצבע מספרית בממד גבוה. זה מאפשר למדענים לזהות קרובים פונקציונליים מרוחקים גם כאשר ה-DNA הבסיסי השתנה רבות או מפוצל לחתיכות, בעיה שכיחה בגנומים בגדר טיוטה. החוקרים מדורגים כל מיקרוב לפי כמה מחלבוניו דומים לאלה שבנתיב מוכר לייצור מולקולה מטרה, וכמה חזקה הדמיון הכולל. ציון משולב זה מדגיש זנים שבהם סט החלבונים המשולב נראה כמי שיכול לבנות את התרכובת הרצויה, ומפחית משקל על מיקרובים שיש להם רק אחד או שניים אנזימים נפוצים ולא מיוחדים.
קריאת תערובות כימיות מורכבות בעזרת בינה מלאכותית
החלק השני מתמקד במה שהמיקרובים בפועל מייצרים במעבדה. באמצעות כרומטוגרפיה נוזלית וספקטרומטריית מסה מאזנת (tandem MS), המדענים רושמים "טביעות אצבע" מפורטות של המולקולות בבירות התסיסה. מערכת העבודה הפנימית של המחברים לפתרון מובנה של מבנים, המכונה WISE, מנקה את האותות הללו, מפרידה פסגות חופפות, ואז משתמשת במודלי בינה מלאכותית שאומנו על מיליוני מבנים הדומים למוצרים טבעיים כדי לנחש אילו צורות מולקולריות מתאימות ביותר לכל ספקטרום. מודל מבוסס טרנספורמר חוזה כיצד אמורים להיראות ספקטרות של מולקולות מועמדות, וציון משולב שוקל עד כמה התבניות הנצפות והחזקות צפויות תואמות, כולל פרטים עדינים כמו דפוסי איזוטופים ומסה מדויקת. באמצעות ניתוח ההתפלגות של ציונים אלה בבנצ׳מרק סטנדרטי, הקבוצה מזהה ספים המבדילים התאמות סבירות מאנשי רעש או מזוייפים דומים, ומאפשרת לסווג כמה ניחושי מבנה כבעלי אמינות גבוהה ולסנן כאלה הברורים כשגויים.
שילוב בין גנים וכימיה
העוצמה האמיתית של השיטה נובעת מהמיזוג של שני זרמי המידע הללו. עבור כל מולקולה מעניינת, מיקרוב עולה לראש הרשימה רק אם הוא מציג גם פוטנציאל גנטי — חלבוניו דומים לאלה שבנתיב מוכר — וגם עדות כימית — הוא מייצר תכונות ספקטרליות שמתאימות למבנה הצפוי. בדיקה מקבילה זו מקטינה אותות שווא שנראים משכנעים רק בסוג אחד של נתונים. המחברים בדקו את המסגרת שלהם על אוסף גדול של זני אקטינובקטריה ומוטנטים, תוך התמקדות בשלוש תרכובות אנטימיקרוביאליות שונות מאוד: ולינומיצין, סורפקטין והאנטיביוטיקה Neomycin B. במקום להסתמך על גנומים מושלמים או על ספריות ספקטרליות מלאות, המערכת פועלת היטב גם כאשר הנתונים מלוכלכים או חלקיים — מציאות שכיחה בקמפיינים של גילוי בשלבים מוקדמים. 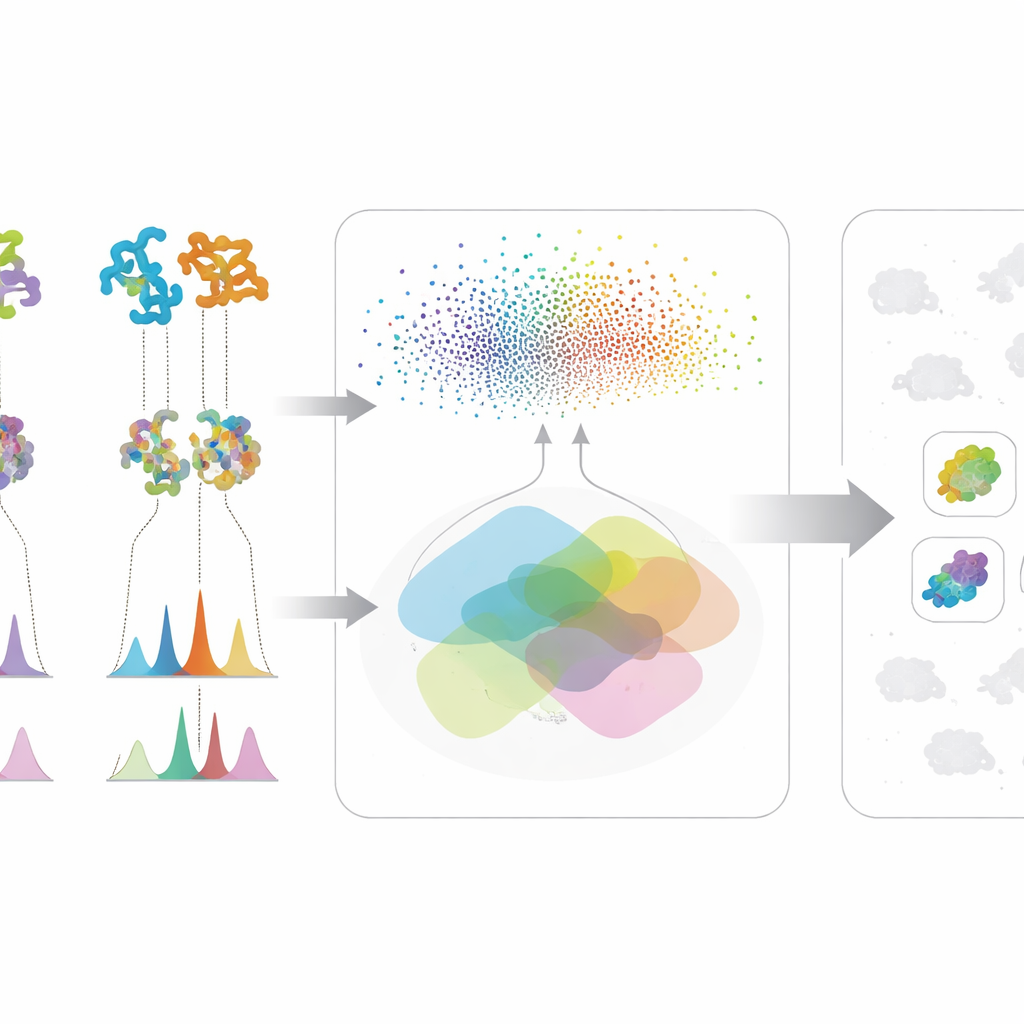
הצבת המסגרת במבחן
במקרה המפורט של Neomycin B, הבינה תחילה חיפשה מיקרובים שחלבוניהם נראו כמו אלה שבנתיב הידוע של ניאומיצין, ואז בדקה האם הספקטרות שלהם רמזו על נוכחות מולקולות דמויות ניאומיצין. ארבעה זנים עברו את שני המסננים; שלושה מהם אושרו בניסויים כיצרנים של Neomycin B, כולל שניים שלא זוהו בעבר ככאלה. עבור ולינומיצין וסורפקטין, המסגרת גם זיהתה יצרנים בדיוק גבוה, בעוד שניסוי ביקורת שבו ערבבו את הציונים באופן אקראי נתן תוצאה גרועה בהרבה. התוצאות הללו מראות שהמודל לוכד יחסים ביולוגיים אמיתיים, ולא רק מקריות אקראית בנתונים, ושניתן להשתמש בו כדי להנחות חוקרים לעבר המועמדים הסבירים ביותר במרחב חיפוש צפוף.
מה משמעות הדבר עבור גילוי תרופות בעתיד
במלים פשוטות, המחברים בנו מנוע המלצות חכם לגילוי מוצרים טבעיים. במקום לבדוק כל מיקרוב וכל אות כימית בשיטה של כוח גס, מדענים יכולים כעת להתמקד ברשימה קצרה של זנים שבהם הפוטנציאל הגנטי והתוצר הכימי מסכימים. זה מקצץ משמעותית בעבודה מבוזבזת, ובו־בזמן משאיר מקום לגילוי מולקולות בלתי צפויות שטרם נמצאות בכל ספר הפניות. ככל שמודלים וערכות נתונים של בינה מלאכותית ממשיכים להשתפר, סוג זה של ניתוח משולב של גנום ומטבולום עשוי לפתוח אזורים עצומים של כימיה מיקרוביאלית שעדיין לא נחקרו, ולחשוף אנטיביוטיקה חדשה וחומרי שימוש אחרים בדיוק כשחברתנו זקוקה להם ביותר.
ציטוט: Tay, D.W.P., Koh, W., Ang, S.J. et al. Accelerating natural product discovery with linked MS-genomics and language/transformer-based models. npj Antimicrob Resist 4, 31 (2026). https://doi.org/10.1038/s44259-026-00206-7
מילות מפתח: גילוי מוצרים טבעיים, מטבוליטים מיקרוביאליים, ספקטרומטריית מסה, מודלים לשוניים לחלבונים, בינה מלאכותית בגילוי תרופות