Clear Sky Science · tr
Alzheimer hastalığı beyin hücrelerinde RNA izoform çeşitliliği, ekzon kaynaştırma varyantları ve hücre başına geçişler
Alzheimer’da küçük RNA farklılıkları neden önemli
Alzheimer hastalığı genellikle plaklar, yumaklar ve ölmekte olan nöronlarla tanımlanır. Ancak bu mikroskop görüntülerinin altında daha ince bir karmaşıklık katmanı yatar: her beyin hücresine hangi proteinleri yapması gerektiğini söyleyen RNA mesajları. Bu çalışma, tek hücre çözünürlüğünde o gizli katmana bakarak, yalnızca genlerin değil her genin RNA’sının tam "sürümleri" olarak adlandırılan izoformların Alzheimer beyinlerinde kapsamlı biçimde değiştiğini gösteriyor. Bu ince mesaj değişikliklerini anlamak, belli beyin hücrelerinin neden çöktüğünü açıklamaya yardımcı olabilir ve yeni biyobelirteçler veya ilaç hedefleri ortaya çıkarabilir.
Bireysel beyin hücrelerinin içini görmek
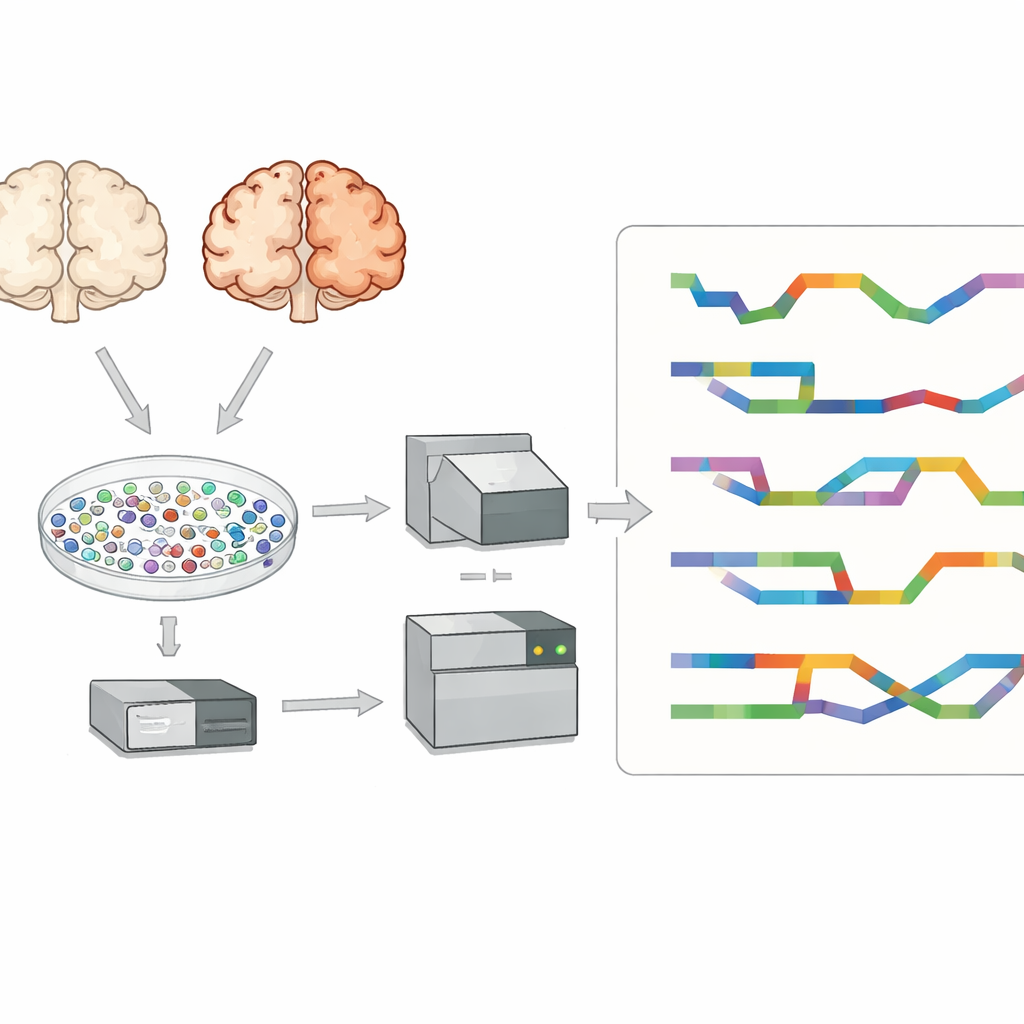
Araştırmacılar, Alzheimer’da güçlü biçimde etkilenen düşünme ve hafıza için önemli bir beyin bölgesi olan prefrontal kortekse odaklandı. Sekiz Alzheimer hastası ve yedi sağlıklı bireyden doku incelediler. Karışık doku yerine onlarca bin bireysel hücre çekirdeğini izole edip her birinin içindeki RNA’yı yakaladılar. Bu, uyarıcı ve inhibe edici nöronlar, astrositler, mikroglia, oligodendrositler ve onların öncülleri gibi ana beyin hücre tiplerini tanımlayıp Alzheimer ve sağlıklı beyinleri tek, karışık bir sinyal yerine hücre tipi bazında karşılaştırmalarını sağladı.
İki tür dizileme gücünü birleştirmek
Çoğu tek hücre çalışması, RNA’nın küçük parçalarını iyi okuyan ancak tam boy transkriptleri ve kesin ekzon desenlerini yeniden oluşturmakta zorlanan kısa-okuma dizilemesini kullanır. Bunu aşmak için ekip, standart kısa-okuma yöntemlerinin yanında PacBio Kinnex adı verilen uzun-okuma teknolojisini kullandı. Kinnex, birçok cDNA molekülünü uç uca bağlayarak tek bir uzun-okuma çalışmasının birçok tam uzunlukta RNA kopyasını yakalamasını sağlar. Dizileme sonrası bu uzun okumalar dijital olarak bireysel moleküllere ayrıldı ve orijinal hücre barkodlarına eşlendi. Bu yaklaşım, hücre tipi kimliği ve ayrıntılı izoform bilgisi birlikte olan yaklaşık 70.000 tek çekirdeği üreterek Alzheimer beynindeki RNA çeşitliliğine alışılmadık derecede zengin bir bakış sundu.
Geniş bir RNA varyantları manzarası
Bu verilerden araştırmacılar 850.000’den fazla RNA izoformu tespit etti ve sonra birden fazla beyinde sağlam biçimde gözlemlenen yaklaşık 53.500 "güvenilir" izoformu tanımlamak için sıkı filtreler uyguladı. Çoğu bilinen transkript türlerine aitti, ancak yaklaşık 4.000’i açıkça yeniydi; bu da iyi çalışılmış insan korteksinin bile beklenmeyen RNA varyantları sakladığını gösteriyor. Birçok gen birden fazla izoform üretti; bazıları—örneğin dystonin geni—onlarca farklı sürüm sergiledi. Ekip ayrıca sıra dışı iç bağlantılara sahip nadir izoformlar gözlemledi; bazıları daha önce Alzheimer’da tanımlanmış olan somatik gen rekombinasyonu adlı bir süreçle ilişkilendirilebilecek nitelikteydi ve beyin RNA’sının ne kadar çeşitli ve dinamik olabileceğini vurguladı.
Genler tek başına gösteremeyecek gizli değişiklikler
Araştırmacılar kısa-okuma verileriyle Alzheimer ve sağlıklı beyinleri gen düzeyinde karşılaştırdıklarında tanıdık desenler gördüler: mikroglia ve astrositlerde inflamatuar yollar daha aktiftir ve nöronlar ile oligodendrositlerde sinaps ve amiloid işleme ile ilişkili genler değişmiştir. Ancak uzun-okuma izoform analizi, gen düzeyindeki ortalamaların tamamen kaçırdığı değişiklikleri ortaya çıkardı. Bazı genler toplam ifade düzeyinde az veya hiç fark göstermezken, belirli izoformlar Alzheimer’da güçlü şekilde artmış veya azalmış ya da göreli bollukta "geçiş" yapmıştı. Örneğin hücrenin iç iskeletiyle ilgili ve nörodejeneratif hastalıklarda protein agregatlarında bulunan SEPTIN4 geninin bir izoformu azalmış, bir diğeri artmış; bunlar gen düzeyinde birbirini iptal etti. İnflamasyonla ilişkili YKL-40 proteinini kodlayan CHI3L1 geni astrositlerde esas olarak segmentleri tutulan tek bir yeni izoform aracılığıyla yükselmiş, bilinen transkript değişmeden kalmıştı. APOE, BIN1, APP ve MAPT gibi AD ilişkili genlerde de benzer izoform düzeyinde kaymalar görüldü; bunlar sıklıkla hücre tipine özgüydü.
Farklı hücre tipleri, farklı RNA imzaları
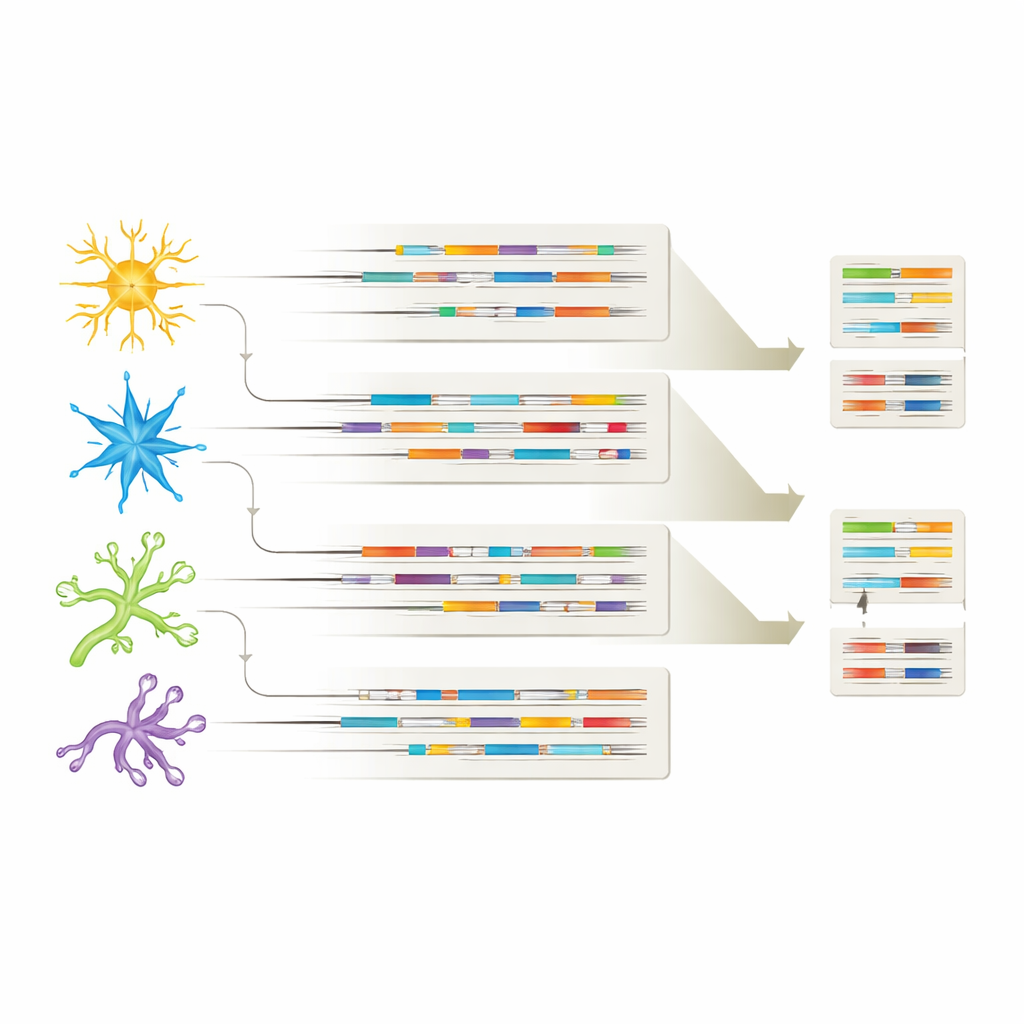
Her izoformu köken aldığı hücre tipiyle ilişkilendirerek çalışma, her ana beyin hücresi popülasyonunun kendine özgü bir izoform "parmak izi" taşıdığını gösterdi. Birçok RNA varyantı nöronlar ve glial hücreler arasında paylaşılıyordu, ancak her hücre tipi ayrıca sağlığa ve hastalığa özgü rollerini ima eden benzersiz izoformlar da ifade ediyordu. Bazı durumlarda belirli izoformlar yalnızca Alzheimer beyinlerinde veya yalnızca belirli hücre tiplerinde görünüyordu; örneğin inhibe edici nöronlarda belirli APP varyantları veya astrositlere sınırlı bir CHI3L1 izoformu. Bu desenler, hangi genlerin açık veya kapalı olduğunun yanı sıra her hücre tipinde hangi spesifik RNA sürümlerinin kullanıldığının Alzheimer’ın gelişimini ve hangi hücrelerin daha savunmasız olduğunu şekillendirebileceğini öne sürüyor.
Alzheimer’ı anlamak ve tedavi etmek için ne anlama geliyor
Bu çalışma, Alzheimer beyninin yalnızca genleri yanlış kullanmadığını, aynı zamanda hücre tiplerine göre farklılık gösteren biçimlerde RNA mesajlarının ince yapısını da yeniden karıştırdığını gösteriyor. Uzun-okuma tek hücre dizilemesi, geleneksel gen düzeyinde çalışmalarda görünmez olan hastalıkla ilişkili izoform değişikliklerini açığa çıkarıyor. SEPTIN4 ve CHI3L1 gibi değişmiş izoformlar da dahil olmak üzere bazı yeni tanımlanan RNA varyantları beyin hasarında doğrudan rol oynayabilir veya inflamasyon ve dejenerasyonun daha hassas biyobelirteçleri olarak hizmet edebilir. Bunların işlevlerini ve klinik yararlılığını test etmek için daha fazla araştırma gerekir, ancak bu çalışma gelecekte Alzheimer’ı anlamak ve nihayetinde tedavi etmek için çabaların yalnızca genleri değil, aynı zamanda bireysel beyin hücrelerindeki RNA izoformlarının tam çeşitliliğini dikkate alması gerektiğini netleştiriyor.
Atıf: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
Anahtar kelimeler: Alzheimer hastalığı, RNA kaynaştırma, tek hücre dizilemesi, RNA izoformları, nöroinflamasyon