Clear Sky Science · ja
アルツハイマー病脳の単一細胞におけるRNAアイソフォーム多様性、スプライシング変異およびスイッチング
アルツハイマーでわずかなRNA差が重要な理由
アルツハイマー病は通常、プラーク、タングル、そして死にゆく神経細胞といった像で語られます。しかし顕微鏡像の下には、さらに微細な複雑さの層が存在します。それは各脳細胞にどのタンパク質を作るかを指示するRNAメッセージです。本研究は単一細胞分解能でその隠れた層を覗き込み、遺伝子だけでなく各遺伝子のRNAの「バージョン」すなわちアイソフォームがアルツハイマー脳で広範に変化していることを示します。これらの微妙なメッセージ変化を理解することは、どの細胞が脆弱になるかを説明し、新たなバイオマーカーや薬剤標的を見つける手がかりになる可能性があります。
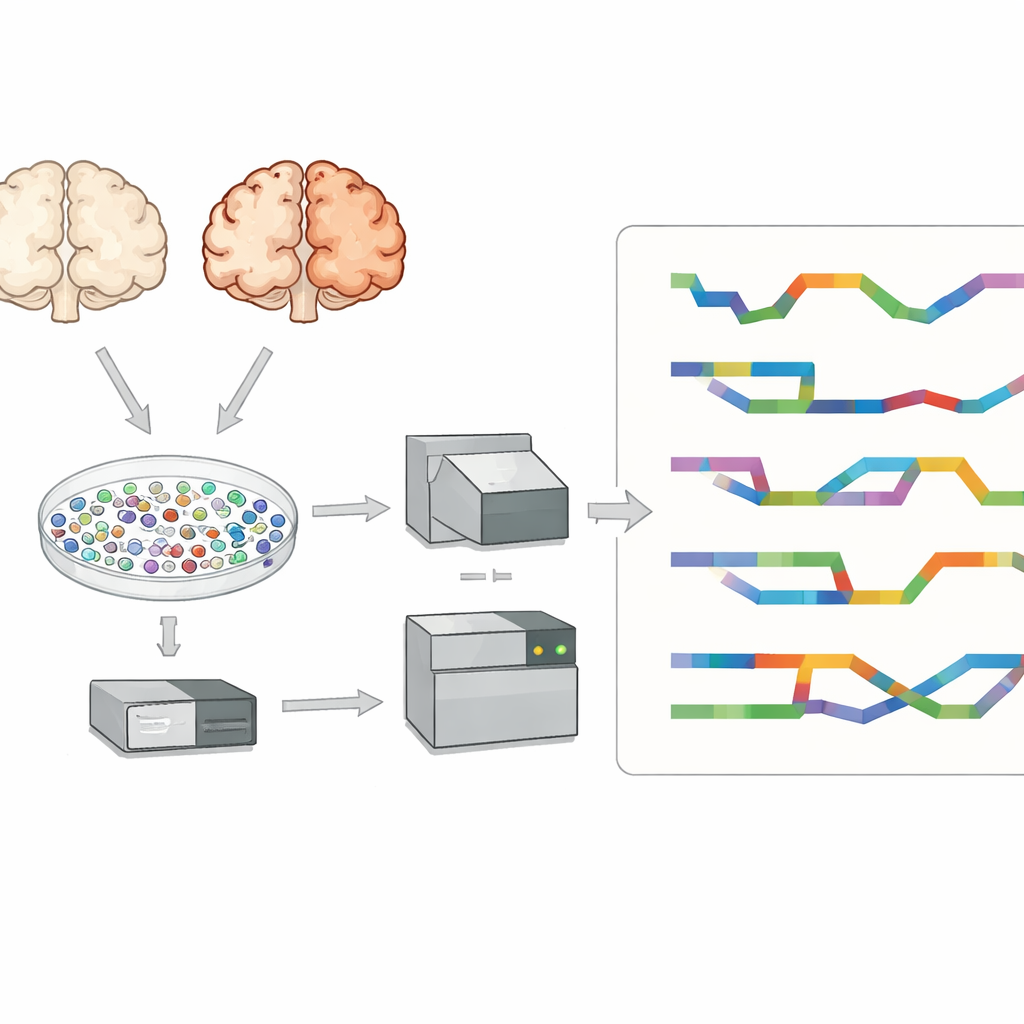
個々の脳細胞の内部を覗く
研究者たちは前頭前皮質に着目しました。これは思考や記憶に関与し、アルツハイマー病で強く影響を受ける領域です。アルツハイマー病の患者8名と非罹患者7名の組織を調べました。混合した組織を調べる代わりに、数万個の個々の細胞核を分離してそれぞれの核内のRNAを捉えました。これにより、興奮性・抑制性ニューロン、アストロサイト、ミクログリア、オリゴデンドロサイトおよびその前駆細胞といった主要な脳細胞型を同定し、アルツハイマー脳と非病変脳を混合シグナルではなく細胞型ごとに比較することが可能になりました。
二種類のシーケンシング技術の併用
ほとんどの単一細胞研究はショートリードシーケンシングを用います。これはRNAの短い断片を正確に読む一方で、完全長転写産物や正確なスプライスパターンを再構築するのは苦手です。この制約を克服するため、チームはPacBio Kinnexというロングリード技術を標準的なショートリード法と併用しました。Kinnexは多数のcDNA分子を端から端まで連結して、単一のロングリードで多くの完全長RNAコピーを捕捉します。シーケンス後、これらの長いリードをデジタルに個々の分子に切り戻し、元の細胞バーコードに対応付けました。この手法により、細胞型同定と詳細なアイソフォーム情報の両方を持つ約7万個の単一核が得られ、アルツハイマー脳におけるRNA多様性の非常に豊かな図を提供しました。
広大なRNAバリアントの景観
これらのデータから、研究者たちは85万を超えるRNAアイソフォームを検出し、厳格なフィルタを適用して約53,500の「信頼できる」アイソフォームを定義しました。これらは複数の脳で頑健に観察されたものです。大部分は既知の転写産物タイプに属していましたが、約4,000は明確に新規であり、よく研究されたヒト皮質でも予期せぬRNAバリアントが隠れていることを明らかにしました。多くの遺伝子が複数のアイソフォームを産み出し、例えばdystonin遺伝子のように数十種類の異なるバージョンを示すものもありました。チームはまた、まれな内部ジャンクションを持つ稀なアイソフォームも観察しており、その一部は以前にアルツハイマー病で報告された体細胞遺伝子再編成と関連する可能性があり、脳RNAがいかに多様で動的であるかを強調しています。
遺伝子レベルだけでは見えない隠れた変化
研究者たちがショートリードデータで遺伝子レベルでアルツハイマー脳と非病変脳を比較すると、既知のパターンが見えました:ミクログリアやアストロサイトで炎症経路がより活性化し、ニューロンやオリゴデンドロサイトではシナプスやアミロイド処理に関係する遺伝子が変化していました。しかしロングリードのアイソフォーム解析は、遺伝子レベルの平均では完全に見落とされる変化を明らかにしました。ある遺伝子は全体の発現にほとんど差がないか全く差が見られないにもかかわらず、特定のアイソフォームが強く増減したり、相対的な存在比が「スイッチ」したりしていました。例えば細胞内の足場に関与し神経変性疾患のタンパク質凝集体で見つかるSEPTIN4は、あるアイソフォームが減少し別のものが増加して互いに打ち消し合い、遺伝子レベルでは変化が見えにくくなっていました。別の例として炎症関連タンパク質YKL-40をコードするCHI3L1は、既知のトランスクリプトは変化しない一方で、保持されたセグメントを持つ単一の新規アイソフォームを介してアストロサイトで主に上方制御されていました。APOE、BIN1、APP、MAPTといったAD関連遺伝子でも、細胞型特異的にアイソフォームレベルのシフトが頻繁に観察されました。
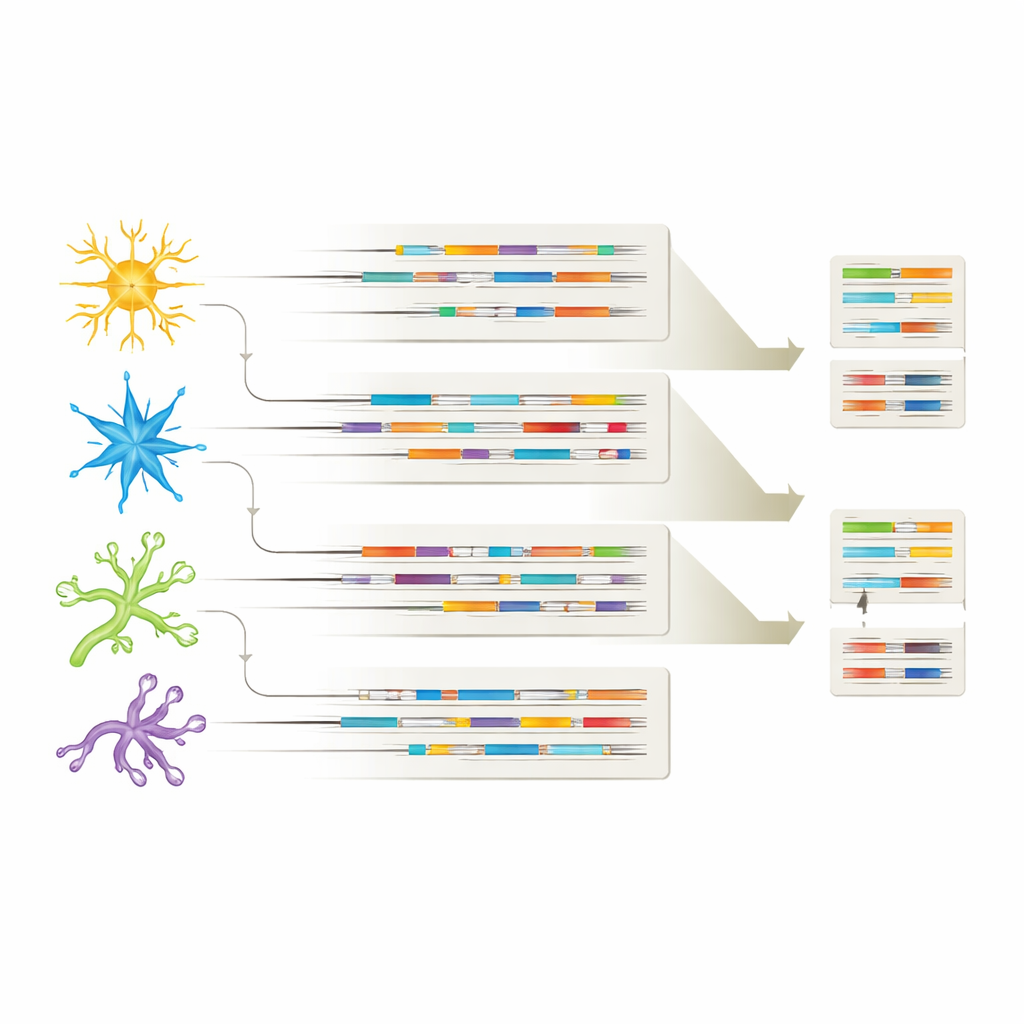
細胞型ごとに異なるRNAシグネチャ
各アイソフォームを起源となる細胞型に結び付けることで、本研究は主要な脳細胞集団ごとにそれぞれ独自のアイソフォーム「指紋」があることを示しました。多くのRNAバリアントはニューロンとグリア細胞の間で共有されていましたが、各細胞型は独自のアイソフォームも発現しており、健康や病気における専門的な役割を示唆します。場合によっては、特定のアイソフォームがアルツハイマー脳にのみ、あるいは特定の細胞型にのみ現れることがありました。例えば抑制性ニューロンに見られる特定のAPP変異体や、アストロサイトに限局したCHI3L1アイソフォームなどです。これらのパターンは、どの遺伝子がオンかオフかだけでなく、各細胞型でどの特定のRNAバージョンが使われているかが、アルツハイマーの進展やどの細胞が脆弱になるかを形作る可能性があることを示唆しています。
アルツハイマー理解と治療への含意
本研究は、アルツハイマー脳が単に遺伝子を誤用しているのではなく、細胞型ごとに異なる方法でRNAメッセージの微細構造を再編成していることを示しています。ロングリード単一細胞シーケンシングは、従来の遺伝子レベルの研究では不可視であった疾患に関連するアイソフォーム変化を露わにします。SEPTIN4やCHI3L1の変化したアイソフォームのような新たに同定されたRNAバリアントの一部は、脳障害に直接関与したり、炎症や変性のより精密なバイオマーカーとして機能したりする可能性があります。これらの機能や臨床的有用性を検証するにはさらなる研究が必要ですが、本研究は、アルツハイマーを理解し最終的に治療を目指すためには、遺伝子だけでなく個々の脳細胞におけるRNAアイソフォームの全多様性を考慮する必要があることを明確に示しています。
引用: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
キーワード: アルツハイマー病, RNAスプライシング, 単一細胞シーケンシング, RNAアイソフォーム, 神経炎症