Clear Sky Science · nl
Diversiteit van RNA-isoformen, splice‑varianten en schakelingen in individuele cellen van het Alzheimer‑brein
Waarom kleine RNA‑verschillen ertoe doen bij Alzheimer
De ziekte van Alzheimer wordt meestal beschreven in termen van plaques, tangles en afstervende zenuwcellen. Maar onder die microscoopbeelden ligt een nog fijnere laag van complexiteit: de RNA‑boodschappen die elke hersencel vertellen welke eiwitten gemaakt moeten worden. Deze studie kijkt naar die verborgen laag op enkel‑celresolutie en laat zien dat niet alleen genen, maar de exacte "versies" van elk gen — de zogenaamde isoformen — uitgebreid veranderd zijn in Alzheimer‑hersenen. Het begrijpen van deze subtiele veranderingen in boodschappen kan helpen verklaren waarom bepaalde cellen het laten afweten en mogelijk nieuwe biomarkers of medicijndoelen onthullen.
Inzicht in individuele hersencellen
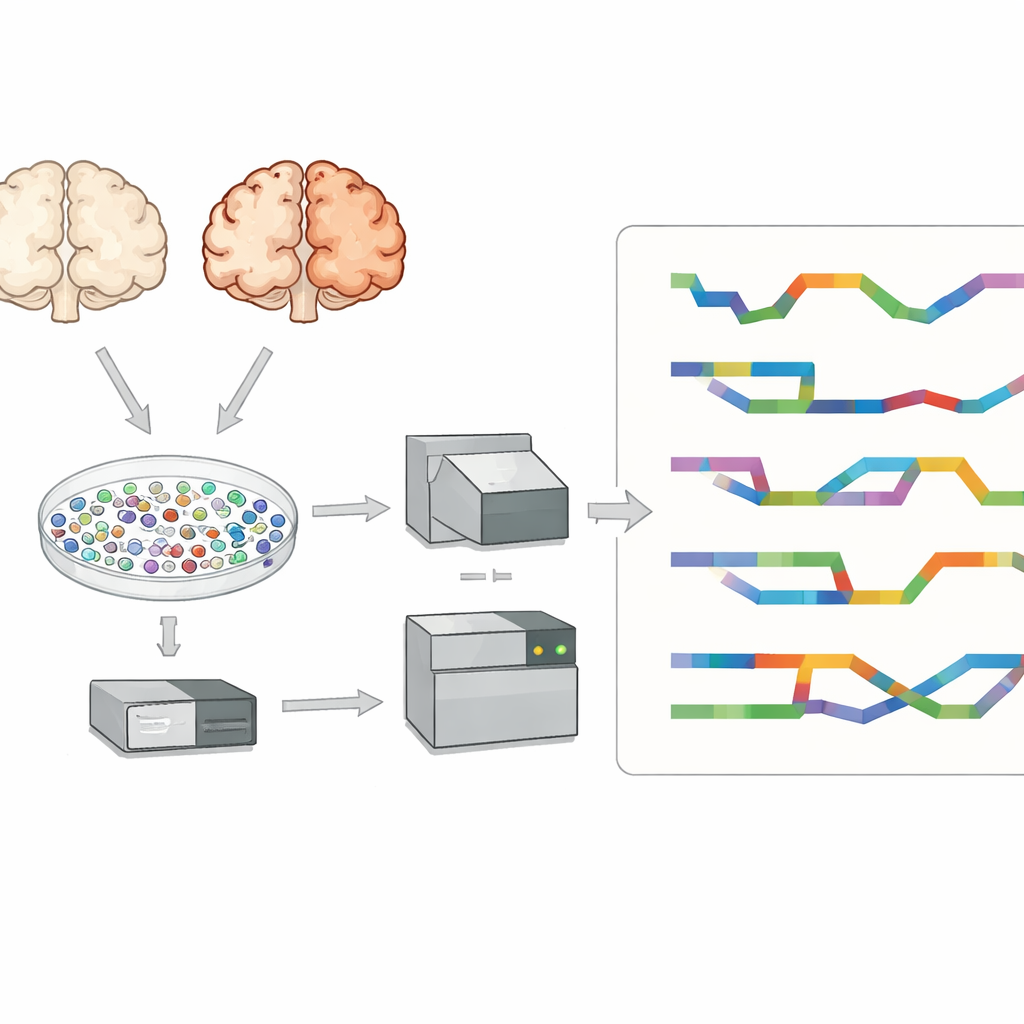
De onderzoekers richtten zich op de prefrontale cortex, een hersengebied dat belangrijk is voor denken en geheugen en dat sterk wordt aangetast bij de ziekte van Alzheimer. Ze onderzochten weefsel van acht mensen met Alzheimer en zeven zonder de ziekte. In plaats van gemengd weefsel te bestuderen isoleerden ze tienduizenden afzonderlijke celkernen en vingen het RNA in elk daarvan op. Dit stelde hen in staat belangrijke hersenceltypen te identificeren — zoals exciterende en remmende neuronen, astrocyten, microgliacellen, oligodendrocyten en hun voorlopers — en Alzheimer‑ en niet‑zieke hersenen celtype voor celtype te vergelijken, in plaats van als één samengevoegd signaal.
Combinatie van twee sequentietechnologieën
De meeste single‑cell studies gebruiken short‑read sequencing, die korte RNA‑fragmenten goed leest maar moeite heeft om volledige transcripties en hun exacte splicepatronen te reconstrueren. Om dit te overwinnen gebruikte het team een long‑read technologie genaamd PacBio Kinnex naast standaard short‑read methoden. Kinnex werkt door veel cDNA‑moleculen aan elkaar te koppelen zodat één long‑read‑run vele volledige RNA‑kopieën vastlegt. Na sequencing werden deze lange reads digitaal teruggesneden tot individuele moleculen en vervolgens gekoppeld aan de oorspronkelijke celbarcodes. Deze aanpak leverde ongeveer 70.000 enkele kernen met zowel celtype‑identiteit als gedetailleerde isoform‑informatie, wat een uitzonderlijk rijk beeld gaf van RNA‑diversiteit in het Alzheimer‑brein.
Een uitgestrekt landschap van RNA‑varianten
Uit deze data detecteerden de wetenschappers meer dan 850.000 RNA‑isoformen en pasten ze strikte filters toe om ongeveer 53.500 "vertrouwde" isoformen te definiëren die robuust werden waargenomen in meerdere hersenen. De meeste behoorden tot bekende transcripttypes, maar bijna 4.000 waren duidelijk nieuw, wat aantoont dat zelfs de goed bestudeerde menselijke cortex nog onverwachte RNA‑varianten verbergt. Veel genen produceerden meerdere isoformen, waarbij sommige — zoals het dystonin‑gen — tientallen verschillende versies lieten zien. Het team zag ook zeldzame isoformen met ongebruikelijke interne junctions, waarvan sommige mogelijk gelinkt zijn aan een proces dat somatische genrecombinatie wordt genoemd en eerder in Alzheimer beschreven is, wat onderstreept hoe divers en dynamisch hersen‑RNA kan zijn.
Verborgen veranderingen die op gen‑niveau onzichtbaar blijven
Toen de onderzoekers Alzheimer‑ en niet‑zieke hersenen op gen‑niveau vergeleken met short‑read data, zagen ze vertrouwde patronen: ontstekingsroutes waren actiever in microgliacellen en astrocyten, en genen die met synapsen en amyloïde verwerking te maken hebben waren veranderd in neuronen en oligodendrocyten. Maar de long‑read isoform‑analyse onthulde veranderingen die gemiddelden op gen‑niveau volledig misten. Sommige genen lieten weinig of geen algemene expressieverschuiving zien, toch waren specifieke isoformen sterk verhoogd of verlaagd of zelfs van relatieve abundantie gewisseld in Alzheimer. Bijvoorbeeld het gen SEPTIN4, betrokken bij het interne skelet van de cel en gevonden in eiwitaggregaten bij neurodegeneratie, had de ene isoform verminderd en een andere verhoogd, waardoor de veranderingen op gen‑niveau elkaar opheffen. Een ander gen, CHI3L1 — dat het ontstekingsgeassocieerde eiwit YKL‑40 codeert — was voornamelijk in astrocyten opgereguleerd via één nieuwe isoform met behouden segmenten, terwijl het bekende transcript onveranderd bleef. Vergelijkbare isoform‑verschuivingen werden gezien voor AD‑gerelateerde genen zoals APOE, BIN1, APP en MAPT, vaak op een celtype‑specifieke manier.
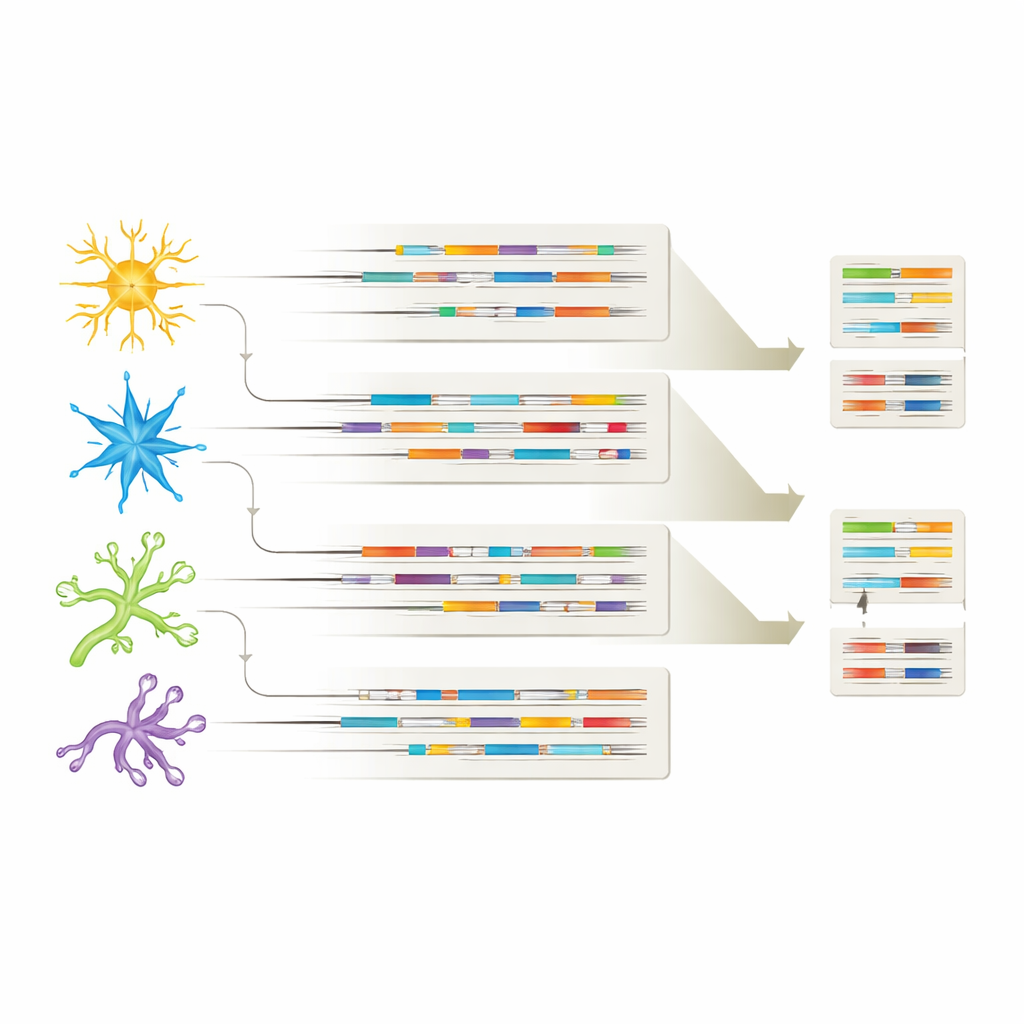
Verschillende celtypen, verschillende RNA‑handtekeningen
Door elke isoform te koppelen aan het celtype van herkomst toonde de studie aan dat elke grote hersencelpopulatie zijn eigen karakteristieke isoform‑"vingerafdruk" draagt. Veel RNA‑varianten werden gedeeld tussen neuronen en gliale cellen, maar elk celtype drukte ook unieke isoformen uit, wat wijst op gespecialiseerde rollen in gezondheid en ziekte. In sommige gevallen leken bepaalde isoformen alleen in Alzheimer‑hersenen of alleen in specifieke celtypen voor te komen, zoals bepaalde APP‑varianten in remmende neuronen of een CHI3L1‑isoform beperkt tot astrocyten. Deze patronen suggereren dat niet alleen welke genen aan of uit staan, maar welke specifieke RNA‑versies in elk celtype worden gebruikt, mede bepalen hoe Alzheimer zich ontwikkelt en welke cellen het meest kwetsbaar zijn.
Betekenis voor begrip en behandeling van Alzheimer
Dit werk laat zien dat het Alzheimer‑brein niet alleen genen verkeerd gebruikt, maar ook de fijne structuur van zijn RNA‑boodschappen op manieren herschikt die per celtype verschillen. Long‑read single‑cell sequencing legt ziekte‑gekoppelde isoformveranderingen bloot die in conventionele gen‑niveau studies onzichtbaar blijven. Sommige van deze nieuw geïdentificeerde RNA‑varianten, zoals gewijzigde isoformen van SEPTIN4 en CHI3L1, kunnen een directe rol spelen bij hersenschade of dienen als preciezere biomarkers voor ontsteking en degeneratie. Hoewel vervolgonderzoek nodig is om hun functies en klinische bruikbaarheid te testen, maakt deze studie duidelijk dat toekomstige inspanningen om Alzheimer te begrijpen — en uiteindelijk te behandelen — niet alleen naar genen moeten kijken, maar naar de volledige diversiteit van hun RNA‑isoformen in individuele hersencellen.
Bronvermelding: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
Trefwoorden: Ziekte van Alzheimer, RNA‑splicing, single‑cell sequencing, RNA‑isoformen, neuroinflammatie