Clear Sky Science · it
Diversità degli isoformi di RNA, varianti di splicing e switching nelle singole cellule del cervello affetto da Alzheimer
Perché piccole differenze nell’RNA contano nell’Alzheimer
La malattia di Alzheimer viene di solito descritta in termini di placche, grovigli e cellule nervose morenti. Ma sotto quelle immagini al microscopio si nasconde uno strato di complessità ancora più fine: i messaggi di RNA che dicono a ogni cellula cerebrale quali proteine produrre. Questo studio guarda a quello strato nascosto con risoluzione a singola cellula, mostrando che non sono interessati soltanto i geni, ma le esatte “versioni” dell’RNA di ogni gene—chiamate isoformi—che risultano ampiamente alterate nei cervelli con Alzheimer. Capire questi sottili cambiamenti nei messaggi potrebbe aiutare a spiegare perché certe cellule cerebrali cedono e potrebbe rivelare nuovi biomarcatori o bersagli farmacologici.
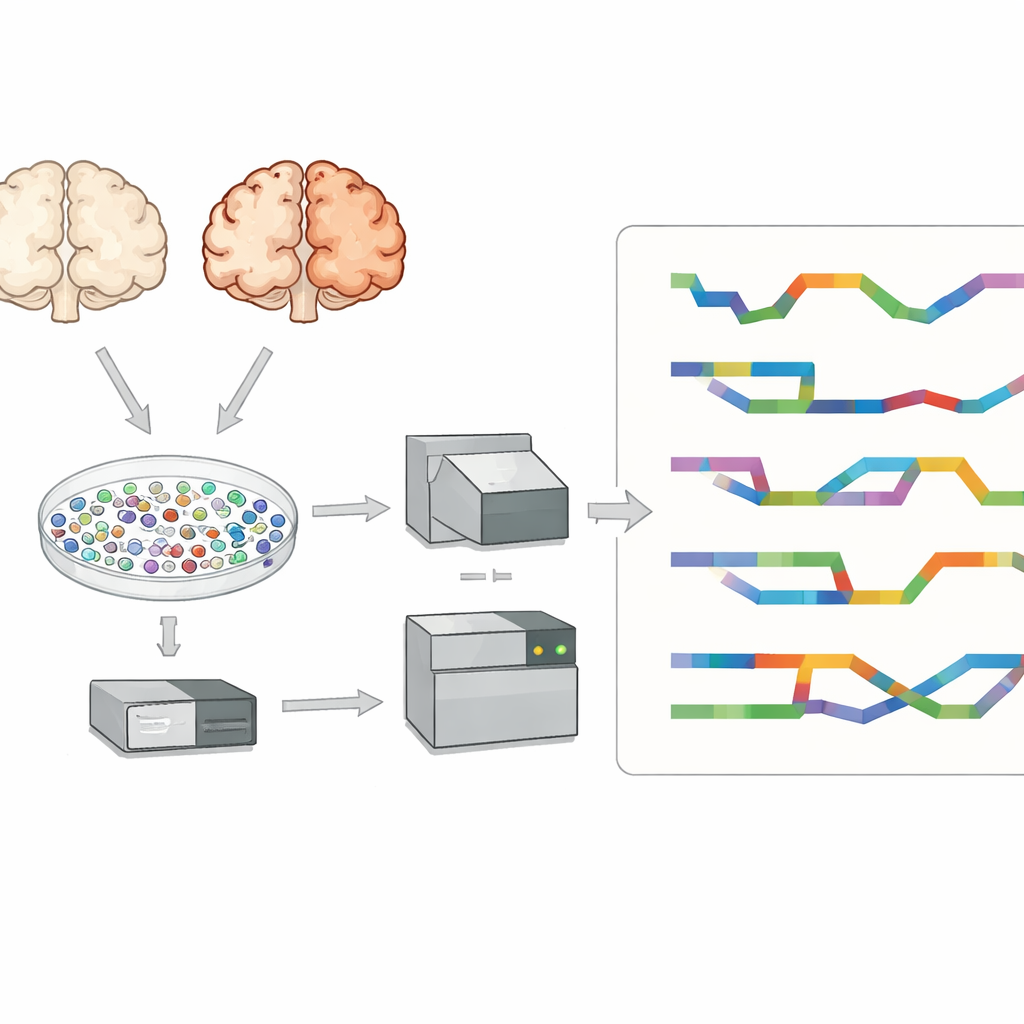
Uno sguardo dentro le singole cellule cerebrali
I ricercatori si sono concentrati sulla corteccia prefrontale, una regione importante per il pensiero e la memoria che è fortemente colpita nella malattia di Alzheimer. Hanno esaminato tessuto proveniente da otto persone con Alzheimer e sette senza la malattia. Invece di studiare tessuto mescolato, hanno isolato decine di migliaia di nuclei cellulari individuali e hanno catturato l’RNA presente in ciascuno. Questo ha permesso loro di identificare i principali tipi cellulari cerebrali—come neuroni eccitatori e inibitori, astrociti, microglia, oligodendrociti e i loro precursori—and di confrontare cervelli con e senza Alzheimer cellula per cellula, invece di come un segnale misto unico.
Combinare due potenze del sequenziamento
La maggior parte degli studi a singola cellula utilizza il sequenziamento a letture corte, che legge bene piccoli frammenti di RNA ma fatica a ricostruire trascritti a lunghezza intera e i loro schemi di splicing esatti. Per superare questo limite, il team ha usato una tecnologia a letture lunghe chiamata PacBio Kinnex insieme ai metodi standard a letture corte. Kinnex funziona collegando molte molecole di cDNA capo a coda in modo che una singola corsa a lettura lunga catturi molte copie di RNA a lunghezza intera. Dopo il sequenziamento, queste letture lunghe sono state digitalmente separate in molecole individuali e poi abbinate ai codici a barre cellulari originali. Questo approccio ha prodotto circa 70.000 nuclei singoli con identità del tipo cellulare e informazioni dettagliate sugli isoformi, fornendo una visione insolitamente ricca della diversità dell’RNA nel cervello con Alzheimer.
Un vasto paesaggio di varianti di RNA
Dai dati, gli scienziati hanno rilevato più di 850.000 isoformi di RNA e hanno poi applicato filtri rigorosi per definire circa 53.500 isoformi “sicuri” osservati in modo robusto attraverso più cervelli. La maggior parte apparteneva a tipi di trascritti noti, ma quasi 4.000 erano chiaramente nuovi, rivelando che anche la corteccia umana ben studiata nasconde ancora varianti di RNA inaspettate. Molti geni producevano più isoformi, con alcuni—come il gene dystonin—che mostravano dozzine di versioni distinte. Il team ha osservato anche isoformi rari con giunzioni interne insolite, alcune potenzialmente collegate a un processo chiamato ricombinazione genica somatica descritto in precedenza nell’Alzheimer, sottolineando quanto possa essere diversificato e dinamico l’RNA cerebrale.
Cambiamenti nascosti che i soli geni non possono mostrare
Quando gli scienziati hanno confrontato cervelli con Alzheimer e non malati a livello di gene usando i dati a letture corte, hanno osservato schemi familiari: le vie infiammatorie risultavano più attive in microglia e astrociti, e i geni legati alle sinapsi e all’elaborazione dell’amiloide erano alterati nei neuroni e negli oligodendrociti. Ma l’analisi degli isoformi con letture lunghe ha rivelato cambiamenti che le medie a livello di gene hanno completamente perso. Alcuni geni mostravano poca o nessuna differenza complessiva nell’espressione, eppure isoformi specifici erano fortemente aumentati o diminuiti o addirittura “scambiati” in abbondanza relativa nell’Alzheimer. Per esempio, il gene SEPTIN4, coinvolto nello scheletro interno della cellula e presente in aggregati proteici nelle malattie neurodegenerative, aveva un isoforma ridotta e un’altra aumentata, annullandosi a vicenda a livello genico. Un altro gene, CHI3L1—che codifica la proteina legata all’infiammazione YKL-40—era sovraespresso negli astrociti principalmente attraverso un singolo isoforma nuovo con segmenti trattenuti, mentre il trascritto noto restava invariato. Spostamenti a livello di isoformi simili sono stati osservati per geni correlati all’AD come APOE, BIN1, APP e MAPT, spesso in maniera specifica per tipo cellulare.
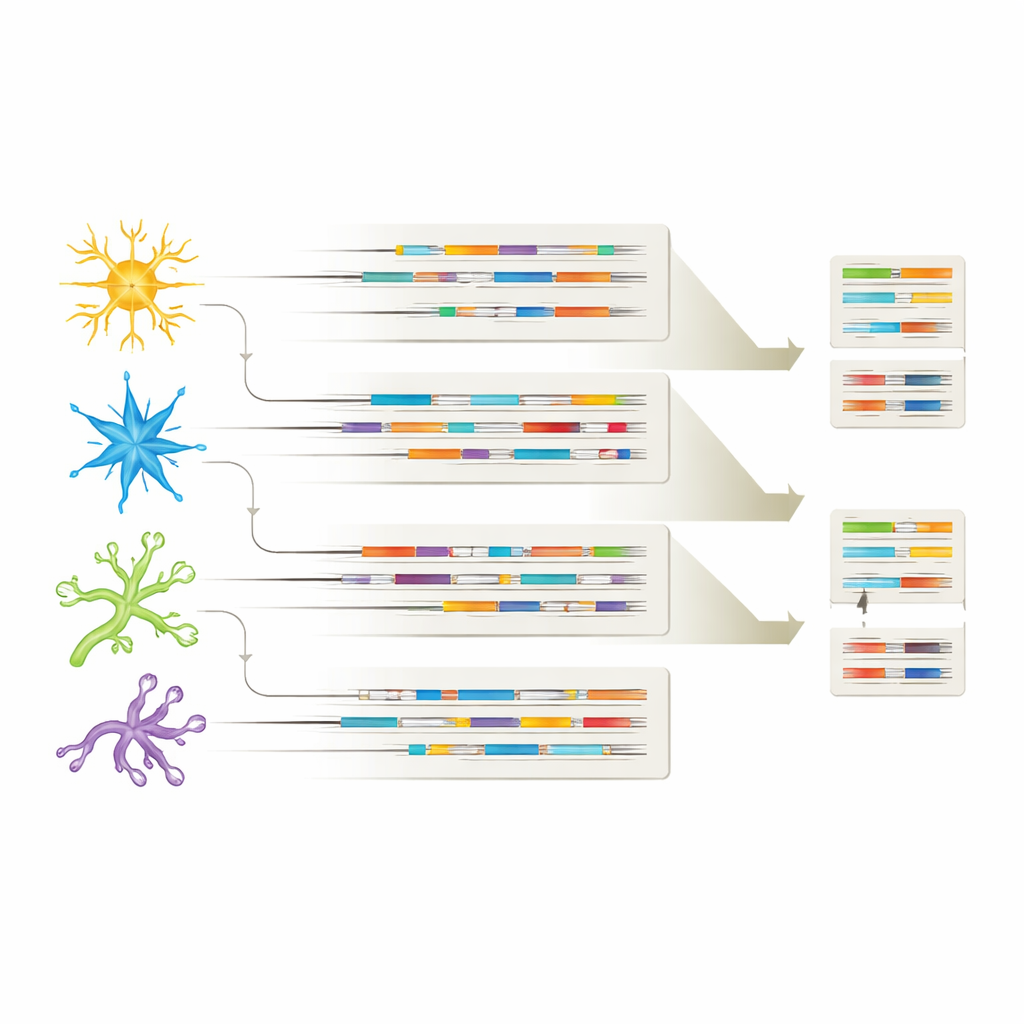
Tipi cellulari diversi, firme di RNA diverse
Collegando ogni isoforma al tipo cellulare di origine, lo studio ha mostrato che ogni grande popolazione cellulare cerebrale porta la propria distintiva “impronta” di isoformi. Molte varianti di RNA erano condivise tra neuroni e cellule gliali, ma ogni tipo cellulare esprimeva anche isoformi unici, suggerendo ruoli specializzati nella salute e nella malattia. In alcuni casi, certi isoformi apparivano solo nei cervelli con Alzheimer o solo in particolari tipi cellulari, come varianti specifiche di APP nei neuroni inibitori o un isoforma di CHI3L1 limitato agli astrociti. Questi schemi suggeriscono che non solo quali geni sono attivi o spenti, ma quali versioni specifiche di RNA vengono usate in ciascun tipo cellulare, possono influenzare come si sviluppa l’Alzheimer e quali cellule sono più vulnerabili.
Cosa significa per la comprensione e il trattamento dell’Alzheimer
Questo lavoro mostra che il cervello con Alzheimer non sta solo malinterpretando i geni, ma rimescola anche la struttura fine dei suoi messaggi RNA in modi che differiscono tra i tipi cellulari. Il sequenziamento singola-cellula a letture lunghe mette in luce cambiamenti di isoformi legati alla malattia che sarebbero invisibili negli studi convenzionali a livello di gene. Alcune di queste varianti di RNA appena identificate, come isoformi alterati di SEPTIN4 e CHI3L1, potrebbero avere ruoli diretti nel danno cerebrale o servire come biomarcatori più precisi di infiammazione e degenerazione. Pur richiedendo ulteriori ricerche per testarne le funzioni e l’utilità clinica, questo studio chiarisce che i futuri sforzi per comprendere—e eventualmente trattare—l’Alzheimer dovranno considerare non solo i geni, ma l’intera diversità dei loro isoformi di RNA nelle singole cellule cerebrali.
Citazione: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
Parole chiave: Malattia di Alzheimer, Splicing dell'RNA, Sequenziamento singola-cellula, Isoformi di RNA, Neuroinfiammazione