Clear Sky Science · fr
Diversité des isoformes d’ARN, variantes d’épissage et basculements dans les cellules individuelles du cerveau atteint d’Alzheimer
Pourquoi de minuscules différences d’ARN comptent en cas d’Alzheimer
La maladie d’Alzheimer est généralement décrite en termes de plaques, d’emmêlements et de neurones mourants. Mais sous ces images microscopiques se cache une couche encore plus fine de complexité : les messages ARN qui indiquent à chaque cellule cérébrale quelles protéines produire. Cette étude explore cette couche cachée à résolution unicellulaire et montre que ce ne sont pas seulement les gènes, mais les « versions » exactes de l’ARN de chaque gène — appelées isoformes — qui sont largement altérées dans les cerveaux d’Alzheimer. Comprendre ces changements subtils des messages pourrait aider à expliquer pourquoi certaines cellules cérébrales échouent et pourrait révéler de nouveaux biomarqueurs ou cibles médicamenteuses.
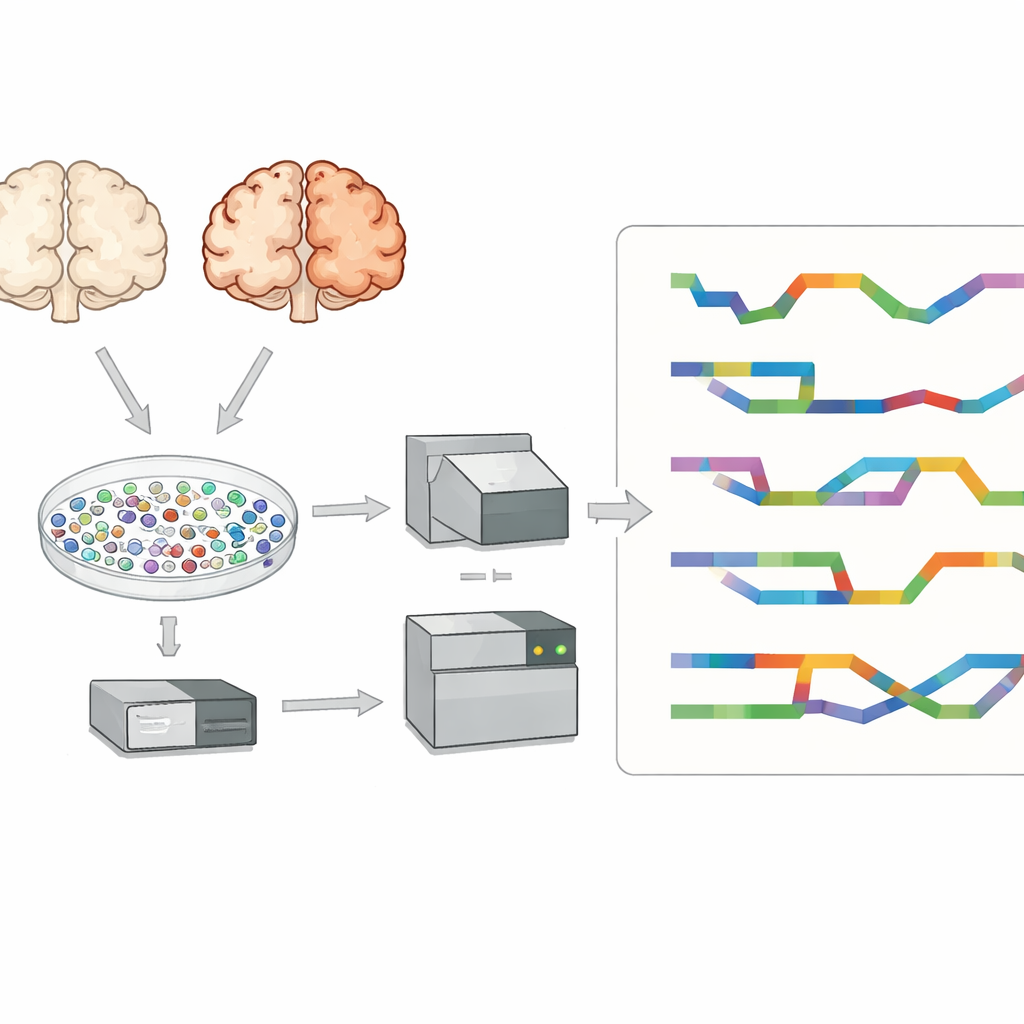
Regarder à l’intérieur des cellules cérébrales individuelles
Les chercheurs se sont concentrés sur le cortex préfrontal, une région cérébrale importante pour la pensée et la mémoire, fortement touchée dans la maladie d’Alzheimer. Ils ont examiné des tissus provenant de huit personnes atteintes d’Alzheimer et de sept personnes non atteintes. Plutôt que d’étudier un tissu mélangé, ils ont isolé des dizaines de milliers de noyaux cellulaires individuels et capturé l’ARN présent dans chacun. Cela leur a permis d’identifier les principaux types cellulaires du cerveau — tels que les neurones excitateurs et inhibiteurs, les astrocytes, les microglies, les oligodendrocytes et leurs précurseurs — et de comparer les cerveaux d’Alzheimer et non malades type cellulaire par type cellulaire, plutôt que comme un signal global mélangé.
Combiner deux puissances de séquençage
La plupart des études unicellulaires utilisent le séquençage à lectures courtes, qui lit bien de petits fragments d’ARN mais a du mal à reconstituer des transcrits complets et leurs schémas d’épissage exacts. Pour surmonter cela, l’équipe a utilisé une technologie à lectures longues appelée PacBio Kinnex en parallèle avec des méthodes standard à lectures courtes. Kinnex fonctionne en reliant de nombreuses molécules d’ADNc bout à bout de sorte qu’un seul run à lectures longues capture de nombreuses copies d’ARN en longueur entière. Après séquençage, ces lectures longues ont été découpées numériquement en molécules individuelles, puis associées aux codes-barres cellulaires d’origine. Cette approche a produit environ 70 000 noyaux individuels avec à la fois l’identité du type cellulaire et des informations détaillées sur les isoformes, offrant une vue exceptionnellement riche de la diversité des ARN dans le cerveau d’Alzheimer.
Un vaste paysage de variantes d’ARN
À partir de ces données, les scientifiques ont détecté plus de 850 000 isoformes d’ARN puis ont appliqué des filtres stricts pour définir environ 53 500 isoformes « fiables » observées de manière robuste dans plusieurs cerveaux. La plupart appartenaient à des types de transcrits connus, mais près de 4 000 étaient clairement nouveaux, révélant que même le cortex humain bien étudié cache encore des variantes d’ARN inattendues. De nombreux gènes produisaient plusieurs isoformes, certains — comme le gène dystonine — présentant des dizaines de versions distinctes. L’équipe a aussi observé des isoformes rares avec des jonctions internes inhabituelles, certaines potentiellement liées à un processus appelé recombinaison génique somatique décrit auparavant dans Alzheimer, soulignant à quel point l’ARN cérébral peut être divers et dynamique.
Des changements cachés que le seul niveau gène ne peut montrer
Lorsque les scientifiques ont comparé les cerveaux d’Alzheimer et non malades au niveau des gènes en utilisant des données à lectures courtes, ils ont observé des schémas familiers : les voies inflammatoires étaient plus actives dans les microglies et les astrocytes, et les gènes liés aux synapses et au traitement de l’amyloïde étaient altérés dans les neurones et les oligodendrocytes. Mais l’analyse des isoformes par lectures longues a révélé des changements que les moyennes au niveau des gènes manquaient complètement. Certains gènes montraient peu ou pas de différence d’expression globale, et pourtant des isoformes spécifiques étaient fortement augmentées ou diminuées, voire « basculées » en abondance relative dans Alzheimer. Par exemple, le gène SEPTIN4, impliqué dans le cytosquelette intracellulaire et retrouvé dans des agrégats protéiques dans les maladies neurodégénératives, présentait une isoforme réduite et une autre augmentée, s’annulant au niveau du gène. Un autre gène, CHI3L1 — qui code pour la protéine liée à l’inflammation YKL-40 — était surexprimé dans les astrocytes principalement via une isoforme nouvelle avec segments retenus, tandis que le transcrit connu restait inchangé. Des basculements au niveau des isoformes similaires ont été observés pour des gènes liés à la MA tels que APOE, BIN1, APP et MAPT, souvent de façon spécifique à un type cellulaire.
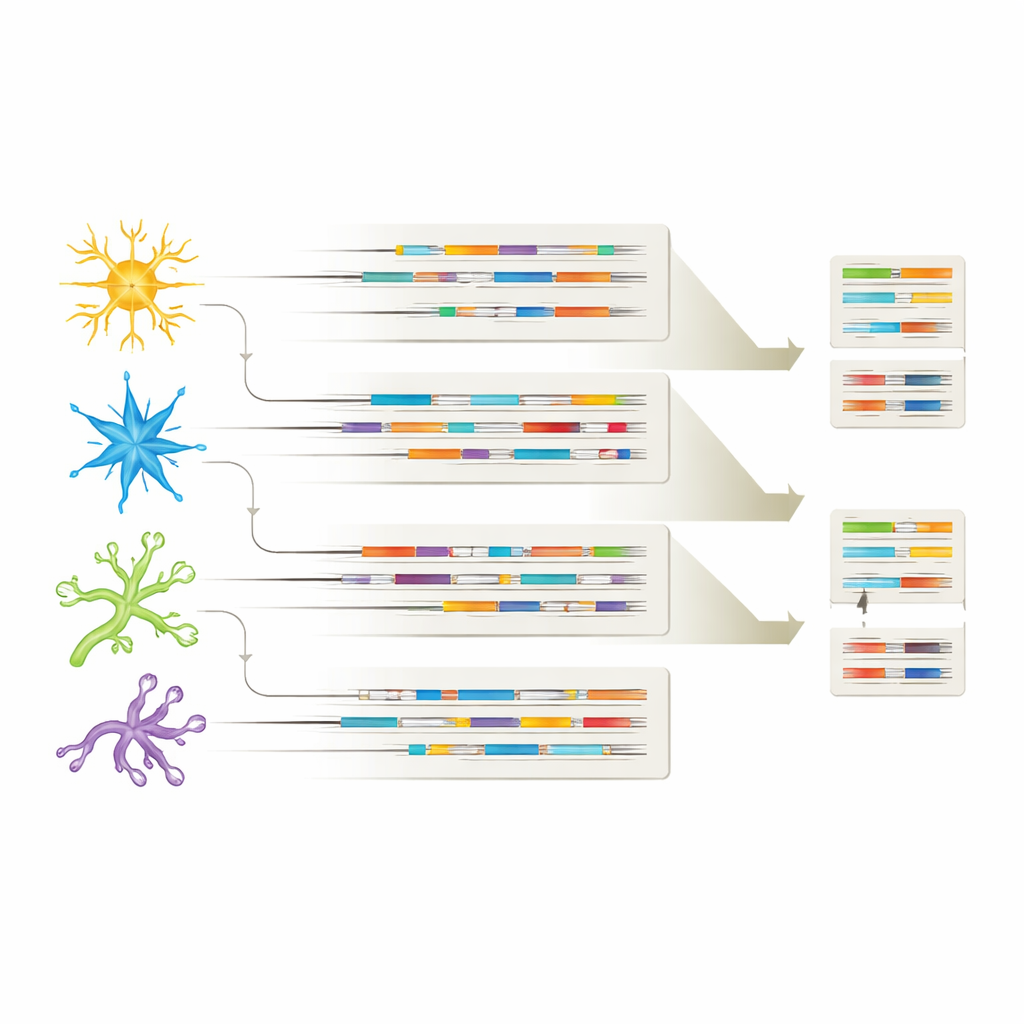
Différents types cellulaires, différentes signatures d’ARN
En reliant chaque isoforme à son type cellulaire d’origine, l’étude a montré que chaque grande population cellulaire cérébrale porte son propre « empreinte » d’isoformes. De nombreuses variantes d’ARN étaient partagées entre neurones et cellules gliales, mais chaque type cellulaire exprimait aussi des isoformes uniques, suggérant des rôles spécialisés en santé et en maladie. Dans certains cas, certaines isoformes apparaissaient uniquement dans les cerveaux d’Alzheimer ou uniquement dans des types cellulaires particuliers, comme des variants spécifiques d’APP dans des neurones inhibiteurs ou une isoforme de CHI3L1 limitée aux astrocytes. Ces motifs suggèrent que non seulement le fait qu’un gène soit actif ou non, mais aussi quelle version d’ARN est utilisée dans chaque type cellulaire, peut influencer le développement de la maladie d’Alzheimer et la vulnérabilité des cellules.
Ce que cela signifie pour comprendre et traiter Alzheimer
Ce travail montre que le cerveau d’Alzheimer ne se contente pas de mal utiliser des gènes, il remixe aussi la structure fine de ses messages ARN de façons différentes selon les types cellulaires. Le séquençage unicellulaire à lectures longues met en lumière des changements d’isoformes liés à la maladie qui resteraient invisibles dans les études conventionnelles au niveau des gènes. Certaines de ces variantes d’ARN nouvellement identifiées, comme des isoformes altérées de SEPTIN4 et CHI3L1, pourraient jouer un rôle direct dans les lésions cérébrales ou servir de biomarqueurs plus précis d’inflammation et de dégénérescence. Bien que des recherches supplémentaires soient nécessaires pour tester leurs fonctions et leur utilité clinique, cette étude montre clairement que les efforts futurs pour comprendre — et éventuellement traiter — la maladie d’Alzheimer devront prendre en compte non seulement les gènes, mais aussi la pleine diversité de leurs isoformes d’ARN dans les cellules cérébrales individuelles.
Citation: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
Mots-clés: Maladie d’Alzheimer, Épissage de l’ARN, Séquençage unicellulaire, Isoformes d’ARN, Neuroinflammation