Clear Sky Science · ar
تنوع متغيرات الـRNA، اختلافات الطيّ والتبديل في الخلايا المفردة في دماغ مرض ألزهايمر
لماذا تهم الاختلافات الصغيرة في الـRNA في ألزهايمر
عادةً ما يوصف مرض ألزهايمر من حيث اللويحات والتشابكات وخلايا العصب المتحللة. لكن تحت تلك الصور الميكروسكوبية يكمن طبقة أدق من التعقيد: رسائل الـRNA التي تخبر كل خلية دماغية أي البروتينات تصنع. هذه الدراسة تلقي نظرة على تلك الطبقة الخفية بدقة خلية مفردة، مُظهِرة أنه ليس فقط الجينات، بل الإصدارات الدقيقة من RNA لكل جين — المسماة الأيزوفورمات — تتغير على نحو واسع في أدمغة المصابين بألزهايمر. فهم هذه التغييرات الطفيفة في الرسائل قد يساعد في تفسير سبب تراجع خلايا دماغية معينة وقد يكشف عن مؤشرات حيوية أو أهداف دوائية جديدة.
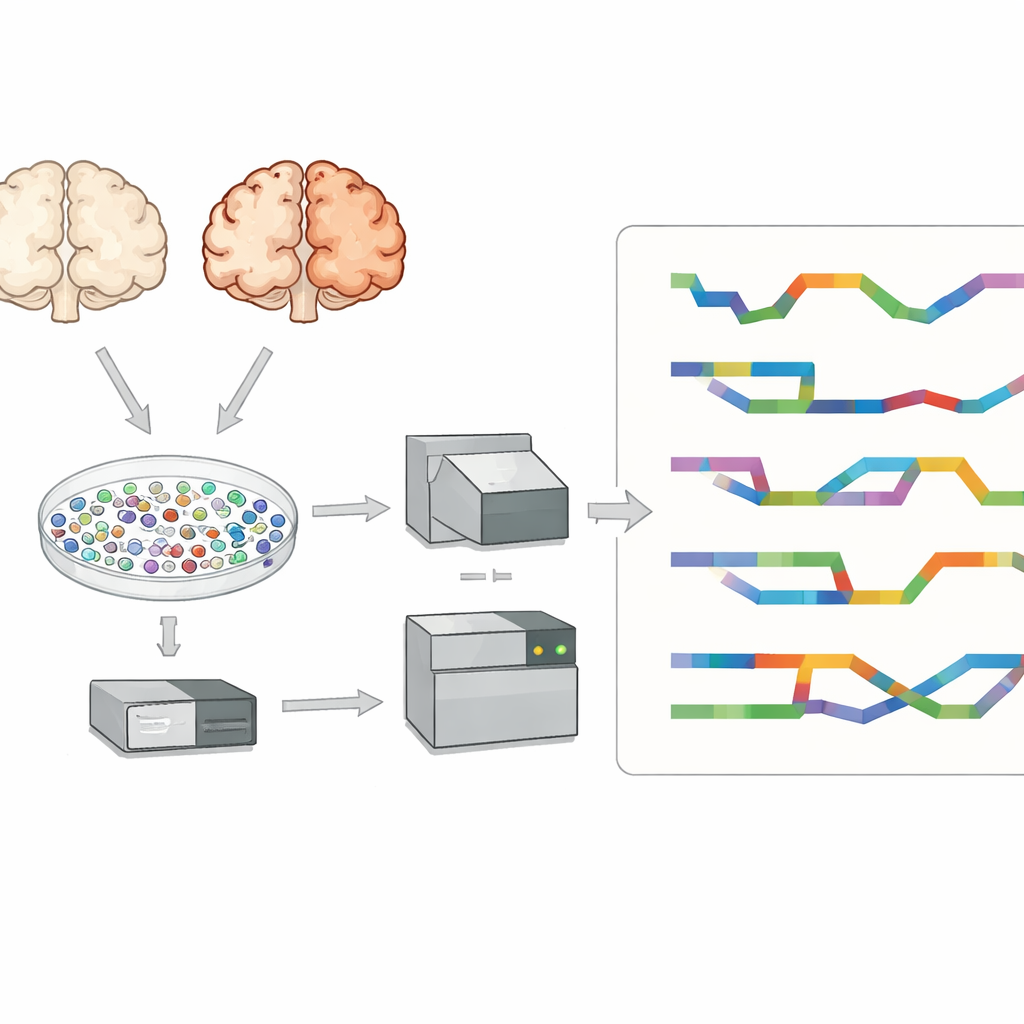
نظرة داخل الخلايا الدماغية المفردة
ركّز الباحثون على القشرة أمام الجبهية، منطقة دماغية مهمة للتفكير والذاكرة وتتأثر بشدة بمرض ألزهايمر. فحصوا أنسجة من ثمانية أشخاص كانوا يعانون ألزهايمر وسبعة لم يعانوا منه. بدلاً من دراسة نسيج ممزوج، عزلوا عشرات الآلاف من نوى الخلايا المفردة والتقطوا الـRNA داخل كل نواة. سمح ذلك بتحديد الأنواع الرئيسية لخلايا الدماغ — مثل الخلايا العصبية المثيرة والمثبطة، والخلايا النجمية، والماكروفاجات الدبقية الدقيقة، وخلايا أوليجوديندروسايت وخلاياها السلفية — ومقارنة أدمغة المصابين وغير المصابين طائفياً بدلًا من إشارة مختلطة واحدة.
دمج نوعين من قوة التسلسل
تستخدم معظم دراسات الخلايا المفردة تسلسل القراءات القصيرة، الذي يقرأ مقاطع صغيرة من الـRNA جيداً لكنه يواجه صعوبة في إعادة بناء النصوص الكاملة وأنماط الطيّ الدقيقة. للتغلب على ذلك، استخدم الفريق تقنية ذات قراءة طويلة تسمى PacBio Kinnex إلى جانب طرق القراءات القصيرة القياسية. تعمل Kinnex عن طريق ربط العديد من جزيئات cDNA في نهاياتها بحيث تلتقط قراءة طويلة واحدة عدة نسخ كاملة الطول من الـRNA. بعد التسلسل، قُطعت هذه القراءات الطويلة رقمياً إلى جزيئات فردية، ثم تم مطابقتها مع شفرات الخلايا الأصلية. أنتج هذا النهج حوالي 70,000 نواة مفردة تحمل كل منها هوية نوع الخلية ومعلومات تفصيلية عن الأيزوفورمات، مما وفر رؤية غير عادية لتنوع الـRNA في دماغ ألزهايمر.
مشهد واسع من متغيرات الـRNA
من هذه البيانات، اكتشف العلماء أكثر من 850,000 أيزوفورم لـRNA ثم طبقوا مرشحات صارمة لتحديد نحو 53,500 أيزوفورم "موثوق" لوحظت بقوة عبر أدمغة متعددة. معظمها انتمت إلى أنواع نصية معروفة، لكن ما يقرب من 4,000 كانت جديدة بوضوح، كاشفة أن القشرة البشرية — حتى المدروسة جيداً — لا تزال تخفي متغيرات RNA غير متوقعة. أنتجت العديد من الجينات عدة أيزوفورمات، مع ظهور بعض الجينات — مثل جين dystonin — بعشرات النسخ المميزة. كما رصد الفريق أيزوفورمات نادرة ذات وصلات داخلية غير اعتيادية، بعضها قد يرتبط بعملية تسمى إعادة تركيب الجينات الجسمانية التي وُصفت سابقاً في ألزهايمر، مما يؤكد مدى تنوع وديناميكية RNA الدماغ.
تغييرات مخفية لا تُظهِرها الجينات وحدها
عندما قارن العلماء بين أدمغة المصابين وغير المصابين على مستوى الجين باستخدام بيانات القراءات القصيرة، رأوا أنماطاً مألوفة: كانت المسارات الالتهابية أكثر نشاطاً في الخلايا الدبقية الدقيقة والخلايا النجمية، وتغيرت الجينات المرتبطة بالمشابك ومعالجة الأميلويد في الخلايا العصبية والأوليغوديندروسايت. لكن تحليل الأيزوفورمات بالقراءة الطويلة كشف تغييرات كانت المتوسطات على مستوى الجين تغفلها تماماً. أظهرت بعض الجينات اختلافاً ضئيلاً أو لا يظهر اختلاف إجمالي في التعبير، ومع ذلك كانت أيزوفورمات محددة قد ازداد أو انخفضت بشدة أو حتى "تبدلت" في وفرتها النسبية في ألزهايمر. على سبيل المثال، كان للجين SEPTIN4، المتورط في هيكل الخلية الداخلي والموجود في تجمعات بروتينية بأمراض التنكس العصبي، أيزوفورم واحد منخفض والآخر مرتفع، مما ألغى بعضهما عند مستوى الجين. جين آخر، CHI3L1 — الذي يشفر البروتين المرتبط بالالتهاب YKL-40 — ارتفع في الخلايا النجمية بشكل رئيسي من خلال أيزوفورم جديد واحد مع أجزاء محتجزة، بينما ظل النص المعروف دون تغيير. لوحظت تحولات على مستوى الأيزوفورمات مماثلة لجينات مرتبطة بألزهايمر مثل APOE وBIN1 وAPP وMAPT، وغالباً ما كانت بطريقة خاصة بنوع الخلية.
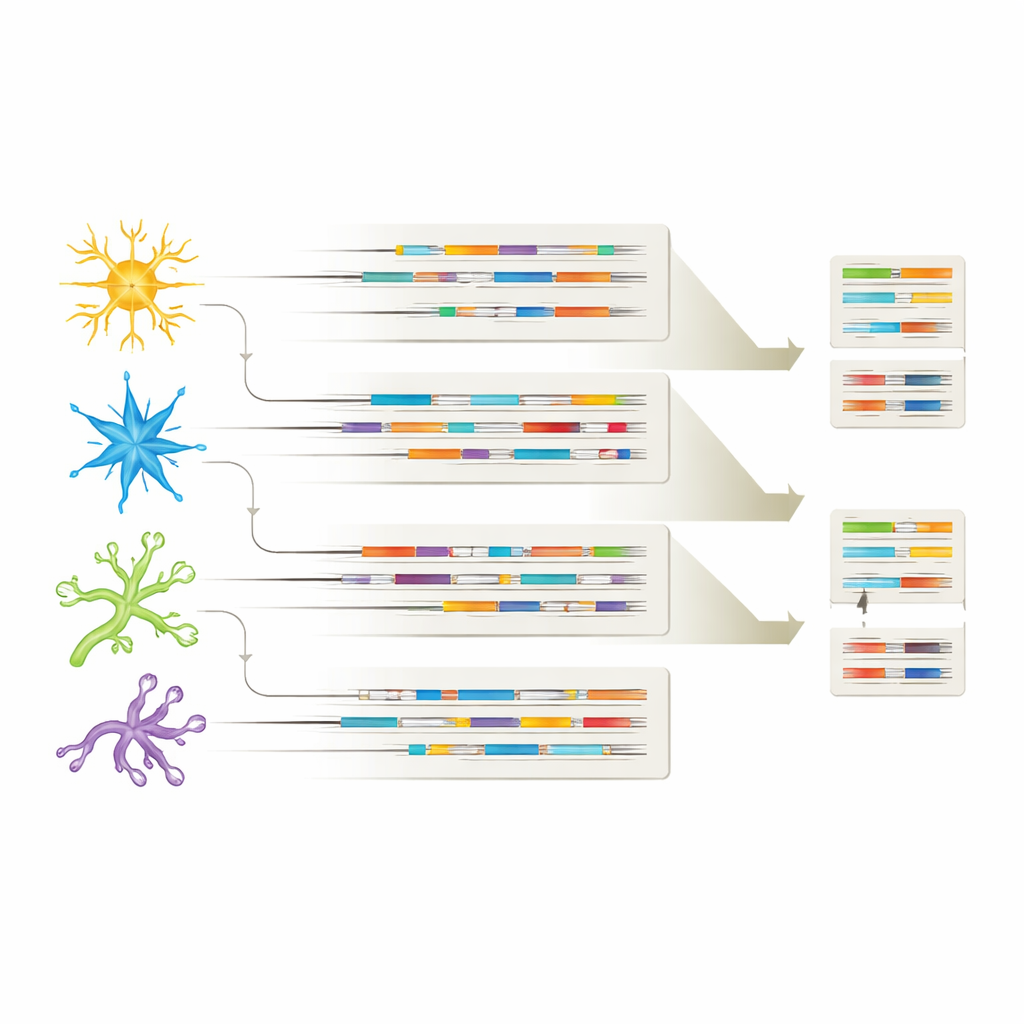
أنواع خلايا مختلفة، توقيعات RNA مختلفة
بربط كل أيزوفورم بنوع الخلية المنبع، أظهرت الدراسة أن كل مجموعة خلوية رئيسية في الدماغ تحمل "بصمة" أيزوفورم خاصة بها. تم مشاركة العديد من متغيرات الـRNA بين الخلايا العصبية والخلايا الدبقية، لكن كل نوع خلية أيضاً عبّر عن أيزوفورمات فريدة، مما يوحي بأدوار متخصصة في الصحة والمرض. في بعض الحالات، ظهرت أيزوفورمات معينة فقط في أدمغة ألزهايمر أو فقط في أنواع خلية معينة، مثل متغيرات APP محددة في الخلايا العصبية المثبطة أو أيزوفورم CHI3L1 مقصور على الخلايا النجمية. تشير هذه الأنماط إلى أن ليس فقط الجينات المشغلة أو المطفأة مهمة، بل أيضاً النسخ المحددة من RNA المستخدمة في كل نوع خلية قد تشكّل كيفية تطور ألزهايمر والخلايا الأكثر عرضة للخطر.
ما الذي يعنيه هذا لفهم وعلاج ألزهايمر
تُظهر هذه الدراسة أن دماغ ألزهايمر لا يخطئ فقط في استعمال الجينات، بل يعيد مزج البنية الدقيقة لرسائل الـRNA بطرق تختلف بين أنواع الخلايا. يكشف التسلسل طويل القراءة على مستوى الخلية المفردة تغييرات في الأيزوفورمات المرتبطة بالمرض كانت ستظل مخفية في دراسات المستوى الجيني التقليدية. قد تلعب بعض هذه المتغيرات المكتشفة حديثاً، مثل أيزوفورمات متغيرة من SEPTIN4 وCHI3L1، أدواراً مباشرة في تلف الدماغ أو تعمل كمؤشرات حيوية أكثر دقة للالتهاب والتنكس. ومع أن هناك حاجة لمزيد من الأبحاث لاختبار وظائفها وفائدتها السريرية، تُبرز هذه الدراسة بوضوح أن الجهود المستقبلية لفهم — وفي النهاية علاج — ألزهايمر ستحتاج للنظر ليس فقط إلى الجينات، بل إلى التنوع الكامل لأيزوفورمات الـRNA في الخلايا الدماغية المفردة.
الاستشهاد: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
الكلمات المفتاحية: مرض ألزهايمر, طيّ الـRNA, تسلسل خلية مفردة, أيزو فورمات الـRNA, الالتهاب العصبي