Clear Sky Science · pt
Diversidade de isoformas de RNA, variantes de splicing e troca em células únicas do cérebro com doença de Alzheimer
Por que pequenas diferenças no RNA importam na doença de Alzheimer
A doença de Alzheimer costuma ser descrita em termos de placas, emaranhados e morte de neurônios. Mas sob essas imagens microscópicas existe uma camada ainda mais fina de complexidade: as mensagens de RNA que dizem a cada célula cerebral quais proteínas produzir. Este estudo espreita essa camada oculta em resolução de célula única, mostrando que não são apenas os genes, mas as exatas “versões” do RNA de cada gene — chamadas isoformas — que estão extensamente alteradas em cérebros com Alzheimer. Compreender essas sutis mudanças nas mensagens pode ajudar a explicar por que certas células cerebrais falham e pode revelar novos biomarcadores ou alvos terapêuticos.
Observando o interior de células cerebrais individuais
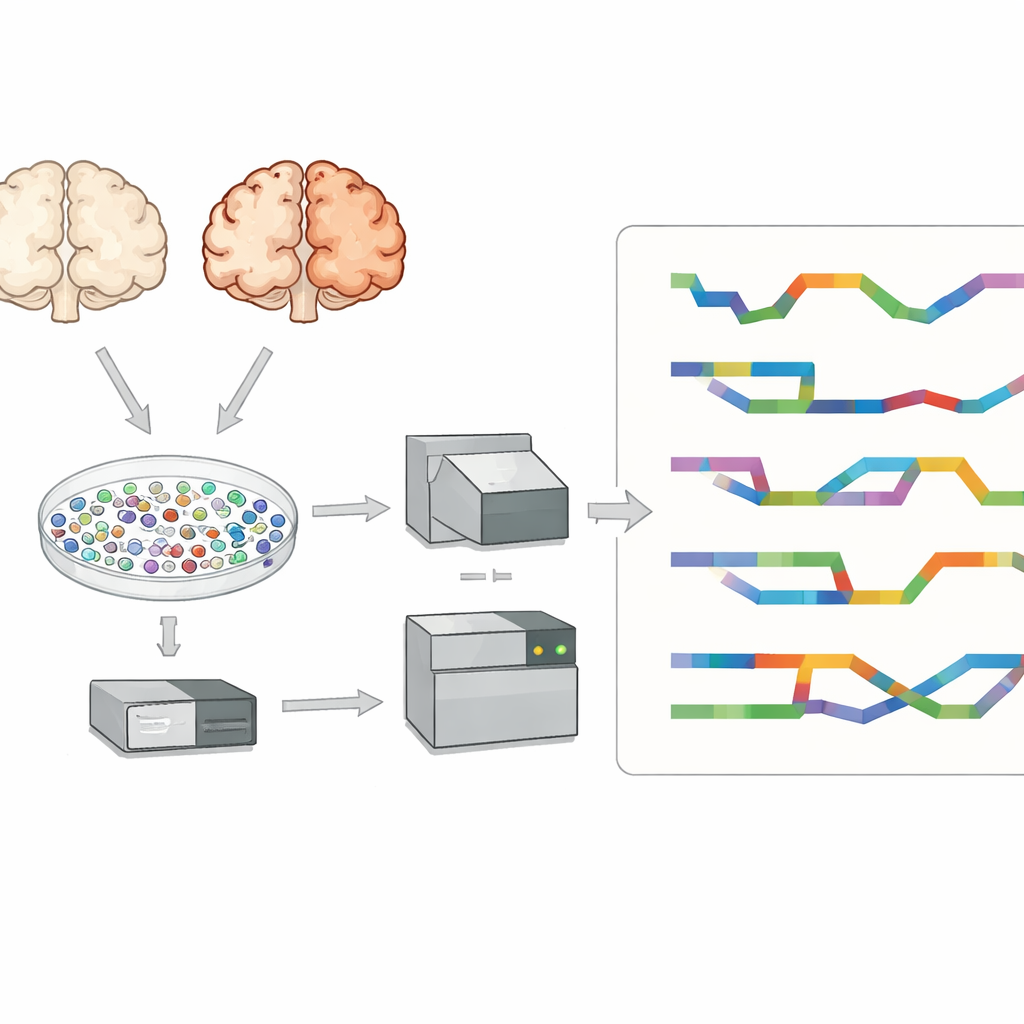
Os pesquisadores focaram no córtex pré-frontal, uma região cerebral importante para pensamento e memória que é fortemente afetada na doença de Alzheimer. Eles examinaram tecido de oito pessoas com Alzheimer e sete sem a doença. Em vez de estudar tecido misturado, isolaram dezenas de milhares de núcleos celulares individuais e capturaram o RNA dentro de cada um. Isso permitiu identificar os principais tipos celulares cerebrais — como neurônios excitatórios e inibitórios, astrócitos, microglia, oligodendrócitos e seus precursores — e comparar cérebros com Alzheimer e sem a doença tipo celular por tipo celular, em vez de um sinal misturado único.
Combinando dois tipos de poder de sequenciamento
A maioria dos estudos de célula única usa sequenciamento de leituras curtas, que lê bem pequenos fragmentos de RNA, mas tem dificuldade para reconstruir transcritos de comprimento total e seus padrões exatos de splicing. Para superar isso, a equipe usou uma tecnologia de leituras longas chamada PacBio Kinnex juntamente com métodos padrão de leituras curtas. O Kinnex funciona ligando muitas moléculas de cDNA de ponta a ponta para que uma única corrida de leitura longa capture muitas cópias de RNA de comprimento total. Após o sequenciamento, essas leituras longas foram digitalmente recortadas de volta em moléculas individuais e, então, associadas às etiquetas de célula originais. Essa abordagem produziu cerca de 70.000 núcleos únicos com identidade de tipo celular e informação detalhada de isoformas, oferecendo uma visão excepcionalmente rica da diversidade de RNA no cérebro com Alzheimer.
Uma vasta paisagem de variantes de RNA
A partir desses dados, os cientistas detectaram mais de 850.000 isoformas de RNA e então aplicaram filtros rígidos para definir aproximadamente 53.500 isoformas "confiáveis" que foram observadas de forma robusta em vários cérebros. A maioria pertencia a tipos de transcritos conhecidos, mas quase 4.000 eram claramente novos, revelando que mesmo o córtex humano bem estudado ainda esconde variantes inesperadas de RNA. Muitos genes produziram múltiplas isoformas, com alguns — como o gene dystonin — exibindo dezenas de versões distintas. A equipe também observou isoformas raras com junções internas incomuns, algumas potencialmente ligadas a um processo chamado recombinação somática de genes descrito anteriormente em Alzheimer, ressaltando quão diverso e dinâmico o RNA cerebral pode ser.
Mudanças ocultas que os genes sozinhos não mostram
Quando os cientistas compararam cérebros com Alzheimer e sem a doença ao nível do gene usando dados de leitura curta, viram padrões familiares: vias inflamatórias estavam mais ativas em microglia e astrócitos, e genes relacionados a sinapses e processamento de amiloide estavam alterados em neurônios e oligodendrócitos. Mas a análise de isoformas por leituras longas revelou mudanças que as médias ao nível do gene perderam completamente. Alguns genes mostraram pouca ou nenhuma diferença geral na expressão, ainda que isoformas específicas estivessem fortemente aumentadas ou diminuídas ou até “trocaram” em abundância relativa no Alzheimer. Por exemplo, o gene SEPTIN4, envolvido na estrutura interna da célula e encontrado em agregados proteicos em doenças neurodegenerativas, tinha uma isoforma reduzida e outra aumentada, anulando-se ao nível do gene. Outro gene, CHI3L1 — que codifica a proteína ligada à inflamação YKL-40 — foi regulado positivamente em astrócitos principalmente por meio de uma única isoforma novel com segmentos retidos, enquanto o transcrito conhecido permaneceu inalterado. Mudanças semelhantes ao nível de isoforma foram observadas para genes relacionados ao Alzheimer, como APOE, BIN1, APP e MAPT, frequentemente de forma específica a tipos celulares.
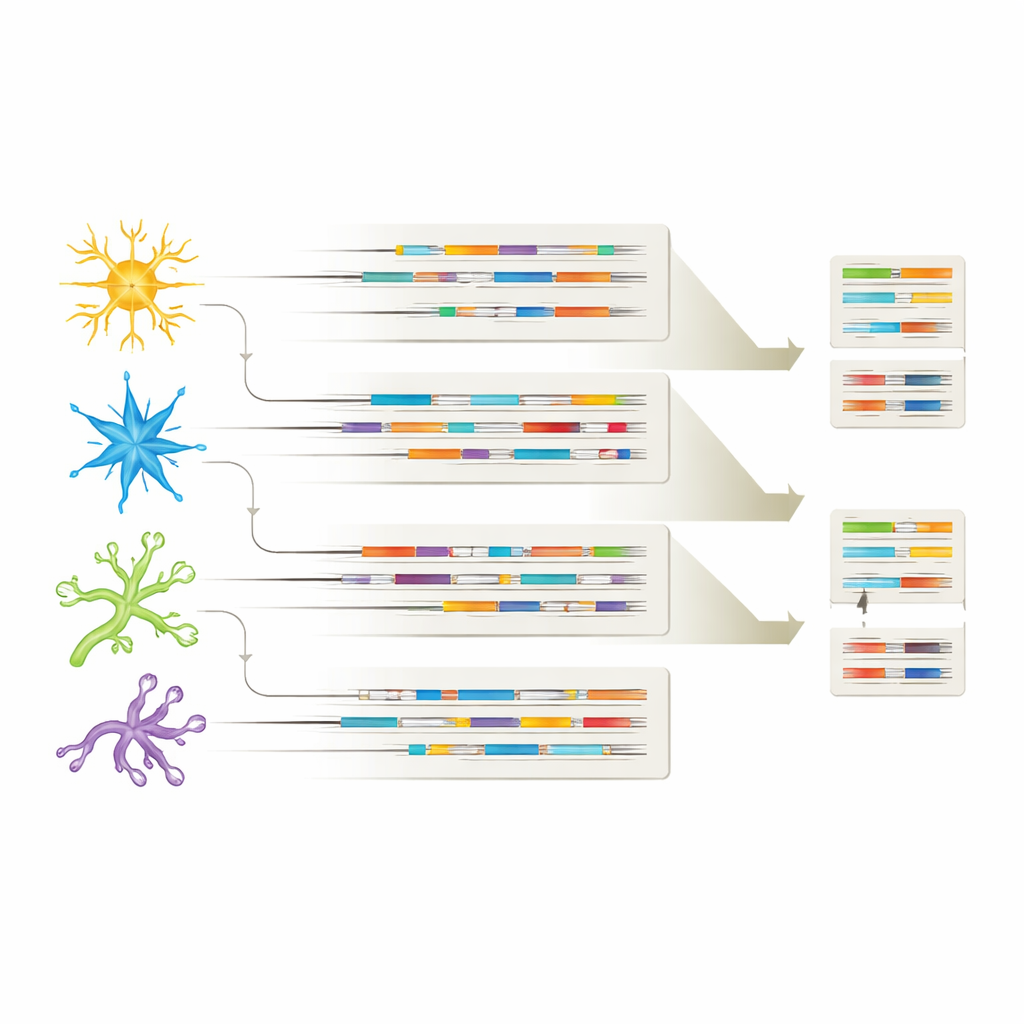
Tipos celulares diferentes, assinaturas de RNA diferentes
Ao vincular cada isoforma ao seu tipo celular de origem, o estudo mostrou que cada grande população celular cerebral carrega sua própria "impressão digital" de isoformas. Muitas variantes de RNA foram compartilhadas entre neurônios e células gliais, mas cada tipo celular também expressou isoformas únicas, sugerindo papéis especializados na saúde e na doença. Em alguns casos, certas isoformas apareceram apenas em cérebros com Alzheimer ou apenas em tipos celulares particulares, como variantes específicas de APP em neurônios inibitórios ou uma isoforma de CHI3L1 limitada a astrócitos. Esses padrões sugerem que não apenas quais genes estão ligados ou desligados, mas quais versões específicas de RNA são usadas em cada tipo celular podem moldar como o Alzheimer se desenvolve e quais células são mais vulneráveis.
O que isso significa para entender e tratar o Alzheimer
Este trabalho mostra que o cérebro com Alzheimer não está apenas fazendo uso incorreto dos genes, mas também remixando a estrutura fina de suas mensagens de RNA de maneiras que divergem entre os tipos celulares. O sequenciamento de célula única com leituras longas expõe mudanças de isoformas ligadas à doença que seriam invisíveis em estudos convencionais ao nível do gene. Algumas dessas variantes de RNA recém-identificadas, como isoformas alteradas de SEPTIN4 e CHI3L1, podem desempenhar papéis diretos no dano cerebral ou servir como biomarcadores mais precisos de inflamação e degeneração. Embora sejam necessárias mais pesquisas para testar suas funções e utilidade clínica, este estudo deixa claro que esforços futuros para entender — e eventualmente tratar — o Alzheimer precisarão considerar não apenas os genes, mas a diversidade completa de suas isoformas de RNA em células cerebrais individuais.
Citação: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
Palavras-chave: Doença de Alzheimer, splicing de RNA, sequenciamento de célula única, isoformas de RNA, neuroinflamação