Clear Sky Science · sv
RNA-isoformmångfald, splitsningsvarianter och växlingar i enskilda celler i Alzheimerhjärnan
Varför små RNA-skillnader spelar roll vid Alzheimer
Alzheimers sjukdom beskrivs vanligtvis med plack, trassel och döende nervceller. Men under dessa mikroskopbilder finns ett ännu finare skikt av komplexitet: RNA-budskapen som talar om för varje hjärncell vilka proteiner den ska tillverka. Denna studie skådar in i det dolda skiktet med enkelcellsupplösning och visar att det inte bara är generna utan också de exakta "versionerna" av varje gens RNA—så kallade isoformer—that är omfattande förändrade i Alzheimerhjärnor. Att förstå dessa subtila budskapsförändringar kan hjälpa till att förklara varför vissa hjärnceller sviktar och kan avslöja nya biomarkörer eller läkemedelsmål.
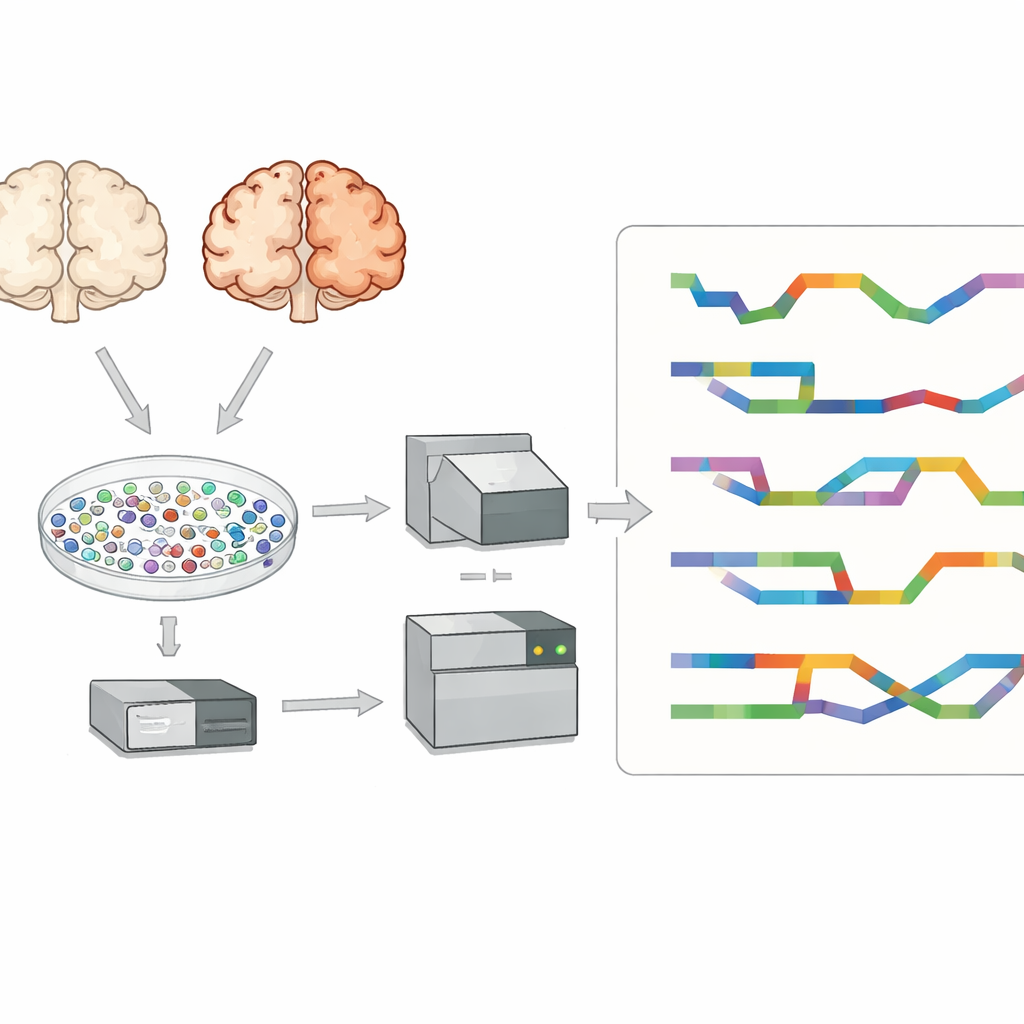
En titt inuti enskilda hjärnceller
Forskarna fokuserade på prefrontala cortex, en hjärnregion viktig för tänkande och minne som påverkas starkt vid Alzheimers sjukdom. De undersökte vävnad från åtta personer med Alzheimer och sju utan sjukdomen. Istället för att studera blandad vävnad isolerade de tiotusentals enskilda cellkärnor och fångade RNA i varje kärna. Detta gjorde det möjligt att identifiera huvudtyper av hjärnceller—såsom excitatoriska och inhibitoriska neuron, astrocyter, mikroglia, oligodendrocyter och deras prekursorer—och jämföra Alzheimer- och friska hjärnor celltyp för celltyp, istället för som en enda blandad signal.
Kombination av två typer av sekvenseringsstyrka
De flesta enkelcellsstudier använder kortläsningssekvensering, vilket läser små RNA-snuttar bra men har svårt att återskapa fullängds-transkript och deras exakta splitsningsmönster. För att komma runt detta använde teamet en långläsningsteknik kallad PacBio Kinnex tillsammans med standard kortläsningsmetoder. Kinnex fungerar genom att länka många cDNA-molekyler ända till ända så att en enda långläsning fångar många fullängds-RNA-kopior. Efter sekvensering delades dessa långa läsningar digitalt tillbaka till individuella molekyler och matchades sedan till ursprungliga cellstreckkoder. Detta tillvägagångssätt producerade cirka 70 000 enskilda kärnor med både celltypidentitet och detaljerad isoforminformation, vilket gav en ovanligt rik bild av RNA-mångfalden i Alzheimerhjärnan.
En vidsträckt landskap av RNA-varianter
Från dessa data upptäckte forskarna mer än 850 000 RNA-isoformer och tillämpade sedan strikta filter för att definiera omkring 53 500 "tillförlitliga" isoformer som observerades robust över flera hjärnor. De flesta tillhörde kända transkripttyper, men nästan 4 000 var tydligt nya, vilket visar att även välstuderad mänsklig cortex fortfarande döljer oväntade RNA-varianter. Många gener producerade flera isoformer, där vissa—som dystonin-genen—visade dussintals distinkta versioner. Teamet observerade också sällsynta isoformer med ovanliga interna junctions, några potentiellt kopplade till en process kallad somatisk genrekombination som tidigare beskrivits i Alzheimer, vilket understryker hur diversifierat och dynamiskt hjärnans RNA kan vara.
Dolda förändringar som gen-nivån inte kan visa
När forskarna jämförde Alzheimer- och friska hjärnor på gen-nivå med kortläsningsdata såg de bekanta mönster: inflammatoriska vägar var mer aktiva i mikroglia och astrocyter, och gener relaterade till synapser och amyloidprocessning var förändrade i neuroner och oligodendrocyter. Men analysen med långläsningsisoformer avslöjade förändringar som gen-nivåmedelvärden helt missade. Vissa gener visade liten eller ingen övergripande förändring i uttryck, ändå var specifika isoformer starkt upp- eller nedreglerade eller till och med "växlade" i relativ frekvens vid Alzheimer. Till exempel hade genen SEPTIN4, involverad i cellens interna skelett och funnen i proteinaggregat vid neurodegenerativa sjukdomar, en isoform minskad och en annan ökad, vilket utlöstes utanför varandra på gen-nivå. En annan gen, CHI3L1—som kodar för det inflammationkopplade proteinet YKL-40—var uppreglerad i astrocyter främst genom en enda ny isoform med behållna segment, medan det kända transkriptet förblev oförändrat. Liknande isoform-förskjutningar sågs för AD-relaterade gener såsom APOE, BIN1, APP och MAPT, ofta på ett celltypsspecifikt sätt.
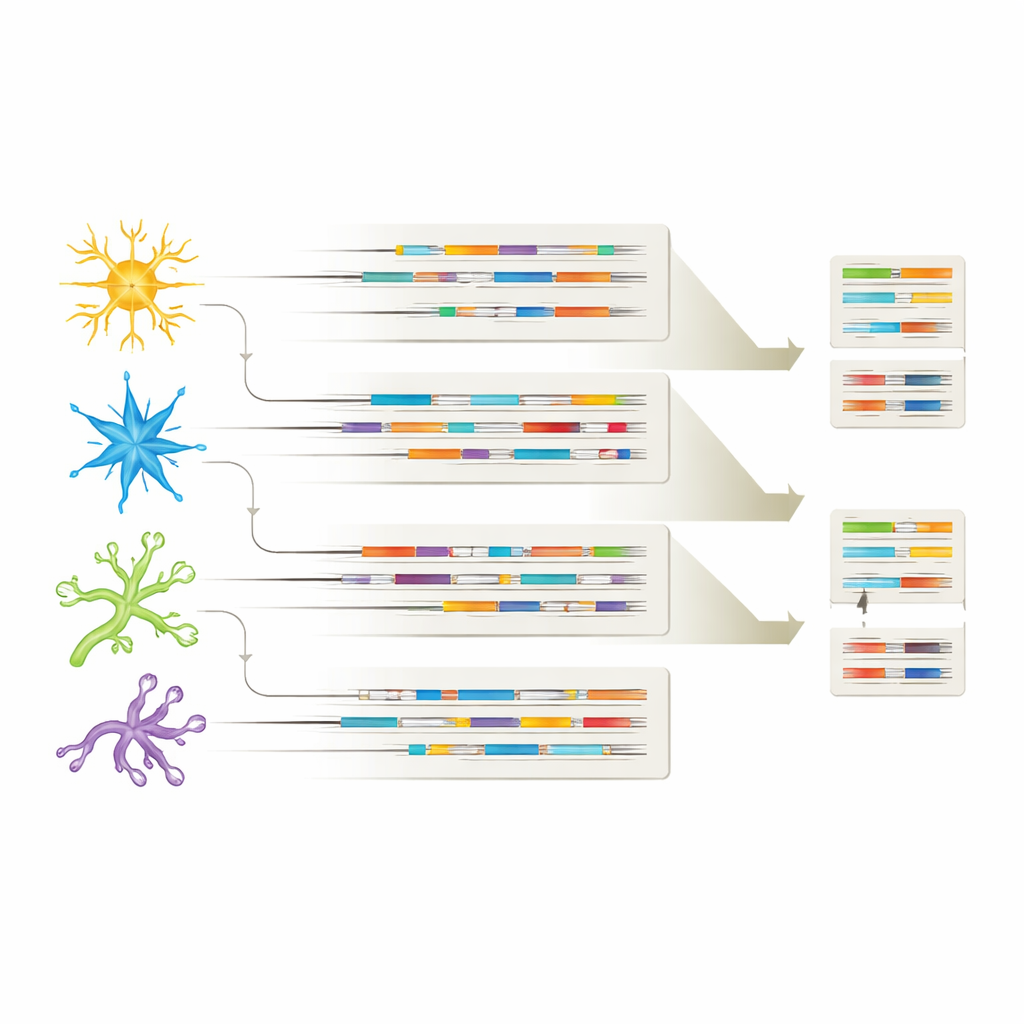
Olika celltyper, olika RNA-signaturer
Genom att koppla varje isoform till dess celltyp visade studien att varje större hjärncellspopulation bär sitt eget karakteristiska isoform-"fingeravtryck." Många RNA-varianter delades mellan neuroner och gliaceller, men varje celltyp uttryckte också unika isoformer, vilket antyder specialiserade roller i hälsa och sjukdom. I vissa fall förekom vissa isoformer endast i Alzheimerhjärnor eller endast i särskilda celltyper, såsom specifika APP-varianter i inhibitoriska neuroner eller en CHI3L1-isoform begränsad till astrocyter. Dessa mönster tyder på att det inte bara är vilka gener som är på eller av, utan vilka specifika RNA-versioner som används i varje celltyp, som kan forma hur Alzheimer utvecklas och vilka celler som blir mest sårbara.
Vad detta innebär för förståelse och behandling av Alzheimer
Detta arbete visar att Alzheimerhjärnan inte bara missbrukar gener, utan också remixar den finstilta strukturen i sina RNA-budskap på sätt som skiljer sig mellan celltyper. Långläsande enkelcellssekvensering exponerar sjukdomsassocierade isoformförändringar som skulle vara osynliga i konventionella gen-nivåstudier. Några av dessa nyupptäckta RNA-varianter, såsom förändrade isoformer av SEPTIN4 och CHI3L1, kan spela direkta roller i hjärnskada eller fungera som mer precisa biomarkörer för inflammation och degeneration. Medan mer forskning krävs för att testa deras funktioner och kliniska användbarhet, visar studien tydligt att framtida ansträngningar att förstå—och så småningom behandla—Alzheimer måste beakta inte bara gener, utan hela mångfalden av deras RNA-isoformer i enskilda hjärnceller.
Citering: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
Nyckelord: Alzheimers sjukdom, RNA-splitsning, single-cell-sekvensering, RNA-isoformer, neuroinflammation