Clear Sky Science · es
Diversidad de isoformas de ARN, variantes de empalme y conmutación en células individuales del cerebro con enfermedad de Alzheimer
Por qué importan las pequeñas diferencias en el ARN en el Alzheimer
La enfermedad de Alzheimer suele describirse en términos de placas, ovillos y pérdida de neuronas. Pero bajo esas imágenes microscópicas existe una capa aún más fina de complejidad: los mensajeros de ARN que indican a cada célula cerebral qué proteínas producir. Este estudio mira esa capa oculta a resolución de célula única, mostrando que no solo los genes, sino las «versiones» exactas del ARN de cada gen —llamadas isoformas— están ampliamente alteradas en los cerebros con Alzheimer. Comprender estos sutiles cambios en los mensajeros podría ayudar a explicar por qué ciertas células cerebrales fallan y podría descubrir nuevos biomarcadores o dianas terapéuticas.
Mirando dentro de células cerebrales individuales
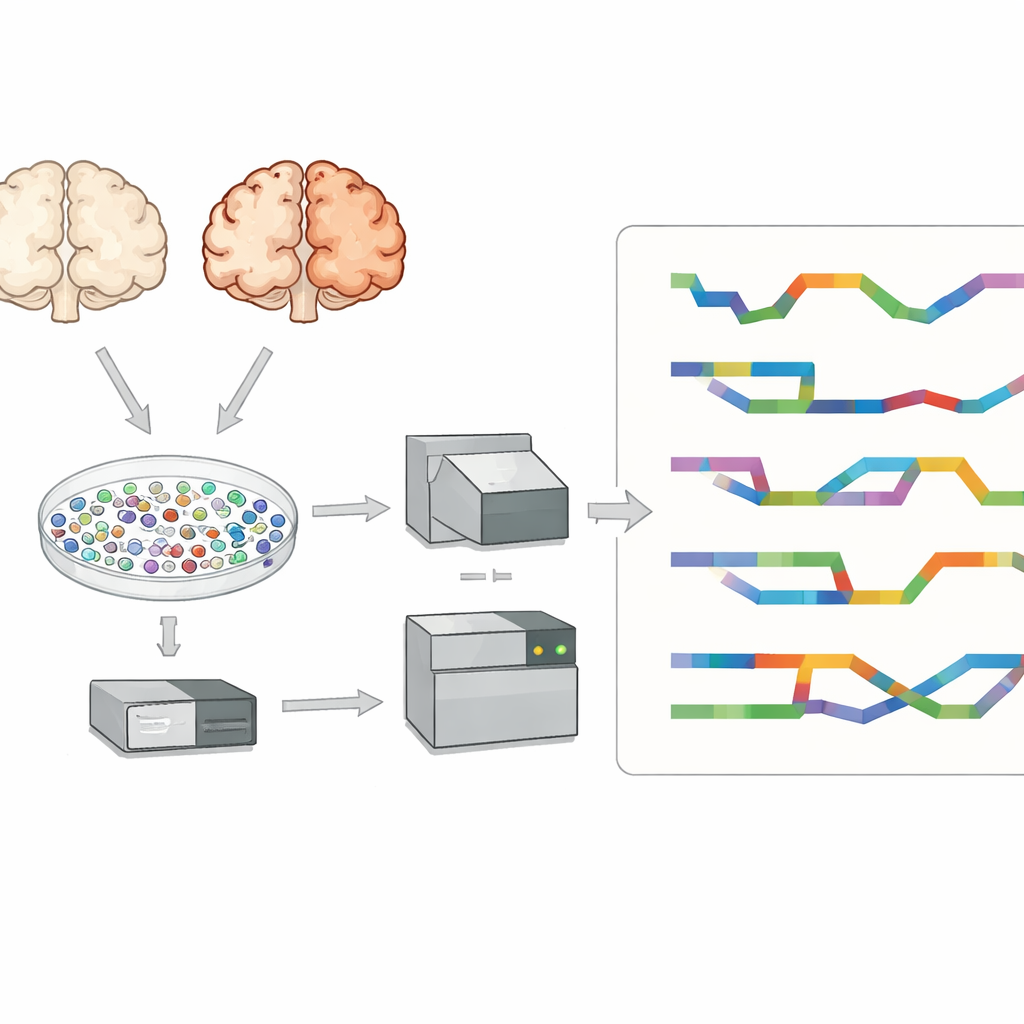
Los investigadores se centraron en la corteza prefrontal, una región cerebral importante para el pensamiento y la memoria que se ve fuertemente afectada en la enfermedad de Alzheimer. Examinaron tejido de ocho personas con Alzheimer y siete sin la enfermedad. En lugar de estudiar tejido mezclado, aislaron decenas de miles de núcleos celulares individuales y capturaron el ARN dentro de cada uno. Esto les permitió identificar los principales tipos celulares del cerebro —como neuronas excitadoras e inhibitorias, astrocitos, microglía, oligodendrocitos y sus precursores— y comparar cerebros con Alzheimer y no enfermos tipo celular por tipo celular, en lugar de tratar todo como una señal mezclada única.
Combinando dos tipos de potencia de secuenciación
La mayoría de los estudios de célula única usan secuenciación de lecturas cortas, que lee bien fragmentos pequeños de ARN pero tiene dificultades para reconstruir transcritos de longitud completa y sus patrones de empalme exactos. Para superar esto, el equipo usó una tecnología de lecturas largas llamada PacBio Kinnex junto con métodos estándar de lecturas cortas. Kinnex funciona vinculando muchas moléculas de ADN complementario extremo con extremo para que una única corrida de lecturas largas capture muchas copias completas de ARN. Tras la secuenciación, estas lecturas largas se fragmentaron digitalmente en moléculas individuales y luego se emparejaron con las etiquetas de cada célula originales. Este enfoque produjo alrededor de 70 000 núcleos individuales con identidad de tipo celular e información detallada de isoformas, proporcionando una visión inusualmente rica de la diversidad de ARN en el cerebro con Alzheimer.
Un vasto paisaje de variantes de ARN
A partir de estos datos, los científicos detectaron más de 850 000 isoformas de ARN y luego aplicaron filtros estrictos para definir unas 53 500 isoformas «confiables» que se observaron de forma robusta en varios cerebros. La mayoría pertenecía a tipos de transcritos conocidos, pero cerca de 4 000 eran claramente novedosas, revelando que incluso la corteza humana bien estudiada aún oculta variantes de ARN inesperadas. Muchos genes produjeron múltiples isoformas, con algunos —como el gen dystonin— mostrando docenas de versiones distintas. El equipo también observó isoformas raras con uniones internas inusuales, algunas potencialmente vinculadas a un proceso llamado recombinación somática de genes descrito previamente en Alzheimer, lo que subraya cuán diverso y dinámico puede ser el ARN cerebral.
Cambios ocultos que los genes por sí solos no muestran
Cuando los científicos compararon los cerebros con Alzheimer y los no enfermos a nivel génico usando datos de lecturas cortas, vieron patrones familiares: las vías inflamatorias estaban más activas en microglía y astrocitos, y genes relacionados con sinapsis y el procesamiento de amiloide estaban alterados en neuronas y oligodendrocitos. Pero el análisis de isoformas con lecturas largas reveló cambios que los promedios a nivel de gen pasaban completamente por alto. Algunos genes mostraban poca o ninguna diferencia global en la expresión, sin embargo isoformas específicas estaban fuertemente aumentadas o disminuidas o incluso «conmutadas» en su abundancia relativa en Alzheimer. Por ejemplo, el gen SEPTIN4, implicado en el andamiaje interno celular y hallado en agregados proteicos en enfermedades neurodegenerativas, tenía una isoforma reducida y otra aumentada, anulándose mutuamente a nivel génico. Otro gen, CHI3L1 —que codifica la proteína vinculada a la inflamación YKL-40— se reguló al alza en astrocitos principalmente a través de una única isoforma novedosa con segmentos retenidos, mientras que el transcrito conocido permaneció sin cambios. Desplazamientos similares a nivel de isoforma se observaron en genes relacionados con el Alzheimer como APOE, BIN1, APP y MAPT, a menudo de forma específica por tipo celular.
Diferentes tipos celulares, diferentes firmas de ARN
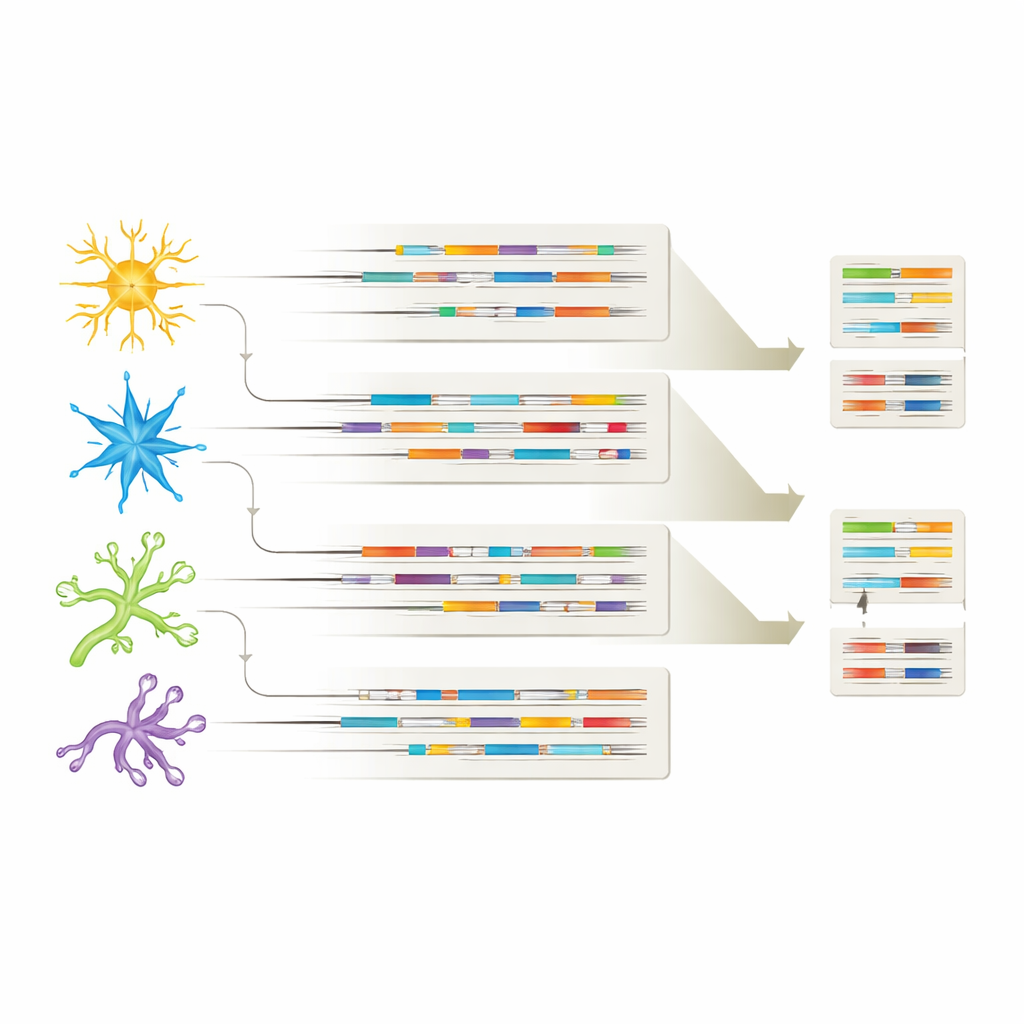
Al vincular cada isoforma con su tipo celular de origen, el estudio mostró que cada gran población celular cerebral tiene su propia «huella» de isoformas distintiva. Muchas variantes de ARN se compartieron entre neuronas y células gliales, pero cada tipo celular también expresó isoformas únicas, lo que sugiere roles especializados en salud y enfermedad. En algunos casos, ciertas isoformas aparecían solo en cerebros con Alzheimer o únicamente en tipos celulares particulares, como variantes específicas de APP en neuronas inhibitorias o una isoforma de CHI3L1 limitada a astrocitos. Estos patrones sugieren que no solo importa qué genes están activos o inactivos, sino qué versiones específicas de ARN se usan en cada tipo celular, lo que puede influir en cómo se desarrolla el Alzheimer y qué células son más vulnerables.
Qué significa esto para entender y tratar el Alzheimer
Este trabajo muestra que el cerebro con Alzheimer no solo está usando mal los genes, sino también remezclando la estructura fina de sus mensajes de ARN de formas que difieren según el tipo celular. La secuenciación de lecturas largas a nivel de célula única expone cambios en isoformas ligados a la enfermedad que serían invisibles en estudios convencionales a nivel génico. Algunas de estas variantes de ARN recién identificadas, como isoformas alteradas de SEPTIN4 y CHI3L1, podrían tener roles directos en el daño cerebral o servir como biomarcadores más precisos de inflamación y degeneración. Aunque se necesita más investigación para probar sus funciones y utilidad clínica, este estudio deja claro que los esfuerzos futuros para entender —y eventualmente tratar— el Alzheimer deberán considerar no solo los genes, sino la plena diversidad de sus isoformas de ARN en células cerebrales individuales.
Cita: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
Palabras clave: Enfermedad de Alzheimer, Empalme de ARN, secuenciación de célula única, isoformas de ARN, neuroinflamación