Clear Sky Science · pl
Różnorodność izoform RNA, warianty splicingu i przełączanie w pojedynczych komórkach mózgu w chorobie Alzheimera
Dlaczego drobne różnice w RNA mają znaczenie w chorobie Alzheimera
Choroba Alzheimera jest zwykle opisywana przez pryzmat płytki, splątków i obumierających komórek nerwowych. Jednak pod obrazami z mikroskopu kryje się jeszcze delikatniejsza warstwa złożoności: komunikaty RNA, które każdej komórce mózgu nakazują, jakie białka wytwarzać. Badanie to zagląda w tę ukrytą warstwę na poziomie pojedynczych komórek, wykazując, że nie tylko geny, lecz dokładne „wersje” RNA każdego genu — zwane izoformami — są w mózgach chorych na Alzheimera szeroko zmienione. Zrozumienie tych subtelnych zmian komunikatów może pomóc wyjaśnić, dlaczego niektóre komórki mózgu zawodzą, i ujawnić nowe biomarkery lub cele terapeutyczne.
Zaglądanie do poszczególnych komórek mózgu
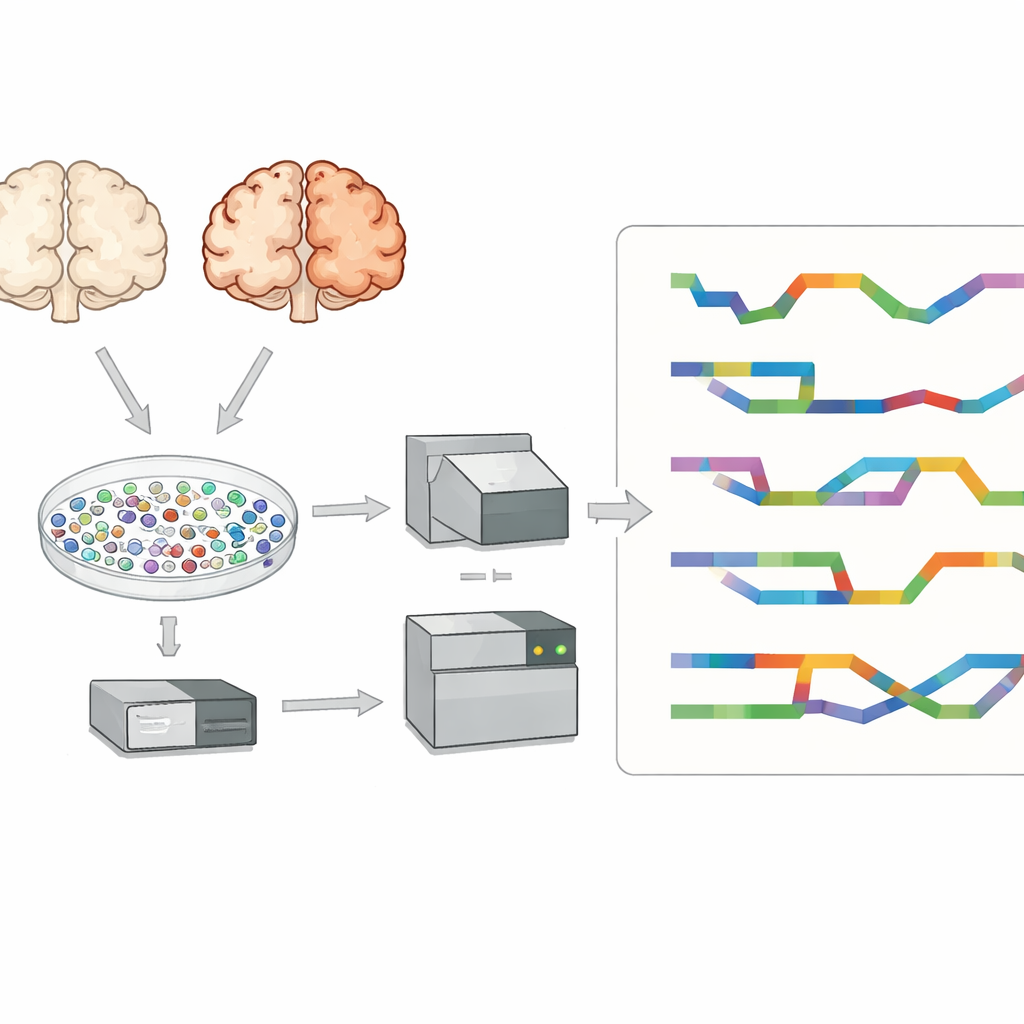
Naukowcy skupili się na korze przedczołowej, obszarze mózgu ważnym dla myślenia i pamięci, który jest silnie dotknięty w chorobie Alzheimera. Zbadali tkankę od ośmiu osób z chorobą Alzheimera i siedmiu bez niej. Zamiast analizować zlepkowaną tkankę, wyizolowali dziesiątki tysięcy pojedynczych jąder komórkowych i uchwycili RNA z każdego z nich. Pozwoliło to zidentyfikować główne typy komórek mózgowych — takie jak neurony pobudzające i hamujące, astrocyty, mikroglej, oligodendrocyty oraz ich prekursory — i porównać mózgi chorych i zdrowe typ komórki po typie, zamiast traktować próbki jako jednorodny sygnał.
Połączenie dwóch rodzajów mocy sekwencjonowania
Większość badań pojedynczych komórek korzysta z sekwencjonowania krótkich odczytów, które dobrze czyta małe fragmenty RNA, ale ma problem z odtworzeniem pełnych transkryptów i ich dokładnych wzorców splicingu. Aby temu sprostać, zespół użył technologii długich odczytów o nazwie PacBio Kinnex obok standardowych metod krótkich odczytów. Kinnex działa, łącząc wiele cząsteczek cDNA jeden za drugim, tak że pojedyncze uruchomienie długiego odczytu obejmuje wiele pełnych kopii RNA. Po sekwencjonowaniu te długie odczyty były cyfrowo dzielone z powrotem na pojedyncze cząsteczki, a następnie dopasowywane do oryginalnych kodów kreskowych komórek. To podejście dostarczyło danych z około 70 000 pojedynczych jąder z informacją o typie komórki i szczegółową informacją o izoformach, dając nietypowo bogaty obraz różnorodności RNA w mózgu chorych na Alzheimera.
Ogromny krajobraz wariantów RNA
Z tych danych naukowcy wykryli ponad 850 000 izoform RNA, po czym zastosowali rygorystyczne filtry, by zdefiniować około 53 500 „pewnych” izoform, które były solidnie obserwowane w wielu mózgach. Większość należała do znanych typów transkryptów, ale niemal 4 000 okazało się wyraźnie nowych, co ujawnia, że nawet dobrze zbadana kora ludzka wciąż kryje nieoczekiwane warianty RNA. Wiele genów produkowało wiele izoform, przy czym niektóre — takie jak gen dystoniny — wykazywały dziesiątki odrębnych wersji. Zespół zaobserwował także rzadkie izoformy z nietypowymi złączeniami wewnętrznymi, niektóre potencjalnie powiązane z procesem zwanym somatyczną rekombinacją genów opisanym wcześniej w kontekście Alzheimera, co podkreśla, jak różnorodne i dynamiczne może być RNA w mózgu.
Ukryte zmiany, których geny same nie pokażą
Gdy naukowcy porównali mózgi chorych na Alzheimera i zdrowe na poziomie genów, używając danych z krótkich odczytów, zobaczyli znane wzorce: szlaki zapalne były bardziej aktywne w mikrogleju i astrocytach, a geny związane z synapsami i przetwarzaniem amyloidu były zmienione w neuronach i oligodendrocytach. Jednak analiza izoform z długich odczytów ujawniła zmiany, których średnie na poziomie genów całkowicie nie wykrywały. Niektóre geny wykazywały niewielkie lub żadne ogólne różnice w ekspresji, a jednak konkretne izoformy były zdecydowanie zwiększone lub zmniejszone, a nawet „przełączone” w względnym udziale w chorobie Alzheimera. Na przykład gen SEPTIN4, zaangażowany w wewnętrzny ruszt komórkowy i znaleziony w agregatach białkowych w chorobach neurodegeneracyjnych, miał jedną izoformę zredukowaną i inną zwiększoną, co nawzajem się znosiło na poziomie genu. Inny gen, CHI3L1 — kodujący białko powiązane z zapaleniem YKL-40 — był w astrocytach podwyższony głównie poprzez jedną nową izoformę z zachowanymi segmentami, podczas gdy znany transkrypt pozostawał niezmieniony. Podobne przesunięcia na poziomie izoform obserwowano dla genów związanych z AD, takich jak APOE, BIN1, APP i MAPT, często w sposób specyficzny dla typu komórki.
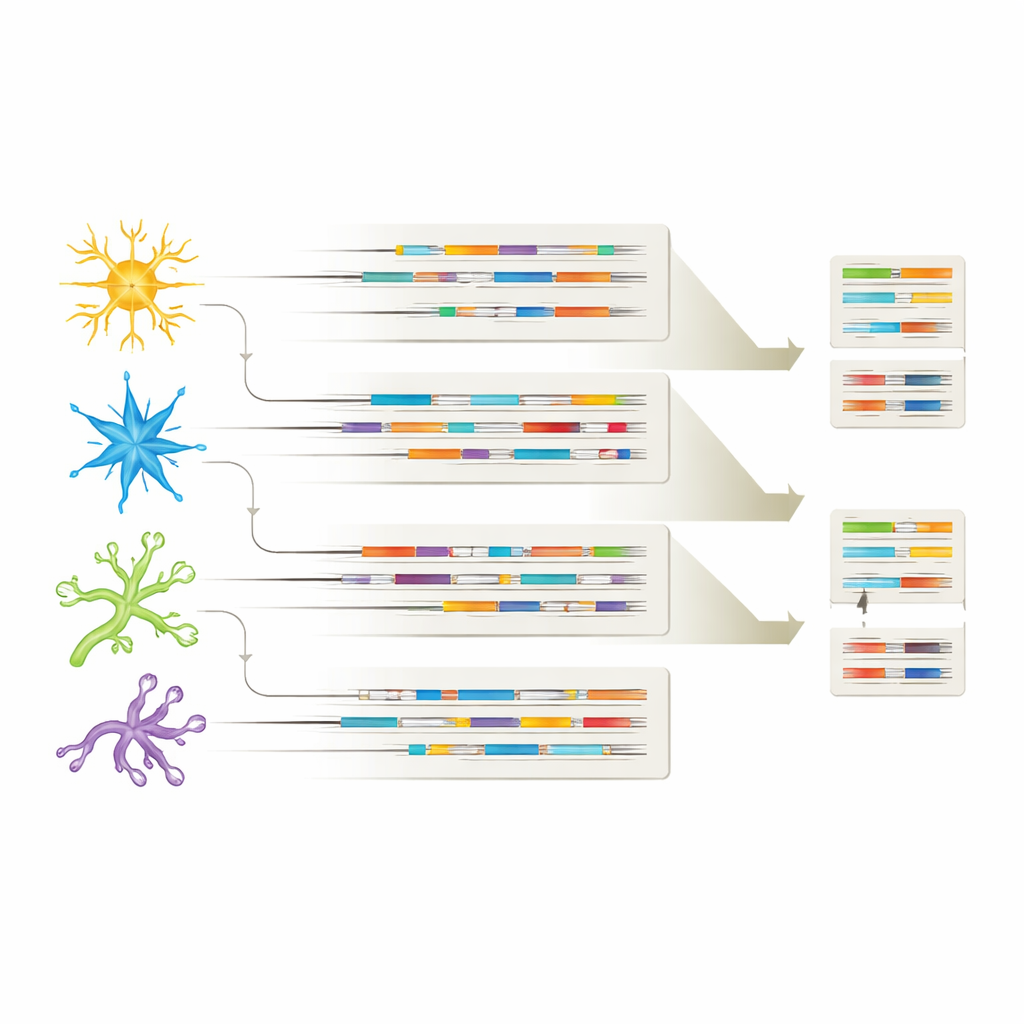
Różne typy komórek, różne sygnatury RNA
Łącząc każdą izoformę z typem komórki, z której pochodziła, badanie pokazało, że każda główna populacja komórek mózgowych niesie własny wyróżniający się „odcisk palca” izoform. Wiele wariantów RNA było współdzielonych między neuronami i komórkami glejowymi, ale każdy typ komórki wyrażał też unikalne izoformy, sugerując wyspecjalizowane role w zdrowiu i chorobie. W niektórych przypadkach pewne izoformy pojawiały się tylko w mózgach chorych na Alzheimera lub tylko w określonych typach komórek, na przykład specyficzne warianty APP w neuronach hamujących albo izoforma CHI3L1 ograniczona do astrocytów. Te wzorce sugerują, że nie tylko to, które geny są włączone lub wyłączone, ale które konkretne wersje RNA są wykorzystywane w każdym typie komórki, może kształtować rozwój Alzheimera i podatność poszczególnych komórek.
Co to oznacza dla zrozumienia i leczenia Alzheimera
Ta praca pokazuje, że mózg chorego na Alzheimera nie tylko niewłaściwie używa genów, lecz także remiksuje drobną strukturę swoich komunikatów RNA w sposób różny w poszczególnych typach komórek. Sekwencjonowanie pojedynczych komórek z długimi odczytami ujawnia związane z chorobą zmiany izoform, które byłyby niewidoczne w konwencjonalnych badaniach na poziomie genów. Niektóre z tych nowo zidentyfikowanych wariantów RNA, takie jak zmienione izoformy SEPTIN4 i CHI3L1, mogą odgrywać bezpośrednią rolę w uszkodzeniu mózgu lub służyć jako bardziej precyzyjne biomarkery zapalenia i degeneracji. Choć potrzebne są dalsze badania, aby przetestować ich funkcje i przydatność kliniczną, badanie to wyraźnie pokazuje, że przyszłe wysiłki mające na celu zrozumienie — i ostatecznie leczenie — choroby Alzheimera będą musiały uwzględniać nie tylko geny, lecz pełną różnorodność ich izoform RNA w pojedynczych komórkach mózgu.
Cytowanie: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
Słowa kluczowe: choroba Alzheimera, splicing RNA, sekwencjonowanie pojedynczych komórek, izoformy RNA, neurozapalenie