Clear Sky Science · de
Vielfalt von RNA-Isoformen, Spleißvarianten und Umschaltungen in Einzelzellen des Alzheimer-Gehirns
Warum winzige RNA-Unterschiede bei Alzheimer wichtig sind
Alzheimer wird meist durch Plaques, Tangles und sterbende Nervenzellen beschrieben. Unter diesen Mikroskopbildern liegt jedoch eine noch feinere Ebene der Komplexität: die RNA-Botschaften, die jeder Gehirnzelle vorschreiben, welche Proteine sie herstellen soll. Diese Studie blickt in dieser verborgenen Ebene auf Einzelzell-Auflösung und zeigt, dass nicht nur Gene, sondern die exakten „Versionen“ der RNA eines jeden Gens – sogenannte Isoformen – im Alzheimer-Gehirn umfangreich verändert sind. Das Verständnis dieser subtilen Nachrichtenänderungen könnte helfen zu erklären, warum bestimmte Zellen versagen, und neue Biomarker oder Arzneimittelziele offenbaren.
Blick in einzelne Gehirnzellen
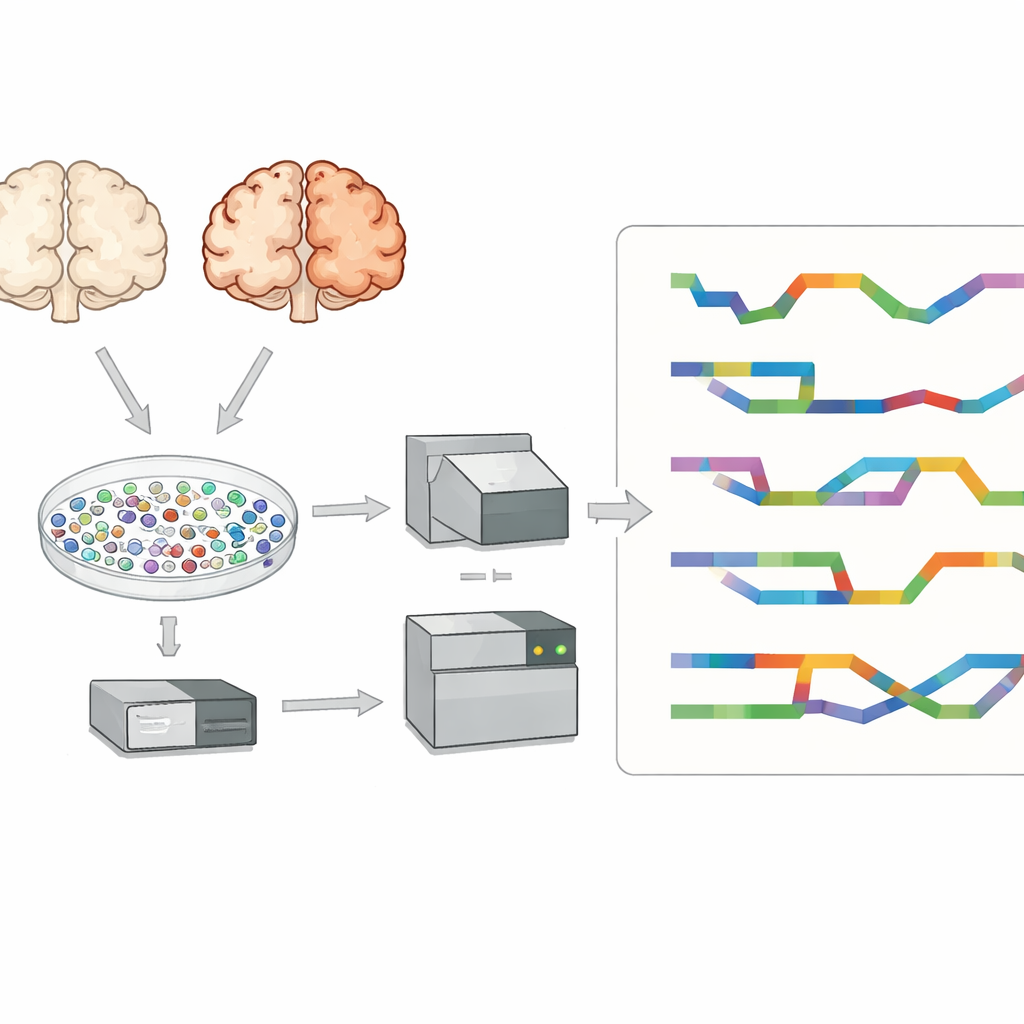
Die Forschenden konzentrierten sich auf den präfrontalen Kortex, eine für Denken und Gedächtnis wichtige Hirnregion, die bei Alzheimer stark betroffen ist. Sie untersuchten Gewebe von acht Personen mit Alzheimer und sieben Kontrollen. Statt gemischtes Gewebe zu analysieren isolierten sie Zehntausende einzelner Zellkerne und erfassten die RNA in jedem einzelnen. So konnten sie die großen Hirnzelltypen identifizieren – etwa exzitatorische und inhibitorische Neurone, Astrozyten, Mikroglia, Oligodendrozyten und deren Vorläufer – und Alzheimer- und gesunde Gehirne zelltypspezifisch vergleichen, statt als einen einzigen gemischten Signal.
Zwei Arten von Sequenzier-Power kombiniert
Die meisten Einzelzellstudien nutzen Kurzlese-Sequenzierung, die kurze RNA-Schnipsel zuverlässig liest, aber Probleme hat, vollständige Transkripte und deren exakte Spleißmuster zu rekonstruieren. Um das zu überwinden, nutzte das Team eine Langlesen-Technologie namens PacBio Kinnex neben üblichen Kurzlese-Methoden. Kinnex verknüpft viele cDNA-Moleküle Ende an Ende, so dass ein einzelner Langlese-Durchlauf viele vollständige RNA-Kopien erfasst. Nach der Sequenzierung wurden diese langen Reads digital in einzelne Moleküle zurückgeschnitten und dann den ursprünglichen Zell-Barcodes zugeordnet. Dieser Ansatz lieferte rund 70.000 einzelne Kerne mit sowohl Zelltyp-Identität als auch detaillierten Isoform-Daten und bot damit einen ungewöhnlich reichen Einblick in die RNA-Vielfalt im Alzheimer-Gehirn.
Eine weite Landschaft von RNA-Varianten
Aus diesen Daten detektierten die Forschenden mehr als 850.000 RNA-Isoformen und wandten strenge Filter an, um etwa 53.500 „vertrauenswürdige“ Isoformen zu definieren, die über mehrere Gehirne robust nachgewiesen wurden. Die meisten gehörten zu bekannten Transkripttypen, doch nahezu 4.000 waren klar neu und zeigten, dass selbst der gut untersuchte menschliche Kortex unerwartete RNA-Varianten verbirgt. Viele Gene erzeugten mehrere Isoformen; einige – etwa das Dystonin-Gen – wiesen Dutzende unterschiedlicher Versionen auf. Das Team beobachtete auch seltene Isoformen mit ungewöhnlichen internen Junctions, manche möglicherweise verknüpft mit einem Prozess namens somatische Genrekombination, der zuvor bei Alzheimer beschrieben wurde, und unterstrich damit, wie vielfältig und dynamisch Gehirn-RNA sein kann.
Verborgene Veränderungen, die Gene allein nicht zeigen
Beim Vergleich von Alzheimer- und Kontrollgehirnen auf Genebene mit Kurzlese-Daten zeigten sich vertraute Muster: Entzündungswege waren in Mikroglia und Astrozyten stärker aktiv, und Gene, die mit Synapsen und Amyloid-Verarbeitung zu tun haben, waren in Neuronen und Oligodendrozyten verändert. Die Langlesen-Isoform-Analyse enthüllte aber Veränderungen, die durch Genmittelwerte vollständig übersehen würden. Einige Gene zeigten wenig oder keinen Gesamtunterschied in der Expression, doch bestimmte Isoformen waren stark erhöht, vermindert oder sogar in ihrer relativen Häufigkeit „umgeschaltet“ im Alzheimer-Gehirn. So war beispielsweise das Gen SEPTIN4, das am zellulären Gerüst beteiligt ist und in Proteinaggregaten neurodegenerativer Erkrankungen gefunden wurde, mit einer Isoform verringert und einer anderen erhöht, so dass sich diese Effekte auf Genebene gegenseitig aufhoben. Ein anderes Gen, CHI3L1 – das das entzündungsassoziierte Protein YKL-40 kodiert – war in Astrozyten hauptsächlich durch eine einzelne neuartige Isoform mit retained Segments hochreguliert, während das bekannte Transkript unverändert blieb. Ähnliche Isoform-Verschiebungen zeigten AD-assoziierte Gene wie APOE, BIN1, APP und MAPT, oft zelltypspezifisch.
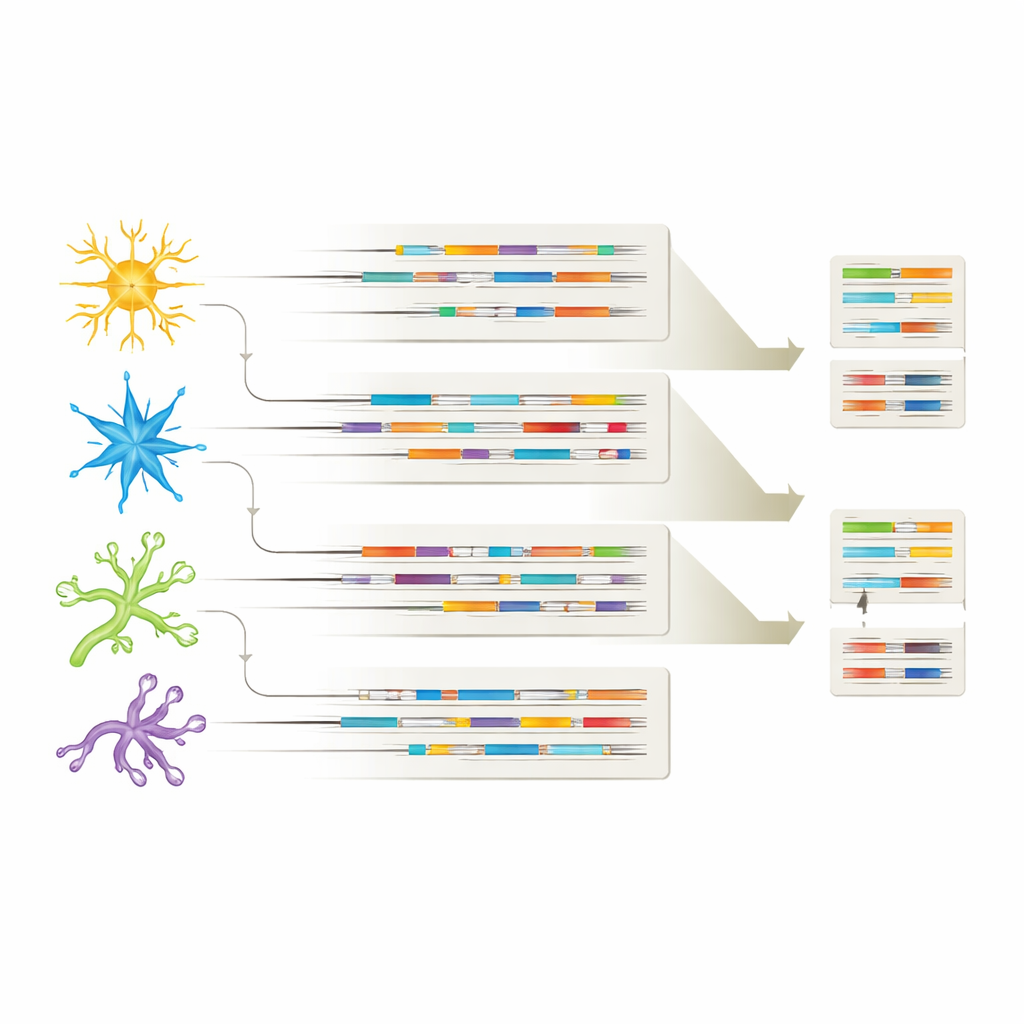
Unterschiedliche Zelltypen, unterschiedliche RNA-Signaturen
Indem jede Isoform mit ihrem Zelltyp verknüpft wurde, zeigte die Studie, dass jede größere Hirnzellpopulation ihren eigenen charakteristischen Isoform-„Fingerabdruck“ trägt. Viele RNA-Varianten wurden zwischen Neuronen und Gliazellen geteilt, aber jeder Zelltyp exprimierte auch einzigartige Isoformen, was auf spezialisierte Rollen in Gesundheit und Krankheit hinweist. In einigen Fällen traten bestimmte Isoformen nur in Alzheimer-Gehirnen oder ausschließlich in bestimmten Zelltypen auf, etwa bestimmte APP-Varianten in inhibitorischen Neuronen oder eine CHI3L1-Isoform, die auf Astrozyten beschränkt war. Diese Muster deuten darauf hin, dass nicht nur welche Gene an- oder ausgeschaltet sind, sondern welche spezifischen RNA-Versionen in jedem Zelltyp genutzt werden, die Entwicklung von Alzheimer und die Anfälligkeit einzelner Zellen mitbestimmen können.
Was das für Verständnis und Behandlung von Alzheimer bedeutet
Diese Arbeit zeigt, dass das Alzheimer-Gehirn nicht nur Gene fehlverwendet, sondern auch die feine Struktur seiner RNA-Botschaften in zelltypspezifischer Weise neu mischt. Langlesen-Einzelzellsequenzierung legt krankheitsassoziierte Isoformveränderungen offen, die in konventionellen Genebene-Studien unsichtbar blieben. Einige der neu identifizierten RNA-Varianten, etwa veränderte Isoformen von SEPTIN4 und CHI3L1, könnten direkt an Hirnschäden beteiligt sein oder als präzisere Biomarker für Entzündung und Degeneration dienen. Zwar sind weitere Studien nötig, um ihre Funktionen und klinische Nützlichkeit zu prüfen, doch macht die Arbeit deutlich, dass künftige Bemühungen, Alzheimer zu verstehen – und schließlich zu behandeln – nicht nur Gene, sondern die volle Vielfalt ihrer RNA-Isoformen in einzelnen Gehirnzellen berücksichtigen müssen.
Zitation: Shahnaee, A., Liu, C.S., Ngo, T. et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol 9, 506 (2026). https://doi.org/10.1038/s42003-026-09759-9
Schlüsselwörter: Alzheimer-Krankheit, RNA-Spleißen, Einzelzellsequenzierung, RNA-Isoformen, Neuroinflammation