Clear Sky Science · tr
Ependimomaya özgü kan-beyin bariyeri farklılıkları çoklu omik yaklaşımla ortaya kondu
Çocuklardaki Kanser İçin Beynin Kapıcılarının Önemi
İnsan beyni, kan–beyin bariyeri adı verilen doğal bir güvenlik sistemiyle sıkı şekilde korunur; bu, kan dolaşımından beyin dokusuna hangi maddelerin girebileceğini katı biçimde kontrol eden sıkı bir hücre tabakasıdır. Bu bariyer sağlık için hayati önem taşır, ancak aynı zamanda kanser ilaçlarının, özellikle çocuklardaki beyin tümörlerine ulaşmasını çok daha zorlaştırır. Bu çalışma, büyük klinik sonuçları olan aldatıcı derecede basit bir soruyu soruyor: ependimom adı verilen pediatrik bir beyin tümörünün farklı alt tipleri farklı tür bariyerlerin arkasında mı yaşıyor ve bu durum birçok ilacın neden başarısız olduğunu açıklamaya yardımcı olabilir mi?
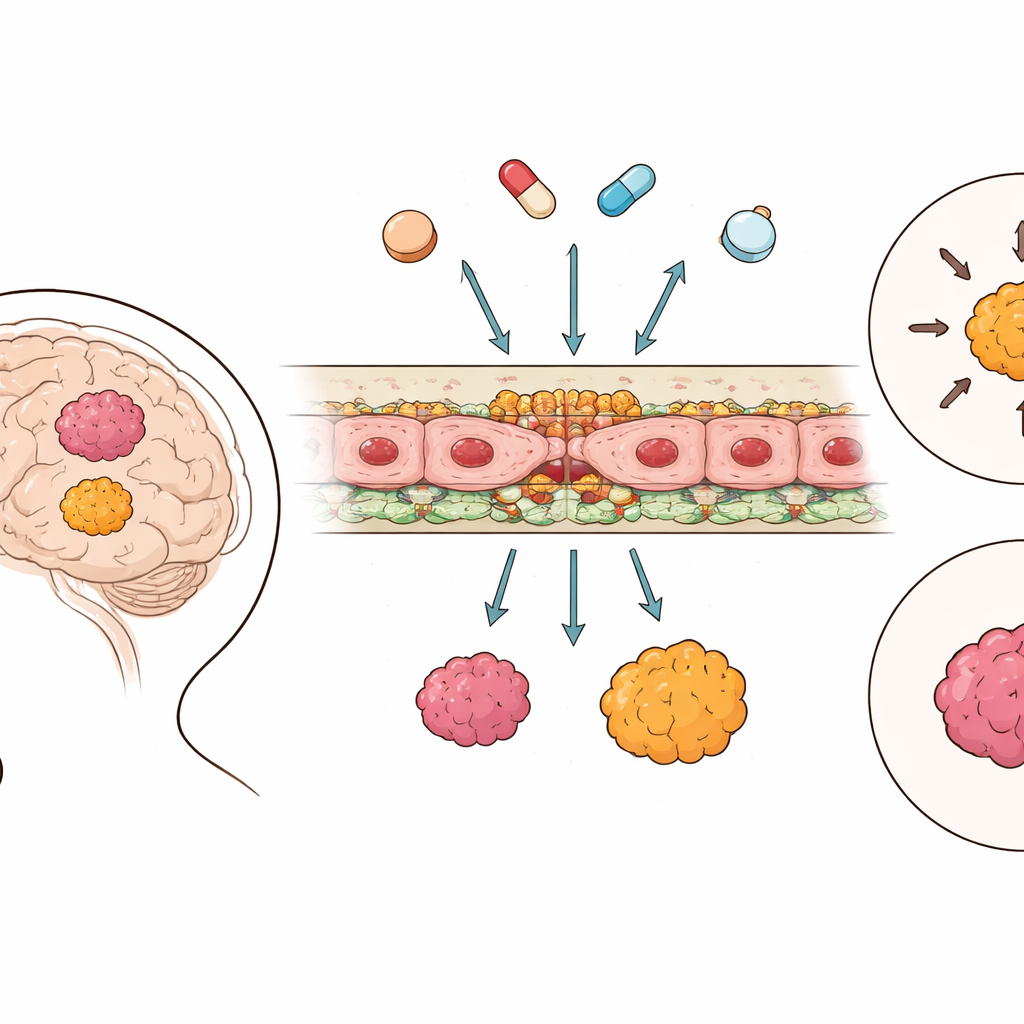
Beyninin Koruyucu Duvarı
Kan–beyin bariyeri, özel bağlantılarla birbirine kilitlenmiş küçük beyin damarlarını döşeyen hücrelerden oluşur ve ilaçları tekrar kan dolaşımına atan moleküler “pompalara” sahiptir. Araştırmacılar, 364 ependimom tümöründen ve 225 sağlıklı beyin örneğinden gelen büyük ölçekli genetik verileri kullanarak bu bağlantılarda ve taşıma sistemlerinde rol oynayan genlerin etkinliğini katalogladılar. Birçok diğer beyin kanserinin aksine ependimom dokusunun, sağlıklı beyne göre ana bağlantı bileşenlerinin daha yüksek aktivitesini gösterdiğini buldular; bu, kan ile tümör arasındaki bariyerin genellikle daha sızdıran değil, aksine daha sıkı olduğunu düşündürüyor. Buna karşılık, ilaç dışa atım pompaları ve diğer taşıyıcılar basit bir açık-kapalı eğiliminden ziyade daha karışık, grup-özgü desenler izledi.
Sadece Konum ya da Yaş Değil, Tümör Tipi
Sonra ekip, beyin gelişimi veya anatomisindeki normal farklılıkların bu desenleri açıklayıp açıklamayacağını sorguladı. Bağlantı ve taşıyıcı gen etkinliklerini özetleyen sinir ağı puanları eğiterek, sağlıklı beyinlerde bilinen özellikleri doğruladılar: bariyer sıkılığı yaşla değişir ve korteks ile beyincik gibi bölgeler arasında farklılık gösterir. Ancak bu yaş ve bölgesel eğilimler tümörlere taşınmadı. Büyük intrakraniyal ependimom grupları arasında bariyerle ilişkili puanlar, tümörün beyinde nerede ortaya çıktığına veya hastanın yaşına bakılmaksızın benzer görünüyordu. Bu da yerel bariyerin nasıl davrandığını belirleyen ana sürücünün tümörün moleküler kimliği—yani alt grubu—olduğunu işaret ediyor.
Bariyer Hücrelerine Yakın Plan
Toplu ölçümler hangi hücrelerin gözlemlenen gen etkinliğinden gerçekten sorumlu olduğunu gizleyebilir. Bunu çözmek için araştırmacılar, birden fazla hasta kohortundan ve yeni bir doğrulama setinden tek hücreli ve tek çekirdekli RNA dizilemeye yöneldiler. Bu daha ayrıntılı veriler, bariyerle ilişkili genlerin çoğunun tümör mikroçevresindeki damar hücrelerinin belirgin bir alt kümesinde yoğunlaştığını ortaya koydu. Bu uzmanlaşmış endotelyal altpopülasyon, CLDN5 gibi klasik bağlantı genleri ve diğer bariyer belirteçlerinin güçlü ifadesini gösterirken tümör hücreleri, immün hücreler ve destek hücreleri çok az ifade gösteriyordu. Bulgular, bu proteinlerin tümör kan damarlarını fiziksel olarak döşediğini gösteren protein ölçümleri ve gelişmiş görüntülemelerle desteklendi; böylece genetik imzaların gerçek bir yapısal bariyeri yansıttığı doğrulandı.
Fare Modellerinde Bariyerin Test Edilmesi
Yeni ilaçlar hastalara ulaşmadan önce genellikle fare modellerinde değerlendirilir; ekip, farklı ependimom gruplarına ait hasta kökenli ksenogreftlerin insan bariyer özelliklerini yeniden üretip üretmediğini inceledi. Bu modellerde, hastadan alınan tümör hücreleri farelerin beyinlerinde büyür ve damarlar büyük ölçüde fare kaynaklıdır. RNA ve protein analizleri yine damar hücrelerinde güçlü bağlantı ifadesi gösterdi, ancak modeller arasında ve tümör ile çevreleyen beyin arasında bazı farklılıklar vardı. Kontrast ajanları ve floresan izleyicilerle yapılan görüntüleme genel olarak bu tümörlerde bariyerin nispeten sağlam kaldığını; ayrıca modeller ve alt gruplar arasındaki ince farklılıkların moleküllerin kanaktan tümör dokusuna ne kadar kolay geçebileceğini etkileyebileceğini öne sürdü.
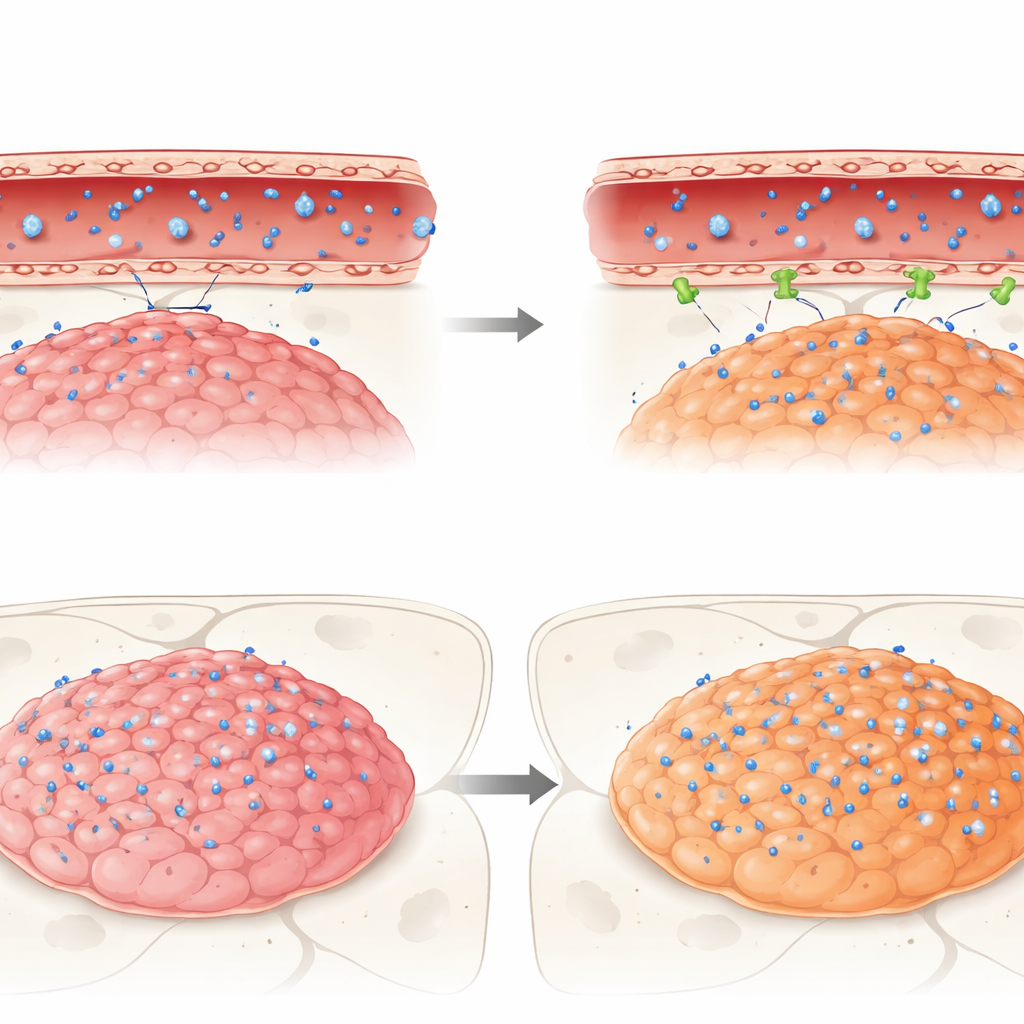
Gerçek İlaçlar Geçmeye Çalıştığında Ne Oluyor
Son olarak araştırmacılar, klinik olarak ilgili üç anti-kanser ilaç—idasanutlin, temsirolimus ve etoposid—in bu fare tümörlerine yolculuğunu izlediler. Üçü de kültürde ependimom hücrelerine karşı etkindı, ama canlı beyinlerde bariyerle karşılaştılar. Hücre zarlarını geçmeye kimyasal olarak elverişli olan idasanutlin, kana kıyasla hem tümörde hem de normal beyinde çok düşük düzeylere ulaştı; bu da bariyer tarafından güçlü bir dışlama olduğunu işaret ediyor. Buna karşılık, belirli pompalar tarafından atıldığı bilinen temsirolimus ve etoposid, bir agresif alt grup (ZFTA füzyon-pozitif) tümörlerinde diğer bir grup (PFA) veya komşu sağlıklı beyne göre daha fazla birikim gösterdi. Yine de hiçbir ilaç tümörlerde in vitro etkin seviyeleriyle eşleşen konsantrasyonlara ulaşamadı; bu da bariyerin umut vaat eden tedavileri sessizce zayıflatabildiğini vurguluyor.
Gelecekteki Tedaviler İçin Anlamı
Halk için ana mesaj basit: ependimom tümörleri aynı tür beyin kapısının arkasında oturmuyor. Bunun yerine her moleküler alt grup, farklı bir kan–beyin bariyeri versiyonuyla geliyor—çoğunlukla şaşırtıcı derecede sıkı—ve bu da farklı ilaçların hedeflerine ne kadar iyi ulaşacağını şekillendiriyor. Hastalardan ve fare modellerinden birden fazla veri katmanını birleştiren bu çalışma, alt gruba özgü bariyer özelliklerini anlamanın ve ölçmenin daha akıllı klinik denemeler tasarlamak için gerekli olduğunu gösteriyor. Bir ilacın kültürde tümör hücrelerini öldürdüğü varsayımına dayanmak yerine, gelecekteki tedaviler her tümörün kapıcılarının nasıl inşa edildiğine göre seçilmeli—ve gerekirse bariyeri değiştiren stratejilerle eşleştirilmeli.
Atıf: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
Anahtar kelimeler: ependimom, kan-beyin bariyeri, pediatrik beyin tümörleri, ilaç dağılımı, çoklu omik