Clear Sky Science · de
Gruppenspezifische Unterschiede der Blut-Hirn-Schranke bei Ependymomen durch einen Multi-Omics-Ansatz aufgedeckt
Warum die Wächter des Gehirns für krebskranke Kinder wichtig sind
Das menschliche Gehirn wird von einem natürlichen Schutzsystem streng bewacht: der Blut‑Hirn‑Schranke, einer dichten Zellschicht, die genau steuert, welche Substanzen aus dem Blut ins Hirngewebe gelangen dürfen. Diese Barriere ist für die Gesundheit unverzichtbar, erschwert aber zugleich die Verabreichung von Krebsmedikamenten in Hirntumoren – besonders bei Kindern. Die Studie stellt eine auf den ersten Blick einfache Frage mit großen klinischen Folgen: Leben verschiedene Subtypen eines pädiatrischen Hirntumors, des Ependymoms, hinter unterschiedlichen Arten von Barrieren, und könnte das erklären, warum viele Wirkstoffe versagen?
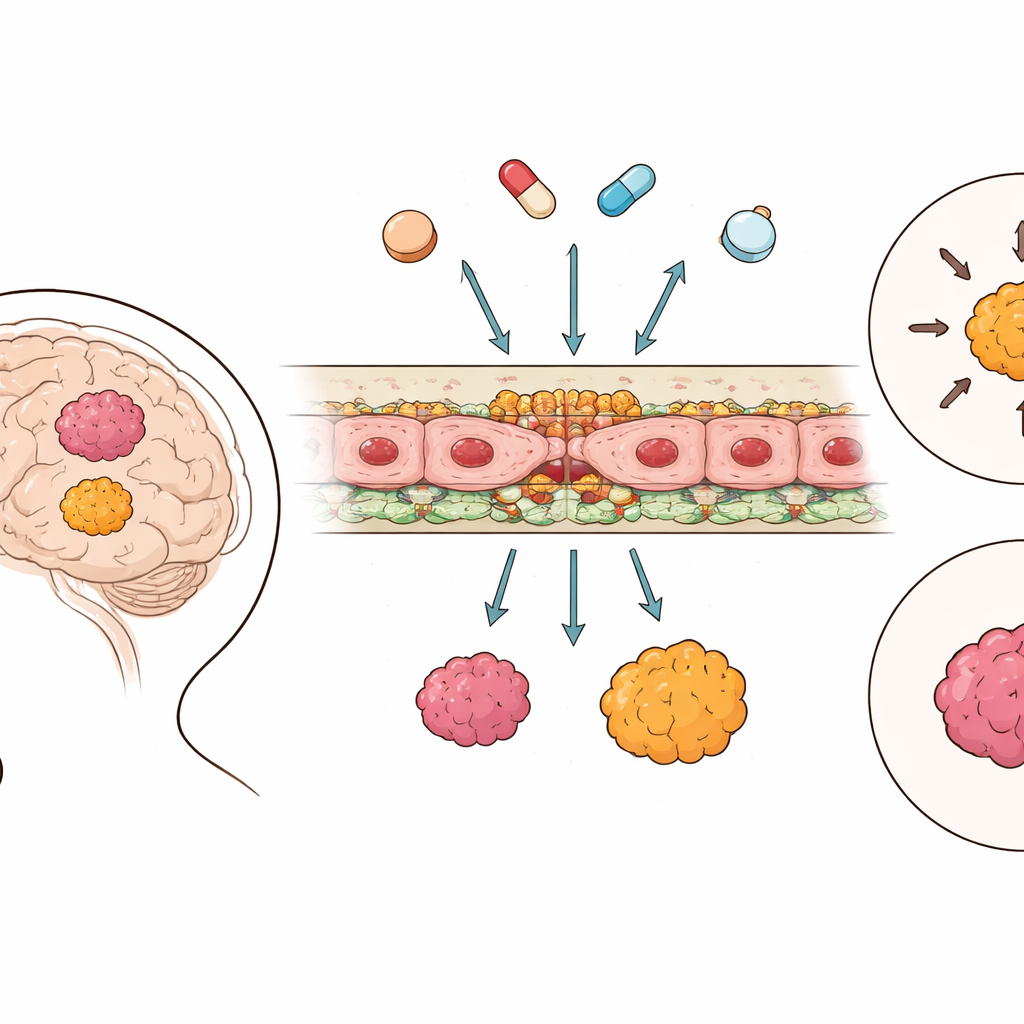
Die schützende Wand des Gehirns
Die Blut‑Hirn‑Schranke besteht aus Zellen, die winzige Hirngefäße auskleiden und durch spezialisierte Verbindungen eng miteinander verknüpft sind; dazu kommen molekulare „Pumpen“, die Wirkstoffe zurück ins Blut befördern können. Anhand großangelegter genetischer Daten von 364 Ependymom‑Tumoren und 225 Proben gesunden Gewebes erfassten die Forschenden die Aktivität von Genen, die an diesen Verbindungen und Transportsystemen beteiligt sind. Anders als bei vielen anderen Hirnkrebsarten zeigte das Ependymomgewebe eine höhere Aktivität zentraler Verbindungs‑Komponenten als das gesunde Gehirn, was darauf hindeutet, dass die Barriere zwischen Blut und Tumor häufig enger statt durchlässiger ist. Im Gegensatz dazu zeigten Wirkstoff‑Effluxpumpen und andere Transporter gemischtere, gruppenspezifische Muster statt eines einfachen An‑oder‑Aus‑Trends.
Nicht nur Lage oder Alter, sondern Tumortyp
Als Nächstes prüfte das Team, ob normale Unterschiede in Entwicklung oder Anatomie des Gehirns diese Muster erklären könnten. Mit künstlichen neuronalen Netzen erzeugten sie Scores, die die Aktivität von Verbindungs‑ und Transportergen zusammenfassen, und bestätigten bekannte Merkmale gesunden Gewebes: Die Dichtigkeit der Barriere verändert sich mit dem Alter und unterscheidet sich zwischen Regionen wie Cortex und Kleinhirn. Diese Alters‑ und Regionaltrends zeigten sich jedoch nicht in den Tumoren. Zwischen den wichtigsten intrakraniellen Ependymomgruppen waren die barrierebezogenen Scores unabhängig davon ähnlich, wo im Gehirn der Tumor entstand oder wie alt der Patient war. Das deutet darauf hin, dass die molekulare Identität des Tumors – seine Subgruppe – der Haupttreiber dafür ist, wie die lokale Barriere funktioniert.
Ein Blick auf die Barriereszellen
Grob gemessene Daten können verschleiern, welche Zellen tatsächlich für die beobachtete Genaktivität verantwortlich sind. Um das aufzulösen, nutzten die Forschenden Einzelzell‑ und Einzelkern‑RNA‑Sequenzierungen aus mehreren Patientenkohorten und einer neuen Validierungsgruppe. Diese feineren Daten zeigten, dass die meisten barrierebezogenen Gene in einer klar abgegrenzten Untergruppe von Gefäßzellen im Tumormikromilieu konzentriert sind. Diese spezialisierte endotheliale Subpopulation zeigte starke Expression klassischer Verbindungs‑Gene wie CLDN5 und anderer Barrieremarker, während Tumorzellen, Immunzellen und Stütz‑Zellen nur sehr wenig exprimierten. Die Ergebnisse wurden durch Proteinmessungen und fortgeschrittene Bildgebung gestützt, die zeigten, dass diese Proteine physisch die Tumorblutgefäße auskleiden – ein Beleg dafür, dass die genetischen Signaturen eine echte strukturelle Barriere widerspiegeln.
Testen der Barriere in Mausmodellen
Da neue Medikamente häufig zunächst in Mausmodellen geprüft werden, untersuchten die Forschenden, ob patientenabgeleitete Xenotransplantate verschiedener Ependymomgruppen die Barriere‑Eigenschaften des Menschen nachbilden. In diesen Modellen wachsen Tumorzellen von Patienten im Gehirn von Mäusen, wobei die Blutgefäße überwiegend mauslichen Ursprungs sind. Analysen von RNA und Protein zeigten erneut eine starke Verbindungs‑Expression in Gefäßzellen, allerdings mit Unterschieden zwischen Modellen und zwischen Tumor und umgebendem Gehirn. Bildgebung mit Kontrastmitteln und fluoreszenten Tracern deutete insgesamt darauf hin, dass die Barriere in diesen Tumoren relativ intakt blieb und subtile Unterschiede zwischen Modellen und Subgruppen beeinflussen können, wie leicht Moleküle vom Blut ins Tumorgewebe gelangen.
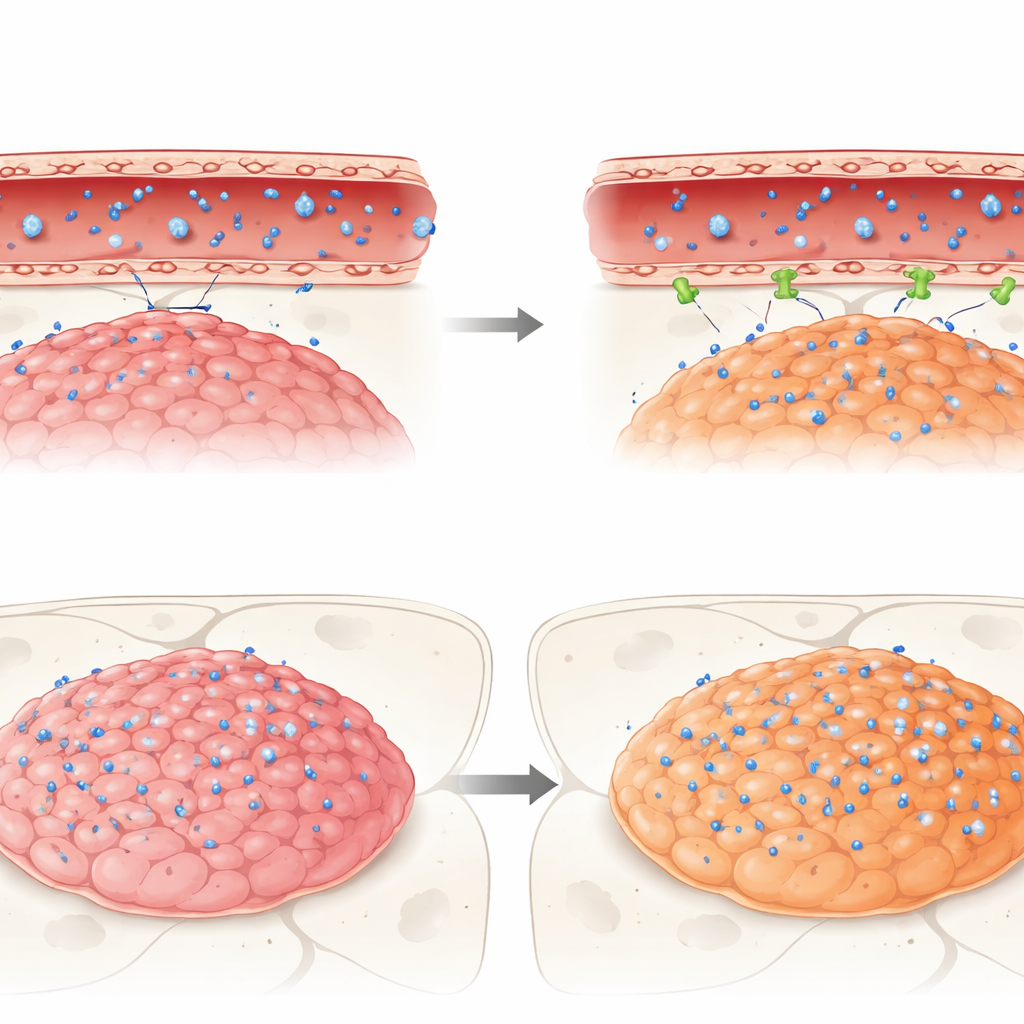
Was passiert, wenn echte Medikamente versuchen zu passieren
Schließlich verfolgten die Forschenden drei klinisch relevante Krebsmedikamente – Idasanutlin, Temsirolimus und Etoposid – in diese Maus‑Tumoren. Alle drei waren in Zellkulturen gegen Ependymomzellen wirksam, stießen aber im lebenden Gehirn auf die Barriere. Idasanutlin, obwohl chemisch geeignet, Zellmembranen zu passieren, erreichte sowohl im Tumor als auch im normalen Gehirn sehr niedrige Konzentrationen im Vergleich zum Blut, was auf eine starke Ausschlusswirkung der Barriere hindeutet. Im Gegensatz dazu akkumulierten Temsirolimus und Etoposid – beides Substrate bestimmter Effluxpumpen – stärker in Tumoren einer aggressiven Subgruppe (ZFTA‑Fusions‑positiv) als in einer anderen Gruppe (PFA) oder im angrenzenden gesunden Gehirn. Dennoch erreichte keines der Medikamente im Tumor Konzentrationen, die mit den in vitro‑wirksamen Werten übereinstimmen, was unterstreicht, wie die Barriere vielversprechende Therapien stillschweigend untergraben kann.
Was das für zukünftige Behandlungen bedeutet
Für Laien ist die zentrale Botschaft klar: Ependymomtumoren stehen nicht alle hinter derselben Art von Gehirn‑Tor. Stattdessen bringt jede molekulare Subgruppe ihre eigene Ausprägung der Blut‑Hirn‑Schranke mit – oft überraschend dicht –, die beeinflusst, wie gut verschiedene Medikamente ihr Ziel erreichen. Durch die Kombination mehrerer Datenebenen aus Patientenproben und Mausmodellen zeigt diese Arbeit, dass das Verstehen und Vermessen dieser gruppenspezifischen Barrieremerkmale entscheidend ist, um klügere klinische Studien zu entwerfen. Anstatt davon auszugehen, dass ein Wirkstoff, der in der Schale Tumorzellen tötet, im Gehirn eines Kindes wirkt, müssen zukünftige Therapien möglicherweise nach der Bauweise der jeweiligen Barriere ausgewählt und gegebenenfalls mit barrieremodifizierenden Strategien kombiniert werden.
Zitation: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
Schlüsselwörter: ependymom, blut‑hirn‑schranke, pädiatrische Hirntumoren, Arzneimittel‑Transport, Multi‑Omics