Clear Sky Science · pt
Diferenças no sangue-encefálico específicas por grupo de ependimoma reveladas por uma abordagem multi-ômica
Por que os guardiões do cérebro importam para crianças com câncer
O cérebro humano é rigidamente protegido por um sistema de segurança natural chamado barreira hematoencefálica, uma camada densa de células que controla estritamente quais substâncias podem entrar no tecido cerebral a partir da corrente sanguínea. Essa barreira é vital para a saúde, mas também torna muito mais difícil levar medicamentos contra o câncer a tumores cerebrais — especialmente em crianças. Este estudo faz uma pergunta aparentemente simples, com grandes implicações clínicas: diferentes subtipos de um tumor cerebral pediátrico chamado ependimoma ficam protegidos por tipos diferentes de barreira, e isso poderia ajudar a explicar por que muitos fármacos falham?
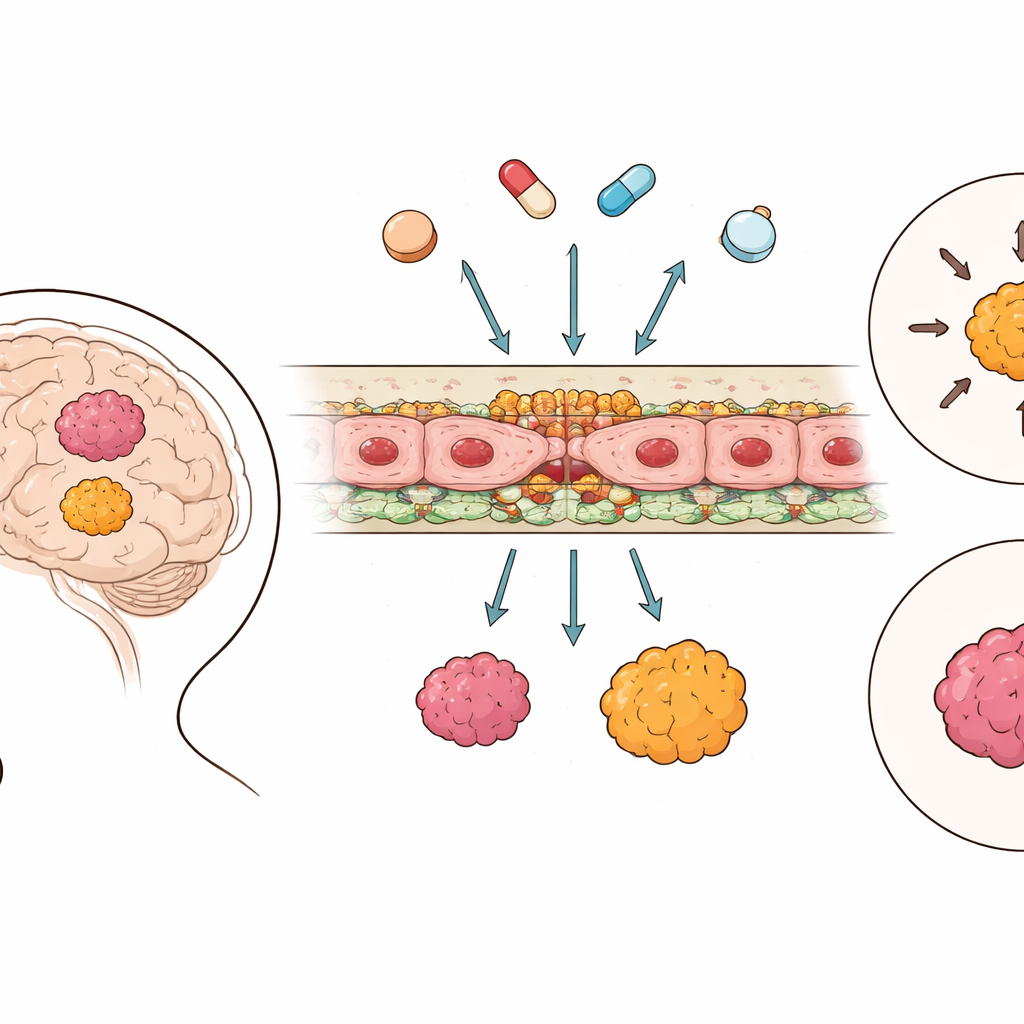
A parede protetora do cérebro
A barreira hematoencefálica é formada por células que revestem os minúsculos vasos cerebrais, unidas por junções especializadas e equipadas com “bombas” moleculares capazes de expelir medicamentos de volta para a corrente sanguínea. Usando dados genômicos em grande escala de 364 tumores de ependimoma e 225 amostras de cérebro saudável, os pesquisadores catalogaram a atividade dos genes envolvidos nessas junções e nos sistemas de transporte. Eles descobriram que, ao contrário de muitos outros cânceres cerebrais, o tecido de ependimoma mostrou na verdade maior atividade de componentes-chave das junções do que o cérebro saudável, sugerindo que a barreira entre o sangue e o tumor é frequentemente mais apertada em vez de mais permeável. Em contraste, bombas de efluxo de drogas e outros transportadores apresentaram padrões mais mistos e específicos por grupo, em vez de uma tendência simples de ligado/desligado.
Não é apenas localização ou idade, mas o tipo de tumor
Em seguida, a equipe investigou se diferenças normais no desenvolvimento ou na anatomia cerebral poderiam explicar esses padrões. Ao treinar pontuações de redes neurais que resumem a atividade dos genes de junção e transportadores, confirmaram características conhecidas em cérebros saudáveis: a “rigidez” da barreira muda com a idade e difere entre regiões como córtex e cerebelo. No entanto, essas tendências relacionadas à idade e à região não se refletiram nos tumores. Entre os principais grupos intracranianos de ependimoma, as pontuações relacionadas à barreira eram semelhantes independentemente do local de origem do tumor no cérebro ou da idade do paciente. Isso aponta para a identidade molecular do próprio tumor — seu subgrupo — como o principal determinante de como a barreira local se comporta.
Focalizando as células da barreira
Medidas em conjunto podem ocultar quais células são realmente responsáveis pela atividade gênica observada. Para resolver isso, os pesquisadores recorreram a sequenciamento de RNA em célula única e em núcleo único de múltiplas coortes de pacientes e a um novo conjunto de validação. Esses dados de maior resolução revelaram que a maioria dos genes relacionados à barreira se concentra em um subconjunto distinto de células dos vasos sanguíneos no microambiente tumoral. Essa subpopulação endotelial especializada apresentou forte expressão de genes clássicos de junção, como CLDN5, e outros marcadores de barreira, enquanto as células tumorais, imunológicas e de suporte expressaram muito pouco. As descobertas foram reforçadas por medidas de proteínas e imagens avançadas, que mostraram essas proteínas realmente revestindo os vasos tumorais, confirmando que as assinaturas genéticas refletem uma barreira estrutural real.
Testando a barreira em modelos murinos
Como novos fármacos costumam ser avaliados em modelos de camundongo antes de chegar aos pacientes, a equipe investigou se xenotransplantes derivados de pacientes de diferentes grupos de ependimoma reproduziam as características humanas da barreira. Nesses modelos, células tumorais de pacientes crescem nos cérebros de camundongos, onde os vasos sanguíneos são em grande parte de origem murina. Análises de RNA e proteína novamente mostraram forte expressão de junções nas células vasculares, mas com algumas diferenças entre modelos e entre tumor e cérebro circundante. Imagens com agentes de contraste e traçadores fluorescentes sugeriram que, no geral, a barreira nesses tumores permanecia relativamente intacta, e que diferenças sutis entre modelos e subgrupos poderiam influenciar com que facilidade moléculas passam do sangue para o tecido tumoral.
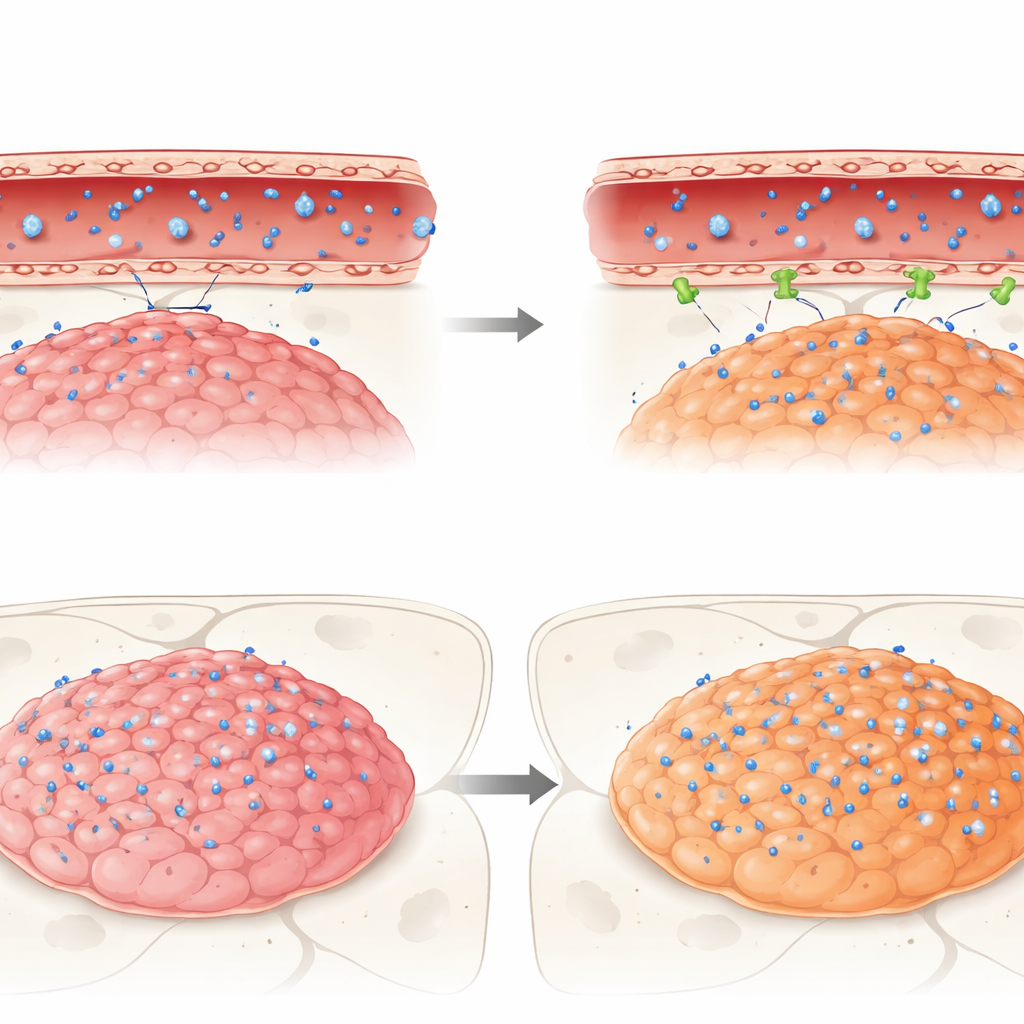
O que acontece quando medicamentos reais tentam atravessar
Por fim, os pesquisadores seguiram a jornada de três medicamentos anticâncer clinicamente relevantes — idasanutlin, temsirolimo e etoposídeo — até esses tumores murinos. Os três foram ativos contra células de ependimoma em cultura, mas em cérebros vivos enfrentaram a barreira. O idasanutlin, embora quimicamente apto a atravessar membranas celulares, atingiu níveis muito baixos tanto no tumor quanto no cérebro normal em comparação com o sangue, sugerindo forte exclusão pela barreira. Em contraste, temsirolimo e etoposídeo, ambos conhecidos por serem expulsos por certas bombas, se acumularam mais em tumores pertencentes a um subgrupo agressivo (ZFTA fusion–positive) do que em outro grupo (PFA) ou no cérebro saudável adjacente. Ainda assim, nenhum dos fármacos alcançou concentrações nos tumores equivalentes às suas doses efetivas observadas in vitro, reforçando como a barreira pode minar silenciosamente terapias promissoras.
O que isso significa para tratamentos futuros
Para um público leigo, a mensagem central é direta: os tumores de ependimoma não estão todos protegidos pelo mesmo tipo de portão cerebral. Em vez disso, cada subgrupo molecular vem com sua própria versão da barreira hematoencefálica — frequentemente surpreendentemente rígida — que determina quão bem diferentes medicamentos conseguem alcançar seus alvos. Ao combinar múltiplas camadas de dados de pacientes e modelos murinos, este trabalho mostra que compreender e medir esses traços específicos por subgrupo da barreira é essencial para projetar ensaios clínicos mais inteligentes. Em vez de presumir que um fármaco que mata células tumorais em uma placa de cultura funcionará no cérebro de uma criança, terapias futuras podem precisar ser selecionadas — e possivelmente combinadas com estratégias que modifiquem a barreira — com base em como os guardiões de cada tumor estão construídos.
Citação: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
Palavras-chave: ependimoma, barreira hematoencefálica, tumores cerebrais pediátricos, administração de fármacos, multi-ômica