Clear Sky Science · nl
Groepsspecifieke verschillen in de bloed-hersenbarrière bij ependymomen onthuld met een multi-omics benadering
Waarom de poortwachters van de hersenen belangrijk zijn voor kinderen met kanker
De menselijke hersenen worden streng beschermd door een natuurlijk beveiligingssysteem, de bloed–hersenbarrière: een nauwsluitende laag cellen die strikt reguleert welke stoffen vanuit de bloedbaan het hersenweefsel binnenkomen. Deze barrière is essentieel voor de gezondheid, maar bemoeilijkt ook het afleveren van kankerbestrijdende medicijnen in hersentumoren—vooral bij kinderen. Deze studie stelt een schijnbaar eenvoudige vraag met grote klinische implicaties: leven verschillende subtypen van een pediatrische hersentumor genaamd ependymoom achter verschillende soorten barrières, en kan dat verklaren waarom veel geneesmiddelen falen?
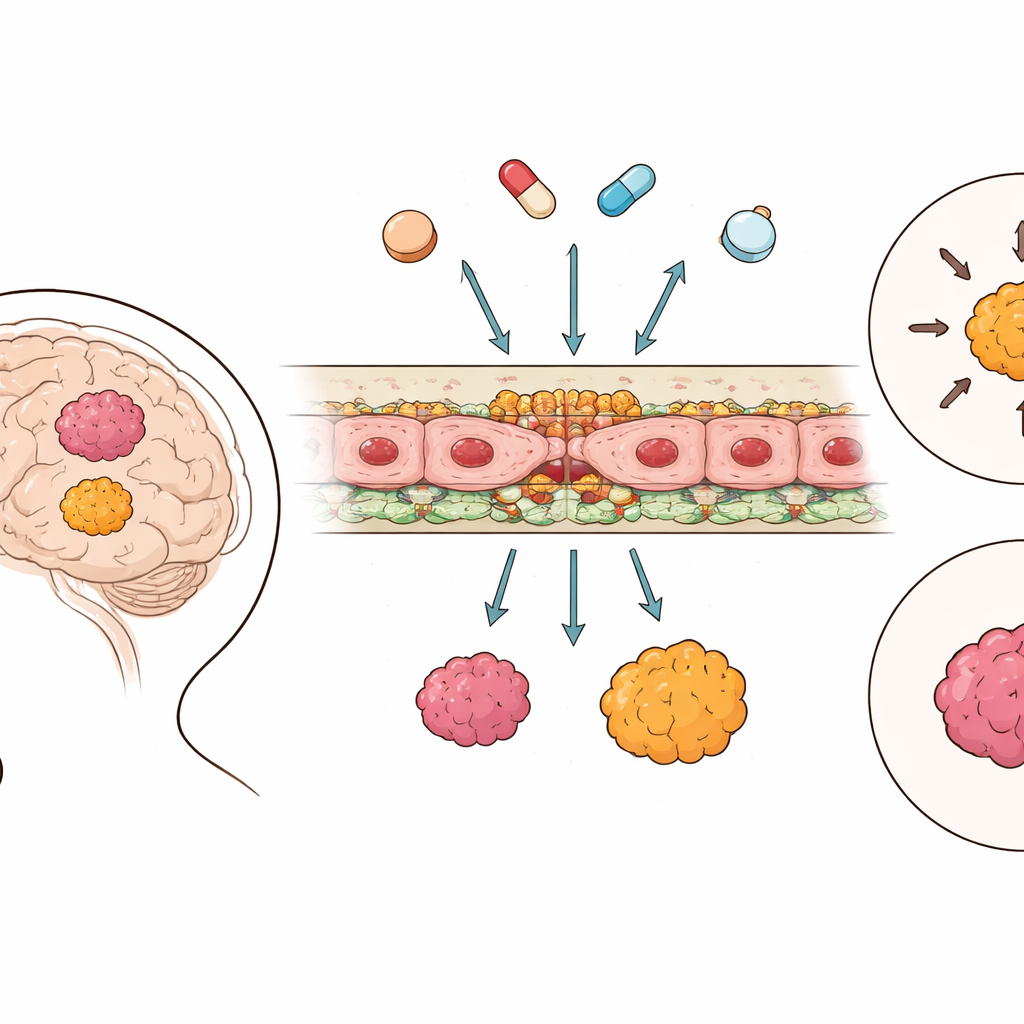
De beschermende muur van de hersenen
De bloed–hersenbarrière bestaat uit cellen die de kleine vaten in de hersenen bekleden, verbonden door gespecialiseerde junctions, en uitgerust met moleculaire "pompen" die medicijnen terug in de bloedbaan kunnen werpen. Met grootschalige genetische gegevens van 364 ependymoomtumoren en 225 monsters van gezond hersenweefsel brachten de onderzoekers de activiteit in kaart van genen die betrokken zijn bij deze junctions en transportsystemen. Ze vonden dat, in tegenstelling tot veel andere hersenkankers, ependymoomweefsel juist een hogere activiteit van belangrijke junctioncomponenten toonde dan gezond hersenweefsel, wat suggereert dat de barrière tussen bloed en tumor vaak strakker in plaats van lekkerder is. Daarentegen volgden drug-effluxpompen en andere transporteurs meer gemengde, groepsspecifieke patronen in plaats van een eenvoudig aan-of-uit patroon.
Niet alleen locatie of leeftijd, maar tumortype
Vervolgens vroeg het team of normale verschillen in hersenontwikkeling of anatomie deze patronen konden verklaren. Door neurale-netwerk-scores te trainen die de activiteit van junction- en transportergen samenvatten, bevestigden ze bekende kenmerken in gezonde hersenen: de strakheid van de barrière verandert met de leeftijd en verschilt tussen regio’s zoals de cortex en het cerebellum. Deze leeftijds- en regiotrends vertaalden zich echter niet naar de tumoren. Binnen de belangrijkste intracraniële ependymoomgroepen leken barrier-gerelateerde scores vergelijkbaar, ongeacht waar in de hersenen de tumor ontstond of hoe oud de patiënt was. Dit wijst erop dat de moleculaire identiteit van de tumor zelf—zijn subgroep—de belangrijkste bepalende factor is voor hoe de lokale barrière zich gedraagt.
Inzoomen op de barrièrecellen
Bulkmetingen kunnen verhullen welke cellen daadwerkelijk verantwoordelijk zijn voor de waargenomen genactiviteit. Om dit te verduidelijken schakelden de onderzoekers over op single-cell en single-nucleus RNA-sequencing uit meerdere patiëntcohorten en een nieuwe validatieset. Deze fijnmazigere gegevens toonden aan dat de meeste barrier-gerelateerde genen geconcentreerd zijn in een onderscheiden subset van bloedvatcellen binnen de tumor-microomgeving. Deze gespecialiseerde endotheliale subpopulatie toonde sterke expressie van klassieke junctiongenen zoals CLDN5 en andere barrièremerkers, terwijl tumorcellen, immuuncellen en ondersteunende cellen weinig tot geen expressie vertoonden. De bevindingen werden versterkt door eiwitmetingen en geavanceerde beeldvorming, die lieten zien dat deze eiwitten fysiek de tumorbloedvaten bekleden, waarmee werd bevestigd dat de genetische signaturen een echte structurele barrière weerspiegelen.
De barrière testen in muismodellen
Aangezien nieuwe medicijnen vaak eerst in muismodellen worden geëvalueerd voordat ze bij patiënten worden getest, onderzochten de onderzoekers of patient-derived xenografts van verschillende ependymoomgroepen menselijke barrièrefuncties reproduceerden. In deze modellen groeien tumorcellen van patiënten in de hersenen van muizen, waarbij de bloedvaten grotendeels muis-afkomstig zijn. Analyse van RNA en eiwit toonde opnieuw sterke junction-expressie in vatcellen, maar met enkele verschillen tussen modellen en tussen tumor en omliggend brein. Beeldvorming met contrastmiddelen en fluorescente tracers suggereerde dat de barrière in deze tumoren over het algemeen relatief intact bleef, en dat subtiele verschillen tussen modellen en subgroepen kunnen beïnvloeden hoe gemakkelijk moleculen van bloed naar tumorweefsel passeren.
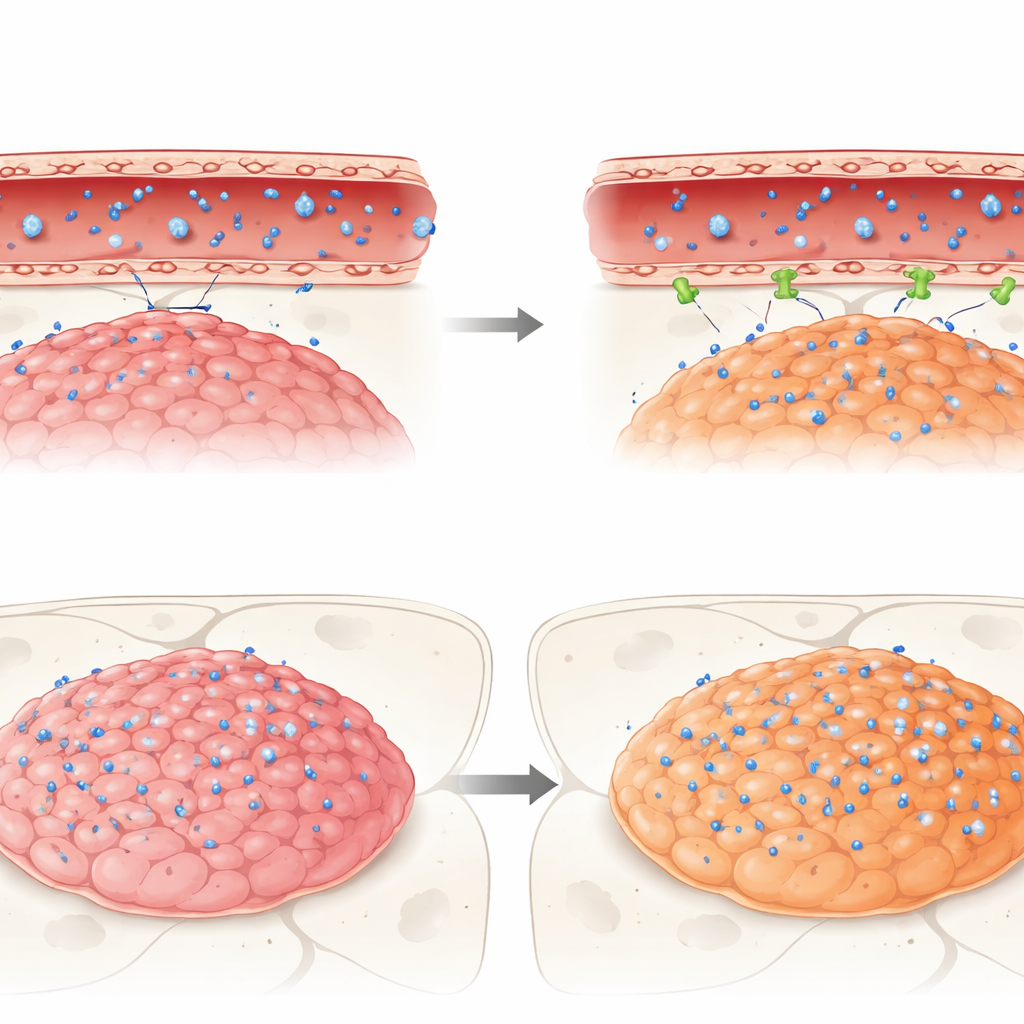
Wat gebeurt er als echte medicijnen proberen over te steken
Ten slotte volgden de onderzoekers de reis van drie klinisch relevante antikanker-medicijnen—idasanutlin, temsirolimus en etoposide—naar deze muizentumoren. Alle drie waren actief tegen ependymoomcellen in kweekschalen, maar in levende hersenen kregen ze te maken met de barrière. Idasanutlin, hoewel chemisch geschikt om celmembranen te passeren, bereikte zeer lage niveaus in zowel tumor als normaal brein vergeleken met het bloed, wat duidt op sterke uitsluiting door de barrière. Daarentegen hoorden temsirolimus en etoposide, beide bekend als substrates van bepaalde pompen, zich meer op te hopen in tumoren behorend tot één agressieve subgroep (ZFTA-fusie–positief) dan in een andere groep (PFA) of het aangrenzende gezonde brein. Toch bereikten geen van de geneesmiddelen concentraties in tumoren die overeenkwamen met hun effectieve niveaus in vitro, wat benadrukt hoe de barrière veelbelovende therapieën stilzwijgend kan ondermijnen.
Wat dit betekent voor toekomstige behandelingen
Voor leken is de kernboodschap eenvoudig: ependymoomtumoren zitten niet allemaal achter hetzelfde type hersenpoort. In plaats daarvan gaat elke moleculaire subgroep gepaard met zijn eigen versie van de bloed–hersenbarrière—vaak verrassend strak—wat bepaalt hoe goed verschillende medicijnen hun doel kunnen bereiken. Door meerdere datalagen van patiënten en muismodellen te combineren, laat dit werk zien dat het begrijpen en meten van deze subgroepspecifieke barrieretreugtigheden essentieel is voor het ontwerpen van slimmere klinische trials. In plaats van aan te nemen dat een medicijn dat tumorcellen in een schaaltje doodt ook werkt in het brein van een kind, moeten toekomstige therapieën mogelijk worden gekozen—en eventueel gecombineerd met barrière-modificerende strategieën—op basis van hoe de poortwachters van elke tumor zijn opgebouwd.
Bronvermelding: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
Trefwoorden: ependymoom, bloed-hersenbarrière, pediatrische hersentumoren, geneesmiddeltoediening, multi-omics