Clear Sky Science · pl
Różnice w barierze krew–mózg zależne od grupy ependymom odkryte dzięki podejściu multi-omics
Dlaczego strażnicy mózgu mają znaczenie dla dzieci z rakiem
Ludzki mózg jest mocno chroniony przez naturalny system ochronny zwany barierą krew–mózg, ciasną warstwę komórek, która ściśle kontroluje, jakie substancje mogą przedostawać się z krwi do tkanki mózgowej. Ta bariera jest niezbędna dla zdrowia, ale utrudnia też dostarczanie leków przeciwnowotworowych do guzów mózgu — szczególnie u dzieci. W tym badaniu postawiono pozornie proste pytanie o istotnym znaczeniu klinicznym: czy różne podtypy pediatrycznego guza mózgu zwanego ependymomą znajdują się za różnymi typami barier i czy to może pomóc wyjaśnić, dlaczego wiele leków zawodzi?
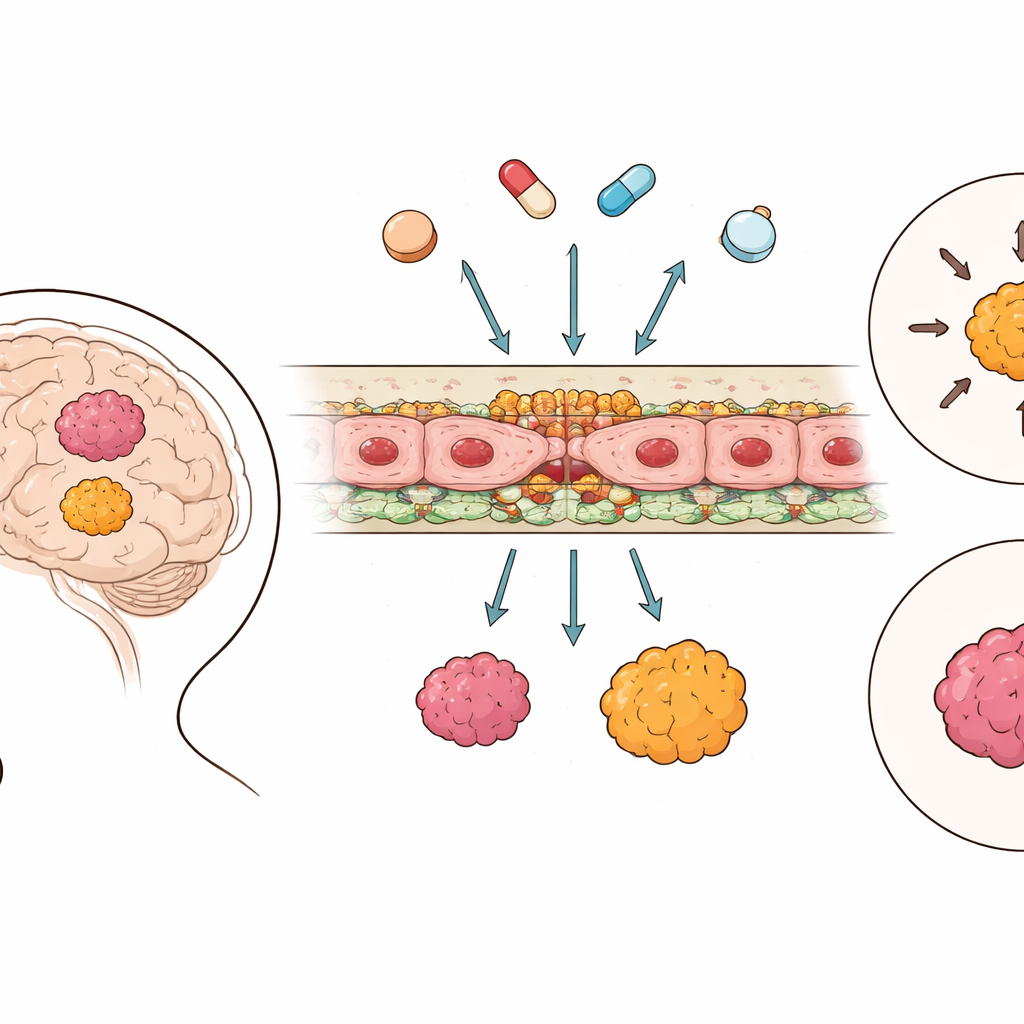
Ochronna ściana mózgu
Bariera krew–mózg zbudowana jest z komórek wyściełających drobne naczynia mózgowe, które są ze sobą szczelnie połączone przez wyspecjalizowane złącza i wyposażone w molekularne „pompki”, potrafiące wyrzucać leki z powrotem do krwi. Wykorzystując duże zbiory danych genetycznych z 364 guzów ependymoma i 225 próbek zdrowego mózgu, badacze sklasyfikowali aktywność genów zaangażowanych w te złącza i systemy transportowe. Stwierdzili, że w przeciwieństwie do wielu innych nowotworów mózgu, tkanka ependymoma wykazywała wyższą aktywność kluczowych składników złączy niż zdrowy mózg, co sugeruje, że bariera między krwią a guzem jest często bardziej szczelna, a nie „przeciekająca”. W przeciwieństwie do tego, pompy wypychające leki i inne transportery wykazywały bardziej zróżnicowane, zależne od grupy wzorce, zamiast prostego trendu włącz/wyłącz.
Nie tylko lokalizacja czy wiek, lecz typ guza
Następnie zespół sprawdził, czy naturalne różnice w rozwoju mózgu lub anatomii mogą wyjaśniać te wzorce. Trenując sieci neuronowe, które podsumowują aktywność genów złączy i transporterów, potwierdzili znane cechy w zdrowym mózgu: szczelność bariery zmienia się z wiekiem i różni się między obszarami, takimi jak kora i móżdżek. Jednak te wiekowe i regionalne trendy nie przenosiły się na guzy. W różnych głównych wewnątrzczaszkowych grupach ependymom, wskaźniki związane z barierą wyglądały podobnie niezależnie od miejsca występowania guza w mózgu czy wieku pacjenta. Wskazuje to, że głównym czynnikiem kształtującym zachowanie lokalnej bariery jest tożsamość molekularna guza — jego podgrupa.
Zbliżenie na komórki tworzące barierę
Pomiary zbiorcze mogą ukrywać, które komórki rzeczywiście odpowiadają za obserwowaną aktywność genów. Aby to rozstrzygnąć, badacze sięgnęli po sekwencjonowanie RNA pojedynczych komórek i jąder z kilku kohort pacjentów oraz nowego zestawu walidacyjnego. Dane o wyższej rozdzielczości ujawniły, że większość genów związanych z barierą koncentruje się w odrębnej podgrupie komórek śródbłonka naczyń krwionośnych w mikrośrodowisku guza. Ta wyspecjalizowana subpopulacja komórek śródbłonkowych wykazywała silną ekspresję klasycznych genów złączy, takich jak CLDN5, i innych markerów bariery, podczas gdy komórki nowotworowe, komórki układu odpornościowego i komórki podporowe wyrażały ich bardzo mało. Odkrycia zostały wzmocnione przez pomiary białek i zaawansowane obrazowanie, które wykazały obecność tych białek fizycznie wyściełających naczynia krwionośne guza, potwierdzając, że sygnatury genetyczne odzwierciedlają rzeczywistą strukturę bariery.
Testy bariery na modelach mysich
Ponieważ nowe leki często są oceniane w modelach mysich przed zastosowaniem u pacjentów, zespół sprawdził, czy ksenografty pochodzące od pacjentów reprezentujące różne grupy ependymom odwzorowują cechy ludzkiej bariery. W tych modelach komórki nowotworowe pacjentów rosną w mózgach myszy, gdzie naczynia krwionośne są w dużej mierze pochodzenia mysiego. Analizy RNA i białek ponownie wykazały silną ekspresję złączy w komórkach naczyniowych, choć występowały pewne różnice między modelami oraz między guzem a otaczającym mózgiem. Obrazowanie z użyciem kontrastów i fluorescencyjnych znaczników sugerowało, że ogólnie bariera w tych guzach pozostaje stosunkowo nienaruszona, a subtelne różnice między modelami i podgrupami mogą wpływać na to, jak łatwo cząsteczki przechodzą z krwi do tkanki guza.
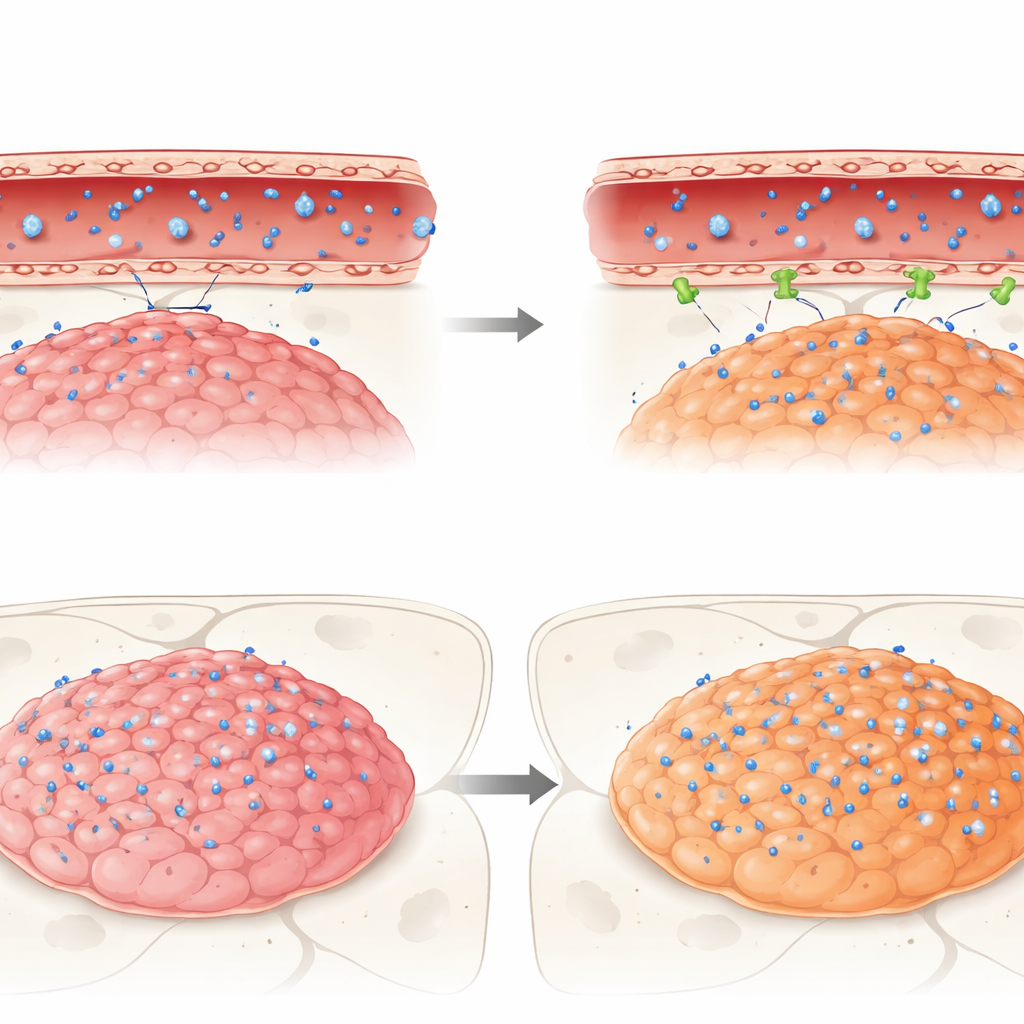
Co się dzieje, gdy prawdziwe leki próbują przejść
Na koniec badacze śledzili drogę trzech klinicznie istotnych leków przeciwnowotworowych — idasanutliny, temsirolimusu i etopozydu — w tych mysich guzach. Wszystkie trzy były aktywne przeciwko komórkom ependymoma w hodowlach, ale w żywych mózgach napotykały barierę. Idasanutlin, choć chemicznie zdolna do przechodzenia przez błony komórkowe, osiągała bardzo niskie poziomy zarówno w guzie, jak i w zdrowym mózgu w porównaniu z krwią, co sugeruje silne wykluczanie przez barierę. Dla odmiany temsirolimus i etopozyd, znane z bycia wypychanymi przez określone pompki, kumulowały się bardziej w guzach należących do jednej agresywnej podgrupy (dodatnia dla fuzyjnego ZFTA) niż w innej grupie (PFA) lub w sąsiadującym zdrowym mózgu. Mimo to żaden z leków nie osiągnął w guzach stężeń odpowiadających ich skutecznym poziomom obserwowanym in vitro, co podkreśla, jak bariera może potajemnie podważać obiecujące terapie.
Co to oznacza dla przyszłych terapii
Dla osoby spoza specjalności główne przesłanie jest proste: guzy ependymoma nie wszystkie znajdują się za tym samym typem bramy mózgowej. Zamiast tego każda molekularna podgrupa ma swoją własną wersję bariery krew–mózg — często zaskakująco szczelną — która determinuje, jak dobrze różne leki mogą dotrzeć do swoich celów. Łącząc wiele warstw danych od pacjentów i modeli mysich, praca ta pokazuje, że zrozumienie i mierzenie tych cech bariery specyficznych dla podgrup jest niezbędne do projektowania inteligentniejszych badań klinicznych. Zamiast zakładać, że lek zabijający komórki guza w hodowli zadziała w mózgu dziecka, przyszłe terapie mogą wymagać doboru — i ewentualnego łączenia z strategiami modyfikującymi barierę — w oparciu o to, jak zbudowani są strażnicy danej zmiany nowotworowej.
Cytowanie: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
Słowa kluczowe: ependymoma, bariera krew–mózg, nowotwory mózgu u dzieci, dostarczenie leków, multi-omics