Clear Sky Science · he
הבדלים במחסום דם-מוח הספציפיים לקבוצות אפנדימומה נחשפו בגישה מולטי-אומיקס
מדוע השומרים של המוח חשובים לילדים עם סרטן
מוח האדם מוגן באופן קפדני על ידי מערכת ביטחון טבעית הנקראת מחסום דם–מוח, שכבה הדוקה של תאים הבוקרת בקפידה אילו חומרים יכולים להיכנס מרקמת הדם אל רקמת המוח. המחסום חיוני לבריאות, אך גם מקשה מאוד על הגעת תרופות לסרטני מוח — בעיקר בילדים. המחקר הזה שואל שאלה שנראית פשוטה אך בעלת השלכות קליניות גדולות: האם תת-סוגים שונים של גידול מוח בילדים הנקרא אפנדימומה נמצאים מאחורי סוגים שונים של מחסומים, והאם זה יכול להסביר מדוע תרופות רבות נכשלות?
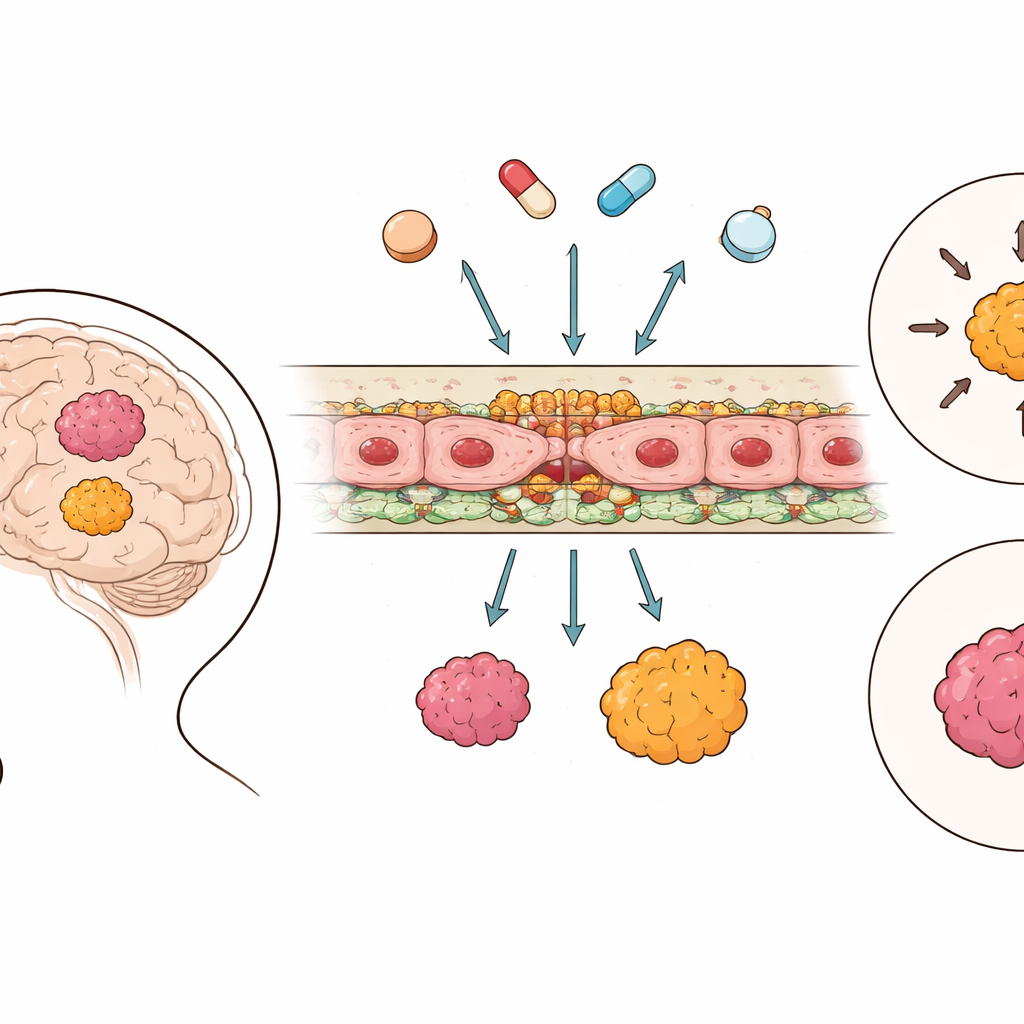
החומה המגוננת של המוח
מחסום דם–מוח נבנה מתאים המצפים כלי דם זעירים במוח וקשורים זה לזה בצמתי מפתח ייחודיים, ומצויד במשאבות מולקולריות היכולות להחזיר תרופות לזרם הדם. באמצעות נתוני גנום בקנה מידה רחב מתוך 364 גידולי אפנדימומה ו-225 דגימות מוח בריא, החוקרים קטלגו את פעילות הגנים המעורבים בצמתי הקישור ובמנגנוני הובלה. הם מצאו שבמפתיע, בניגוד לרבים מסוגי סרטן מוח אחרים, רקמת האפנדימומה הראתה בפועל פעילות גבוהה יותר של רכיבי הצמתים המרכזיים מאשר המוח הבריא, מה שמעיד שהמחסום בין הדם לגידול לעתים קרובות הדוק יותר ולא דולף יותר. לעומת זאת, משאבות הוצאה וטרנספורטרים אחרים הראו דפוסים מעורבים ותלויי-קבוצה במקום מגמה פשוטה של דלק/כיבוי.
לא רק מיקום או גיל — אלא סוג הגידול
בהמשך, הצוות בדק האם הבדלים נורמליים בהתפתחות או באנאטומיה של המוח עשויים להסביר את הדפוסים האלה. על ידי אימון ציוני רשתות עצביות המסכמים את פעילות גני הצמתי והטרנספורטר, הם אישרו תכונות ידועות במוחות בריאים: ההידוק של המחסום משתנה עם הגיל ומשתנה בין אזורים כגון הקורטקס והצרבלום. עם זאת, מגמות גיליות ואזוריות אלה לא המשיכו לגידולים. בין קבוצות האפנדימומה התוך-גולגולתיות העיקריות, ציוני הקשורים למחסום נראו דומים ללא תלות במקום הופעת הגידול במוח או בגיל המטופל. זה מרמז שזהות מולקולרית של הגידול — תת-הקבוצה שלו — היא הגורם העיקרי המעצב את אופן התנהגות המחסום המקומי שלו.
התקרבות לתאי המחסום
מדידות עיבוד-כולל יכולות להסתיר אילו תאים אכן אחראים על פעילות הגנים הנצפתה. כדי לפתור זאת, החוקרים השתמשו ברצף RNA ברמת תא יחיד וגרעין יחיד ממספר קוהורטים של מטופלים ובסט אימות חדש. נתונים חדים יותר אלה חשפו שרוב הגנים הקשורים למחסום מרוכזים בתת-אוכלוסייה מובחנת של תאי כלי דם בסביבה המיקרו-טומוראלית. תת-אוכלוסייה אנדותלית מיוחדת זו הראתה ביטוי חזק של גני צמתי קלאסיים כגון CLDN5 וסמנים מחסום נוספים, בעוד שתאי הגידול, תאי מערכת החיסון ותאי תמיכה הביעו מעט מאוד. הממצאים נתמכו במדידות חלבון ובהדמיה מתקדמת, שהראו כי חלבונים אלה באמת מצפים את כלי הדם של הגידול, ואישרו שהחתימות הגנטיות משקפות מחסום מבני אמיתי.
בדיקת המחסום במודלים עכבריים
מכיוון שתרופות חדשות מוערכות לרוב במודלים עכבריים לפני הגעתן למטופלים, הצוות בחן האם זינוקראפטים נגזרים ממטופלים של קבוצות אפנדימומה שונות משחזרים תכונות מחסום אנושיות. במודלים אלה, תאי גידול ממטופלים גדלים במBrains של עכברים, שבהם כלי הדם הם ברובן ממקור עכברי. ניתוחי RNA וחלבון הראו שוב ביטוי חזק של צמתים בתאי כלי הדם, אך עם כמה הבדלים בין המודלים ובין הגידול והמוח הסובב. הדמיה עם סוכני ניגוד ומסילות פלואורסצנטיות הציעה שבאופן כללי המחסום בגידולים אלה נשאר די שלם, וששוני עדין בין מודלים ותת-קבוצות יכול להשפיע על קלות מעבר מולקולות מן הדם אל רקמת הגידול.
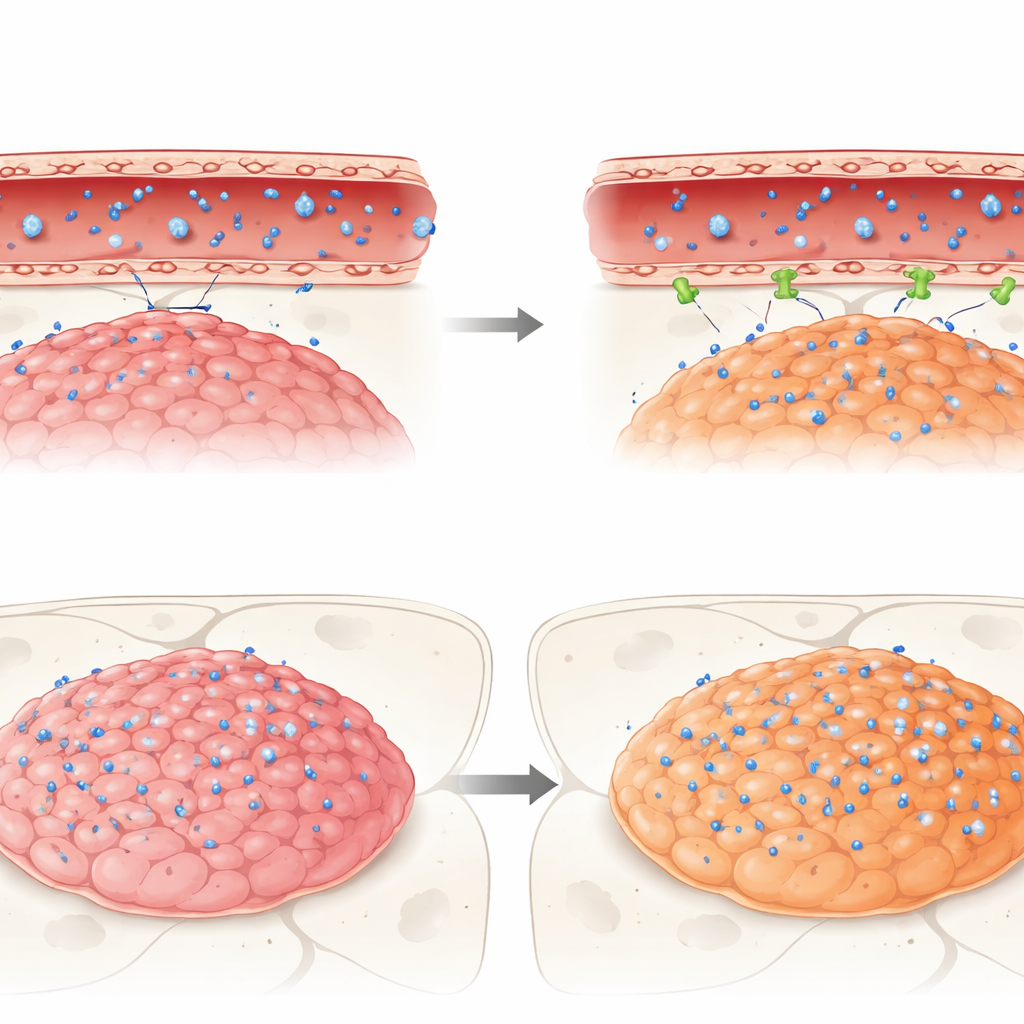
מה קורה כשתרופות אמיתיות מנסות לעבור
לבסוף, החוקרים עקבו אחר מסלול של שלוש תרופות אנטי-סרטניות בעלות רלוונטיות קלינית — אידסאנאטלין, טמסירולימוס ואתופוסיד — אל תוך גידולי העכבר האלה. שלושתן היו פעילות כנגד תאי אפנדימומה בעיונות, אך במוחות חיים הן נתקלו במחסום. אידסאנאטלין, למרות התאמה כימית לחציית ממברנות תא, הגיע לרמת ריכוז נמוכה מאוד הן בגידול והן במוח הרגיל לעומת הדם, מרמז על הוצאה חזקה על ידי המחסום. לעומת זאת, טמסירולימוס ואתופוסיד, שניהם ידועים כמיוצאים על ידי משאבות מסוימות, הצטברו יותר בגידולים המשתייכים לתת-קבוצה אגרסיבית אחת (חיובית לשחלוב ZFTA) מאשר בקבוצה אחרת (PFA) או במוח הבריא השכן. עם זאת, אף אחד מן התרופות לא הגיע בריכוזים בגידולים שתואמים את רמות היעילות שנראו במבחנה, מה שמדגיש כיצד המחסום יכול לחבל בשקט בטיפולים מבטיחים.
מה משמעות הדבר לטיפולים עתידיים
לאנשי הקהל הכללי, המסר המרכזי פשוט: גידולי אפנדימומה אינם כולם מאחורי אותו סוג גדר מוחית. במקום זאת, לכל תת-קבוצה מולקולרית יש את הגרסה שלה של מחסום דם–מוח — לעתים קרובות מפתיעה בהידוקו — אשר מעצבת עד כמה תרופות שונות יכולות להגיע ליעדיהן. על ידי שילוב שכבות רבות של נתונים ממטופלים וממודלים עכבריים, עבודה זו מראה שהבנת ומדידת התכונות הספציפיות של המחסום בכל תת-קבוצה היא חיונית לתכנון ניסויים קליניים חכמים יותר. במקום להניח שתרופה שהורגת תאי גידול בעיונות תעבוד במוח של ילד, טיפולים עתידיים עשויים להידרש להיבחר — ואולי גם להיות משולבים עם אסטרטגיות לשינוי המחסום — על בסיס האופן שבו שומרי השער של כל גידול בנויים.
ציטוט: Sundheimer, J.K., Benzel, J., Federico, A. et al. Ependymoma group-specific blood-brain barrier differences uncovered by a multi-omics approach. Sci Rep 16, 12061 (2026). https://doi.org/10.1038/s41598-026-47499-2
מילות מפתח: אפנדימומה, מחסום דם-מוח, גידולי מוח בילדים, העברת תרופות, מולטי-אומיקס